Глицин (гликокол, a-аминоуксусная).
СН2 – СООН
|
NH2
Единственная оптически неактивная аминокислота. Является одной из самых распространенных, характерна для желатины. Имеет сладкий привкус. Является предшественником при биосинтезе пуриновых оснований, порфириновой части гемоглобина, хлорофилла, геминовых ферментов. Участвует в образовании клеточных стенок бактерий. Функционирует как тормозной медиатор в спинном мозге (ствол мозга, спинной мозг).
Аланин (a-аминопропионовая кислота).
a
СН3 – СН – СООН
|
NH2
Играет большую роль в обмене азотистых соединений, исходный продукт для синтеза каротиноидов, каучука, жиров, углеводов.
Валин (a-амино-b-метилмасляная кислота).
b a
СН3 – СН – СН – СООН
| |
CH3 NH2
Обладает способностью к гидрофобным взаимодействиям. Участвует в синтезе алкалоидов, циклопептидов, пантотеновой кислоты, пенициллина.
Серин (a-амино-b-оксипропионовая кислота)
b a
СН2 – СН – СООН
| |
OH NH2
Входит в состав фосфолипидов (фосфатидилсеринов), полипептидов брадикинина, каллидина, участвует в построении активных центров ряда протеолитических ферментов, синтезе аминоспирта сфингозина (компонента сфинголипидов). В таких белках как казеин молока и вителлин яичного желтка содержится в виде сложного эфира – серинфосфорной кислоты, которая играет важную роль в метаболизме молодого растущего животного организма. У растений образуется в ходе фотодыхания из глицина.
L-Метионин (a-амино- g- метилтиомасляная кислота)
g b a
СН2 – СН2 – СН – СООН
| |
S – CH3 NH2
Является одним из основных доноров метильных групп и серы. Используется при биосинтезе углеводов клеточных стенок растений, холина, адреналина, креатина, стеринов, тиамина, серосодержащих аминокислот (гомоцистемна, цистенина, цистина). Данной аминокислотой богат белок молока – казеин. Как липотропный фактор метионин используется при лечении атеросклероза. Метионин при распаде дает характерные продукты гниения – Н2S, RSH (меркаптаны), характерные для изолированных тканей и для кишечника.
L-Цистеин (a-амино-b-тиопрорионовая кислота).
b a
СН2 – СН – СООН
| |
SH NH2
Является серосодержащей аминокислотой, источник серы. Является восстанавливающим агентом в связи с наличием сульфгидрильной SН-группы. За счет SН принимает участие в образовании дисульфидных связей –S-S- между полипептидными цепями или внутри одной цепи, что важно в образовании третичной структуры белковой молекулы. Из двух молекул цистеина при окислении получается цистин, легко происходит обратный переход, причем в белках цистин преобладает над цистеином. Цистин и цистеин характерен для фибриллярных белков (волосы, ногти, рога, копыта). Входит в состав трипептида глютатиона, в виде амина в кофермент А, входит в состав активных центров многих ферментов.
Лейцин, изолейцин (aаминоизокапроновая кислота).
g b a
СН3 – СН – СН2 – СН – СООН
| |
CH3 NH2
Лейцин впервые выделен в 1819 г. из сыра. Обнаружен также в составе многих других белков, например в белках яиц (овальбумин), миозине мышц, в фибриногене крове и белках молока.
Изолейцин – важная аминокислота, впервые выделен из фибрина.
Обе аминокислоты плохо растворимы в воде, способны к гидрофобным взаимодействиям.
Треонин (a-амино-b-оксимасляная кислота).
g b a
СН3 – СН – СН – СООН
| |
OH NH2
Участвует в синтезе витамина В12, антибиотика актиномицина Д.
Диаминомонокарбоновые аминокислоты
Лизин (a, e-диаминокапроновая кислота)
a
Н2С – (СН2)3 – СН – СООН
| |
NH2 NH2
Содержится почти во всех белках, особенно много его в белках молок рыб, относящихся к протаминам и гистонам. Является исходным продуктом при синтезе алкалоидов (анабазин, никотин, лупанин, кониин). Участвует своей e-аминогруппой в образовании комплекса между белковой частью фермента и коферментом, например в биотин-зависимых ферментах.
Содержится в незначительных количествах в белках семян злаковых, особенно кукурузы, что существенно обесценивает кормовые свойства последней.
Аргинин (a-амино-S-гуанидилвалериановая кислота).
a
H2N – C – NH – (CH2)3 – CH – COOH
|| |
NH NH2
Играет большую роль в белковом обмене, участвуя в синтезе мочевины, креатина. Входит в большом количестве в состав основных белков-гистонов и протаминов, в связи с чем его много в белках рыбьих молок.
Моноаминодикарбоновые аминокислоты
Аспарагиновая кислота (a-аминоянтарная кислота).
a
НООС – СН2 – СН – СООН
|
NH2
Очень плохо растворима в воде, ее раствор имеет кислую реакцию. Содержится в больших количествах во всех растительных белках и играет важную роль в обмене веществ у растений и животных, в частности, принимая участие в реакциях переаминирования, образовании мочевины, креатина, циклопептидов. При ее декарбоксилировании образуется a- или b-аланин, необходимый для синтеза карнозина, ансерина и коэнзима А (Ко А). Амид аспарагиновой кислоты – аспарагин накапливается в очень больших количествах при прорастании семян бобовых растений, особенно в темноте, из-за отсутствия углеводов или при избытке аммиака. Аспарагин обнаружен в плазме крови и в составе некоторых животных белков (инсулин, гемоглобин, мпиоглобин и др.). У человека и животных аспарагин, как и аспарагиновая кислота, активно участвует в реакциях переаминирования, служит предшественником при синтезе пуриновых и пиримидиновых оснований, никотиновой кислоты, у растений является запасной и транспортной формой азота.
Глутаминовая кислота (a-аминоглутаровая кислота).
a
НООС – СН2 - СН2 – СН – СООН
|
NH2
В водных растворах дает кислую реакцию. Входит в состав витамина фолиевой кислоты, глутатиона. Наряду с аспаргиновой кислотой играет первостепенную роль в аминокислотном обмене, активно участвуя в реакциях переаминирования, дезаминирования, прямого аминирования. При декарбоксилировании глутаминовой кислоты образуется g-аминомасляная кислота, имеющая большое значение в метаболизме мозга, усиливающая, в частности, процессы торможения, и d-аминолевулиновая кислота, участвующая в синтезе порфиринов. Амид глутаминовой кислоты – глутамин, является транспортной формой азота у животных и растений, исходным соединением при синтезе пуриновых и пиримидиновых оснований, никотиновой кислоты. Мононатриевая соль глутаминовой кислоты служит вкусовой приправой, обладая вкусом и запахом куриного бульона.
Диаминодикарбоновые аминокислоты
Цистин – дицистеин (a, a¢-диамино-b, b¢-дитиопропионовая кислота).Образуется из двух молекул цистеина за счет дисульфидной сшивки (- S- S-).
Циклические аминокислоты.
Фенилаланин (a-амино-b-фенилпропионовая кислота).
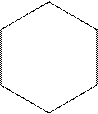 a
a
- CН2 – СН - СООН
 |
|
NH2
Участвует в биосинтезе флавоноидов, алкалоидов. Обладает способностью к гидрофобным взаимодействиям. Обуславливает ксантопротеиновую реакцию на белки.
Тирозин (a-амино-b-парагидроксифенилпропионовая кислота).
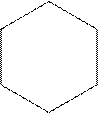 a
a
 - CH2 – CH - COOH
- CH2 – CH - COOH
|
OH
|
OH
Является исходным субстратом для синтеза гормонов (тироксин, норадреналин, адреналин), алкалоидов (морфин, кодеин, папаверин). Окисление тирозина под влиянием тирозиназы приводит к образованию меланинов (пигмент кожи, волос, перьев).
Триптофан (a-амино-b-индолилпропионовая кислота).
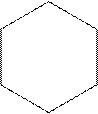 b a
b a

 - CH2 – CH – COOH
- CH2 – CH – COOH

 |
|
NH2
 |
N
Бедны триптофаном семена злаков. При кислотном гидролизе белков распадается. Триптофан служит исходным продуктом для синтеза никотиновой кислоты (витамин РР), гетероауксина.
Гистидин (a-амино-b-имидазолилпропионовая кислота).
b a


 N C – CH2 – CH – COOH
N C – CH2 – CH – COOH

 |
|
NH2

 HC CH
HC CH
N
Принадлежит к группе основных аминокислот – в водных растворах дает щелочную реакцию. Значительное количество гистидина содержится в глобине – белковом компоненте гемоглобина крови. Входит в активные центры некоторых протеолитических ферментов.
Пролин (пирролидин 2-карбоновая кислота).


 H2C CH2
H2C CH2



 H2C CH - COOH
H2C CH - COOH
NH
Является иминокислотой. Хорошо растворим в спирте. Особенно велико содержание пролина в белках семян злаков (проламины), в коллагене, эластине и белке эмали зубов. Входит в состав ряда антибиотиков.
Оксипролин (4-гидроксипирролидин-2-карбоновая кислота).


 HOHC CH2
HOHC CH2



 H2C CH - COOH
H2C CH - COOH
NH
Является иминокислотой.
 2015-10-14
2015-10-14 7864
7864
