Реакции горения – цепные, протекают через образование и взаимодействия молекул с активными центрами (АЦ) – свободными атомами и радикалами.
Механизмы реакций:
Горение водорода. Суммарное уравнение – 2Н2 + О2 = 2Н2О
Основные элементарные реакции:
1. Реакции образования АЦ (зарождение цепей):

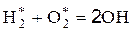
2. Реакции продолжения цепи (получение конечного продукта):
OH + H2 = H2O + H
3. Реакции разветвления цепи:
H + O2 = OH + O,
O + H2 = OH + H
H + H2O = 2 OH
4. Обрыв цепей («гибель» активных центров) на стенке:
H = Hадс, H + Hадс = H2
O = Oадс, O + Oадс = O2
5. Обрыв цепей в объеме:
H + OH + M = H2O + M*,
|
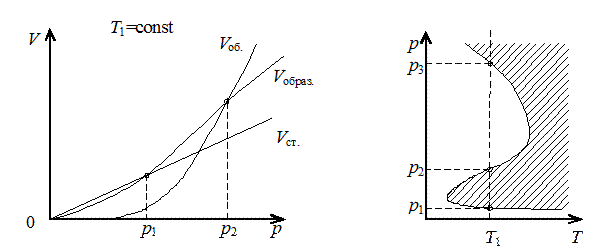
V ст = const²× p,
V об = const²¢× p 3.
Условие воспламенения газовой смеси:
Скорость образования активных центров больше скорости их исчезновения на стенке и в объеме. V образ.> (V ст; V об)
Горение СО.
Суммарное уравнение – 2СО + О2 = 2СО2
Основные элементарные реакции:
1. Образование активных центров благодаря наличию примеси водорода
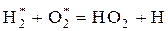 ,
,
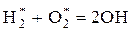 .
.
2. Реакция продолжения цепи
OH + CO = CO2 + Н
3. Реакции разветвления цепей
Н + О2 = ОН+ О
О + Н2О = 2ОН
4. Реакции обрыва цепей в объеме
О + СО + М = СО2 + М*
О + О2 + М = 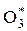 + М
+ М
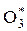 + СО = СО2 + О2
+ СО = СО2 + О2
Особенность кинетики горения СО. – протекание ее лишь в присутствии хотя бы
микропримесей водорода или водяного пара.
Для интервала температур 1500 – 2500 °С кинетическое уравнение для скорости горения СО
V = k [CO]×[H2O]нач, при [H2O]нач £ 3 об.%.
Горение СН4.
Суммарное уравнение – 2СН4 + О2 = 2СО + 4Н2
Основные элементарные реакции:
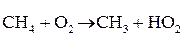
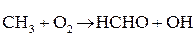
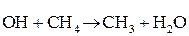
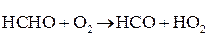
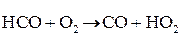
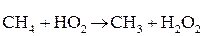
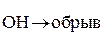
Факторы, влияющие на скорость горения газов:
1. Температура.
Увеличивает скорость активации, расширяет область воспламенения.
2. Примеси (в том числе инертные газы).
Замедляют диффузию активных частиц к стенкам, уменьшают V ст и Р1.
Ускоряют гибель в объеме, увеличивают V об , уменьшают Р2
3. Форма, размер сосуда, адсорбционные свойства материала сосуда
Изменяют скорость диффузии АЦ и скорость адсорбции АЦ на стенках.
 2020-01-14
2020-01-14 530
530








