Тема 4. Использование лабораторных животных в диагностических исследованиях. Цели использования лабораторных животных в вирусологии
Задание к следующему занятию
Подведение итогов занятия
Задания
1. Найти под световым микроскопом в препаратах и зарисовать:
а) цитоплазматические тельца-включения;
б) внутриядерные тельца-включения;
в) вирионы вируса оспы в окраске по Морозову.
2. Ознакомиться с устройством и принципом работы электронного микроскопа.
3. Дешифрировать электронные микрофотографии вирионов разных вирусов (дать их схематический рисунок).
Самостоятельная работа студентов
Студенты знакомятся с устройством светового, люминесцентного и электронного микроскопов (в лаборатории), зарисовывают схему строения электронного микроскопа. Знакомятся с подготовкой препаратов для электронной микроскопии. Просматривают готовый препарат в люминесцентном микроскопе. Зарисовывают схему прямого и непрямого метода РИФ.
Контрольные вопросы:
|
|
|
1. Устройство электронного микроскопа.
2. Методы подготовки препаратов для просмотра в электронном микроскопе.
3. Люминесцентную микроскопию (РИФ) прямой и непрямой методы.
4. Значение электронной и люминесцентной микроскопии в вирусологических исследованиях.
Цель занятия: ознакомить студентов с требованиями к видам лабораторных животных, их карантинированием, содержанием, кормлением, мечением.
Оборудование и материалы: набор инструментов в стерилизаторе (ножницы, иглы, шприцы, пинцеты, корнцанги), лабораторные животные, ватные спиртовые тампоны краски для мечения, эфир, ксилол, мультимедийное оборудование, плакаты и презентации MS Office Power Point по теме занятия.
Объяснение преподавателя: Большинство вирусов разных таксономических групп могут быть отличимы друг от друга на основе патогенности для лабораторных животных разных видов или возраста.
4.1 Виды лабораторных животных. Наиболее широко в вирусологических лабораториях применяют мышей, белых крыс, кроликов, морских свинок, хомяков, цыплят. У молодых мышей экспериментально воспроизводят грипп, альфа- и флавивирусные инфекции, ящур (на новорожденных мышатах) и др. Они восприимчивы ко многим вирусам, их легко разводить и с ними удобно работать. Лучше использовать мышей инбредных линий, так как они почти одинаково реагируют на тот или иной вирус. У крыс также создают инбредные линии, но эти животные более устойчивы к определенным вирусным инфекциям, чем мыши. Онкогенность некоторых вирусов широко изучают на золотистых хомячках. Для вирусологических опытов обычно используют гладкошерстных морских свинок массой 250–300 г.
|
|
|
Ту или иную инфекцию иногда изучают на животных нескольких видов, обладающих разной чувствительностью к данному вирусу, что позволяет дифференцировать вирусы, вызывающие клинически сходные симптомы болезни (например, ящур, везикулярный стоматит, везикулярная экзантема и везикулярная болезнь свиней).
По генетическим качествам лабораторных животных делят на четыре группы:
1) животные смешанного происхождения, полученные от разных животноводов, такие животные гетерогенны;
2) животные, полученные непосредственно из одного источника, однако генетически такие животные вариабельны;
3) инбредные линии животных. Их получают в результате спаривания брата с сестрой или родителей с детьми по крайней мере не менее 20 поколений. При таком методе разведения достигается все возрастающая степень гомозиготности.
4) однородные гибриды F1. Высокая степень гетерозиготности, характерная для каждого гибрида, связана здесь с генетическим однообразием, которое соответствует степени гомозиготности родительских линий. Как правило, однородные гибриды F1 менее изменчивы, чем обе родительские линии. Животные-мутанты имеют отдельно выраженный наследственный фактор, который обусловливает видимое отклонение от нормальной формы.
Отрицательная сторона выделения вируса на лабораторных животных – возможность диагностических ошибок вследствие активации скрытого вирусоносительства. В этом случае развитие симптомов болезни после введения материала не следствие действия введенного вируса, а результат самой процедуры, нарушающей предшествующее равновесие в организме. В это время проявляется вирус или другой инфекционный агент, длительно персистирующий в организме. Выражается это резкими неврологическими симптомами (повороты вдоль длинной оси тела).
Наличие скрытой вирусной инфекции может также выражаться уменьшением или исчезновением чувствительности животных к исследуемому вирусу вследствие явления интерференции. Возможен и противоположный эффект, а именно – явление синергизма в действии вирусов, что дает иногда результаты, трудные для правильной интерпретации.
Для некоторых вирусологических работ, например при выделении вируса с невыясненными болезнетворными свойствами, необходимо использовать гнотобиотов. Термин «гнотобиоты» объединяет две категории животных: безмикробных (стерильных), не содержащих никаких жизнеспособных микробов, и гнотофор – носителей одного (моногнотофоры), двух (дигнотофоры) или более (полигнотофоры) микроорганизмов. В настоящее время безмикробные животные по динамике роста делятся на три группы: I – обезьяны, поросята, цыплята растут лучше обычных животных или наравне с ними; II – крысы, мыши, собаки, кошки растут наравне с обычными животными; III – морские свинки, кролики, козлята, ягнята растут хуже обычных животных.
Стерильных птиц получают посредством инкубации яиц со стерильной скорлупой в стерильном инкубаторе, лабораторных животных – путем кесарева сечения или гистерэктомии. Содержат животных в стерильных изоляторах. Воздух, вода и корм должны быть стерильными.
Особое значение среди гнотобиотов занимают СПФ-животные (Specific pathogen free), которые свободны только от патогенных микроорганизмов. В их организме имеются все необходимые для нормальной жизнедеятельности бактерии и вирусы, которые в совокупности создают группу так называемой резидентной (полезной) микрофлоры. В настоящее время получены лабораторные СПФ-животные – крысы, морские свинки, кролики, поросята, птицы и др.
4.2 Цели использования лабораторных животных. В настоящее время лабораторных животных используют в вирусологии для:
|
|
|
– обнаружения вируса в патматериале;
– первичного выделения вируса из патматериала;
– накопления вирусной массы;
– поддержания вируса в лаборатории в активном состоянии;
– титрования вируса;
– получения гипериммунных сывороток;
– в качестве тест-объекта в реакции нейтрализации.
В вирусологии используют кроликов, морских свинок, белых крыс, белых мышей, золотистых хомячков. Однако только некоторые вирусы удается культивировать на животных перечисленных видов. Во многих случаях для тех же целей используют других чувствительных к данному вирусу животных: кур, голубей, котят, щенков и т. д. Так, биопробу при диагностике оспы птиц ставят на курах, оспы овец – на овцах, чумы свиней – на подсвинках.
4.3 Требования к лабораторным животным. Комплектуя группы животных для вирусологических исследований, необходимо выполнять следующие требования:
– животное должно быть чувствительным к данному вирусу;
– возраст его имеет большое значение для культивирования многих вирусов. Большинство вирусов лучше размножается в организме молодых и даже новорожденных животных. Например, для биопробы на бешенство и ящур используют мышей-сосунов, на ларинготрахеит птиц – цыплят. Но в то же время заражение взрослых кроликов вирусом болезни Ауески ведет к появлению ярких и специфичных клинических признаков заболевания;
– стандартная чувствительность достигается подбором животных определенного возраста и одинаковых по массе;
– лабораторные животные должны быть здоровы. Животные, поступающие в виварий вирусологической лаборатории, должны быть привезены из благополучного по инфекционным заболеваниям хозяйства. Их содержат изолированно, т. е. в карантине (белых мышей и крыс 14 дней, а остальных животных 21 день). В этот период за животными ведут ежедневное клиническое наблюдение. При подозрении на наличие инфекционной болезни животных подвергают лабораторному исследованию. В случае установления инфекционного заболевания среди животных всю поступившую партию уничтожают.
|
|
|
4.4 Содержание лабораторных животных. Виварий для лабораторных животных должен иметь основное помещение для животных, моечную (с боксом, сушильными и стерилизационными установками), кухню для приготовления корма с одним по крайней мере столом, оборудованным для приготовления корма, и холодильником для скоропортящихся продуктов, кладовую, операционную, гардероб и санитарное помещение для обслуживающего персонала. Помещения должны быть чистыми. Стены и полы легко дезинфицируемыми. Запасы корма следует хранить в специальных помещениях. В местах содержания опытных животных желательно иметь гигрометр и термометр.
Мышей, крыс, хомяков и морских свинок в период опыта рекомендуется содержать в стеклянных банках с крышкой из проволочной сетки или перфорированного листового железа. Это облегчает наблюдение за ними, а банки легко чистить и дезинфицировать. Можно содержать животных в металлических клетках, которые также легко дезинфицировать.
В качестве подстилки применяют материалы, которые адсорбируют влагу и могут быть использованы животными для постройки гнезда: стружку для мышей, крыс, хомяков, морских свинок, хорьков, кур; опилки для крупных мышей, крыс, хомяков, хорьков, кур; солому для хомяков, морских свинок, кроликов, собак, кур; мякину для мышей, крыс; сено для мышей, крыс, хомяков, хорьков, кур; песок для кур. Следует использовать такую подстилку, которая образует как можно меньше пыли, так как последняя может привести к заболеванию органов дыхания. Любую подстилку необходимо предварительно стерилизовать при 100 °С в течение 30 мин.
Помещения для лабораторных животных периодически дезинфицируют, особенно перед размещением новой партии животных. Это относится и к предметам ухода за животными (лопаты, скребки, метелки и др.), которые соприкасаются с навозом и различными отбросами из помещения. После окончания каждого опыта клетки обязательно обрабатывают дезинфицирующими растворами, чему должна предшествовать чистка как клеток, так и помещения.
Посуду для корма и воды ежедневно смачивают дезинфицирующим раствором, после чего моют и споласкивают чистой водой. Помещения обрабатывают 1% раствором едкого натра, который используют в течение суток. Дезковрики пропитывают свежим раствором каждые 2 дня. Для дезинфекции предметов ухода, мытья полов и посуды рекомендуется использовать 3% раствор хлорамина, который должен быть применен в течение 2 ч. В виварии необходимо уничтожать вредителей: мух, комаров, блох, власоедов, клещей, вшей, муравьев, мышей, крыс.
Лабораторных животных размещают так, чтобы, с одной стороны, было обеспечено функционирование всех систем организма в пределах физиологической нормы, с другой – исключено взаимное перезаражение и распространение инфекции за пределы вивария. Животных содержат в виварии с учетом их физиологической потребности в освещенности и температуре. Так, мышам, крысам нужны полумрак и температура воздуха около 20 °С, морским свинкам, кроликам и курам – дневной свет и температура в пределах 16–23, 14–18 и не ниже 0°С соответственно. Плотность посадки должна составлять примерно 1 г массы лабораторных животных на 1 см2 дна клетки. Животных обеспечивают регулярным и полноценным кормлением и постоянно питьевой водой.
Если виварий один, зараженных животных содержат изолированно от здоровых и с последних начинают уборку помещения и кормление. Для ухода за зараженными животными используют отдельный инвентарь и кормушки. Лучше иметь два вивария: для содержания здоровых и зараженных животных.
Обслуживающий персонал при работе в виварии пользуется спецодеждой: халатом, резиновыми перчатками, фартуком, непромокаемой обувью. В виварии ежедневно дезинфицируют инвентарь и проводят влажную уборку с применением дезинфицирующих веществ. По окончании эксперимента клетки дезинфицируют, погибших животных обезвреживают сжиганием в печах или автоклавированием.
В группу для проведения опыта подбирают животных с одинаковыми показателями массы, температуры, состава крови и т. д. От этого в значительной степени зависит успех выделения, титрования и пассирования вируса. При этом учитывают восприимчивость животных к различным вирусам. Отобранных животных метят, распределяют по банкам или клеткам, отмечают дату постановки опыта, его номер, заражающую или профилактическую дозу препарата и, если необходимо, как мечены животные. Последнее важно, когда в одной банке или клетке находятся животные нескольких групп.
Таблица 1
Масса животных в разном возрасте
| Возраст | Масса, г | ||
| Морские свинки | Кролики | Мыши | |
| Дней | 1,5 | ||
| 37-55,7* | 3,0 | ||
| - | 4,5 | ||
| - | |||
| - | |||
| - | |||
| 221-240-250 | - | ||
| Месяцев | |||
| 350-400 | 167-307 | 10-11 | |
| - | 419-526 | 16-18 | |
| 450-500 | 612-897 | 18-19 | |
| 650-700 | 909-1069 | 20-22 | |
| 700-750 | 1221-1237 | - | |
| - | 1931-2017 | - |
* Масса кроликов зависит от величины помета: первые цифры при помете из 8 кроликов, вторые – при помете из 3 кроликов.
Выписывая из питомника беременных животных, особенно мышей, следует учитывать, что самки первое потомство нередко уничтожают. Поэтому лучше брать животных, беременных 2–3-й раз. Беременных белых мышей и крыс следует брать в виварий не позже чем за 2–3 дня до родов, а кроликов и морских свинок – за 15 – 20 дней. Перемещение животных в более поздние сроки беременности приводит к аборту.
Для предупреждения каннибализма и аборта беременных мышей размешают по 2 – 3 в банку, а белых и хлопковых крыс, морских свинок и кроликов – по одной. Клетки для морских свинок должны быть размером 0,3 х 0,5 м. а для кроликов – 0,75 х 1,0 м. Маток, проявляющих каннибализм, надо немедленно удалять из гнезда. На каждую матку (белую мышь, белую крысу) должно приходиться не более 10–12 новорожденных Большая нагрузка способствует каннибализму. При проведении с молодыми животными длительных опытов (особенно зимой) в пищу мышей необходимо добавлять витаминизированный рыбий жир, а в рацион хлопковых и белых крыс – молоко и мясо.
Таблица 2
Температура тела, пульс и число дыханий у здоровых животных
| Вид животных | Температура, °С | Пульс в 1 мин | Дыхание в 1 мин |
| Морская свинка | 37,9-39,4 | ||
| Кролик | 38,5-39,7 | ||
| Крыса белая | 37,5-39,3 | - | |
| Мышь белая | 37,0-39,0 | - | |
| Собака | 37,5-39,0 | ||
| Кошка | 38,0-39,5 | ||
| Курица | 40,0-42,0 | -14 | |
| Голубь | 41,0-43,0 | 140-200 | 16-28 |
| Овца | 38,0-41,0 | 12-20 | |
| Свинья | 38,0-40,0 | 10-20 | |
| Корова | 37,5-39,5 | 40-80 | 10-30 |
| Лошадь | 37,5-38,5 | 24-44 | 8-16 |
Таблица 3
Состав крови некоторых лабораторных животных (по В.Н.Никитину)
| Вид животных | Гемоглобин г% | Число эритроцитов, млн /мл | Число лейкоцитов | Лейкоцитарная формула | |||||||
| Базофилы | Эози- нофи- лы | Мие- лоци- ты | Юные | Пало- чко- ядер- ные | Сег-мен-то-ядер-ные | Лимфоциты | Моноциты | ||||
| Собака | 6,5 | 1,0 | - | - | 3,0 | 58,0 | 25,0 | 7,0 | |||
| Овца | 9,4 | 8,2 | 0,6 | 4,5 | - | - | 1,2 | 33,0 | 57,7 | 3,0 | |
| Кошка | 7,0 | - | 4,0 | - | - | 6,0 | 52,0 | 37,7 | 2,1 | ||
| Кролик | 5,0 | 5,0 | 1,0 | - | - | - | 30,0 | 60,0 | 4,0 | ||
| Морская свинка | 5,0 | 12,0 | 0,1 | 6,0 | - | - | 0,5 | 35,0 | 53,4 | 5,0 | |
| Крыса белая | 11О | 6,0 | 15,0 | - | 2,0 | - | - | - | 30,0 | 67,0 | 1,0 |
| Мышь белая | 9,0 | 13,0 | 0,5 | - | - | - | 2,0 | 36,0 | 60,0 | 0,5 | |
| Курица | 3,5 | 36,0 | 3,0 | 4,0 | - | - | 0,25 | 36,0 | 50,0 | 6,75 | |
| Голубь | 4,0 | 10,4-31,4 | 2,0 | 1,5 | - | - | - | - | 55,5 | 34,9 | |
| Лягушка | 0.38 | 2,4-39,1 | 23,0 | 6,0 | - | - | 44,5 | 38,3-39,1 |
Проявлению каннибализма в значительной мере способствуют посторонние запахи, приобретаемые новорожденными в ходе манипулирования с ними экспериментатора Новорожденных животных следует брать только прокипяченным пинцетом Экспериментатор должен работать в перчатках, с которых смыты следы антисептика (йода, фенола и др.) Заражать новорожденных животных лучше на весу или на толстом слое стерильной фильтровальной бумаги.
В группу для проведения опыта подбирают животных с одинаковыми показателями массы, температуры, состава крови и т. д. (табл. 1-3). От этого в значительной степени зависит успех выделения, титрования и пассирования вируса. При этом учитывают восприимчивость животных к различным вирусам Отобранных животных метят, распределяют по банкам или клеткам, отмечают дату постановки опыта, его номер, заражающую или профилактическую дозу препарата и, если необходимо, как мечены животные Последнее важно, когда в одной банке или клетке находятся животные нескольких групп.
4.5 Техника безопасности при работе с лабораторными животными. Прежде всего, сотрудники должны быть защищены от естественных инфекционных болезней животных и от воспроизводимых на них экспериментальных инфекций, возбудители которых патогенны для человека.
Наиболее часто встречается среди лабораторных животных такая естественная инфекция, как сальмонеллез. Заразившиеся люди переносят заболевание в гастроинтестинальной или тифоподобной (генерализованной) форме. Опасность для людей представляют также листериоз, псевдотуберкулез, туберкулез, туляремия.
Поскольку многие инфекционные болезни животных протекают в бессимптомной персистирующей форме, животных необходимо периодически обследовать.
Источником инфицирования людей могут служить экспериментально зараженные животные и их эктопаразиты. Профилактика заражения людей от животных проводится с учетом возможного пути передачи данного возбудителя. Состояние здоровья сотрудников лаборатории находится под медицинским контролем с учетом особенностей инфекции, с возбудителем которой работают сотрудники.
При работе в лаборатории с вирусами бешенства, клещевого энцефалита, инфекционного гепатита и некоторыми другими инфекциями сотрудникам делают прививки против этих болезней. В случае необходимости проводят экстренную профилактику специфическим иммуноглобулином или сывороткой реконвалесцентов. Одновременно осуществляют весь комплекс противоэпидемических мероприятий, необходимый при данной инфекционной болезни.
4.6 Метка лабораторных животных. Метка является непременным условием использования животных в эксперименте. На клетке, в которой помещены зараженные животные, укрепляют бирку с надписью, отражающей использованный для заражения вирус (или номер экспертизы исследуемого патологического материала), количество зараженных животных, дату заражения и, если надо, другие сведения.
Для животных разных видов применяют разные способы индивидуальной метки. Для крупных животных и кур используют металлические бирки со штампованным номером. Бирки надевают на корень уха (кроликам), вставляют в ушную раковину по типу серьги (морским свинкам), надевают на ногу – окольцовывают (курам).
При использовании в эксперименте небольшой группы животных и при непродолжительном сроке его можно выстригать шерсть знаками на спине, бедрах (у кроликов). Морских свинок можно различать по окраске, которую регистрируют в рабочем журнале.
Метка белых мышей, белых крыс может быть проведена ампутацией отдельных пальцев на передних или задних конечностях, каждый из которых соответствует тому или другому порядковому номеру: на передних лапах – единицам, на задних – десяткам. Однако чаще пользуются методом нанесения цветных пятен на непигментированную шерсть. Насыщенный раствор пикриновой кислоты лучше других красителей (растворов фуксина, бриллиантовой зелени) удерживается на шерсти и коже животных. Цветные метки ставятся в местах, соответствующих определенному порядковому номеру животного. Так, если тело животного мысленно разделить на три продольные части (левый бок, спина, правый бок), то нанесение цветных пятен начинают с левого верхнего угла, т. е. лопатки, и это будет соответствовать 1 (рис. 8). Тогда, двигаясь назад, левый бок соответствует 2, а левое бедро – 3, далее затылок – 4, спина – 5, область репицы – 6, правое плечо – 7, правый бок – 8, правое бедро – 9. Используя два цвета красителей, можно дать обозначения одним из них – единиц, другим – десятков.
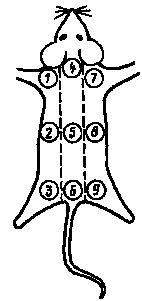
Рисунок 8. Метка лабораторных животных
 2014-02-05
2014-02-05 5543
5543
