Железоуглеродистые сплавы - сложные системы, состоящие из 5-6 и более компонентов. Один из них попадает в сплавы в процессе металлургического передела (кремний, сера, фосфор, кислород, водород и др.) - примеси, другие специально вводятся в сплавы для изменения их свойств в нужном направлении (хром, никель, молибден, вольфрам и др.) - легирующие элементы.
Основными элементами, определяющими структуру и свойства, являются железо и углерод. Поэтому эти сложные сплавы рассматриваются как двойные - железо-углерод, а влияние примесей и легирующих элементов рассматривается самостоятельно в соответствующих разделах. На практике применяются сплавы, содержащие < 6% С.
Соединение Fe3С (цементит) неустойчиво (метастабильно) и при соответствующих условиях (медленном охлаждении) возможна кристаллизация из жидкости свободного углерода в виде графита. Железоуглеродистые сплавы, содержащие < 6,67% С могут кристаллизоваться по двум типам диаграмм: метастабильной - Fe - Fe3C, когда свободного углерода не образуется, и стабильной, Fe - С, когда возможно выделение свободного углерода из жидкости или в результате распада цементита. Эти диаграммы изображают на одном графике, линии метастабильной диаграммы сплошные, стабильной пунктирные.
Железо - переходный металл серебристо-белого цвета. Атомный номер 26, атомная масса 55,85, атомный радиус 1,27 А, электронная формула 1S2 2S2 2Р6 3S2 ЗР6 3D6 4S2. Чистое железо содержит 0.001% примесей, техническое железо (армко) - 0,1 % примесей. Температура плавления - 1539 С, кипения - 3200 С.
В твердом состоянии в зависимости от температуры Fe иметь две полиморфные модификации альфа и гамма: Fe – α существует при температурах ниже 910о С и выше 1392 Со. В интервале 1392-1539 Со Fe - α часто обозначают как Fe – γ.
Кристаллическая решетка Fe - α объемноцентрированный куб с периодом решетки 2,8606 А.
До 768о С (точка Кюри) она ферромагнитна, при более высоких температурах - паромагнитна.
Кристаллическая решетка Fe- γ - гранецентрированный куб с периодом решетки 3,645 А. Плотность более высокая - 8,0 - 8,1 г/смЗ. Это значит, что при полиморфном превращении альфа --> гамма происходит сжатие, объемный эффект - 1%.
Полиморфное превращение связано с различием в изменении величины свободной энергии решетки ОЦК И ГЦК с температурой.
Температуры превращения в твердом состоянии называются критическими точками и обозначается буквой А с соответствующими индексами. Ас и Аг не совпадают вследствие теплового гистерезиса (все превращения происходят при некотором нагреве или переохлаждении).
Свойства технического железа при 200 С: НВ 80; 220-250 МПа.
Углерод. В природе встречается в двух аллотропических формах - алмаз и графит, атомный номер 6, плотность 2,5 г/смЗ, атомная масса 12,, атомный радиус 0,77 А, температура плавления 35000 С. Углерод полиморфен. При атмосферном давлении устойчивая модификация графит. Решетка графита гексагональная, структура слоистая. Слабые связи между параллельными слоями атомов и очень прочные (ковалентные) - между атомами внутри слоя.
Углерод растворим в железе в жидком и твердом состояниях, а также может быть в виде химического соединения карбида железа- цементита, а в высокоуглеродистых сплавах в виде графита.
В системе железо-углерод различают следующие фазы: жидкий сплав, твердые растворы внедрения - феррит и аустенит, химические соединения - цементит и графит.
Феррит(Ф) - твердый раствор внедрения углерода (и других примесей) в железе, решетка, ОЦК. Различают альфа-феррит с максимальной растворимостью углерода 0,025% (при 7270С) и минимальной растворимостью 0,006% (при 200 С), и высокотемпературный - феррит с предельной растворимостью углерода 0,1% (при 14990С).
Атомы углерода располагаются в решетке феррита в центре грани куба, где имеется максимальная пора. Механические свойства альфа -феррита близки к свойствам армко-железа,. До 7680 С ферромагнитен.
Аустенит (А) - твердый раствор внедрения углерода (и других примесей) в гамма-железе решетка ГЦК. Предельная растворимость - 2,14 (при 1147° С). Атомы углерода в решетке гамма - железа располагаются в центре элементарной ячейки, где может поместиться сфера радиусом 0,41 атомного радиуса железа,т.е. близкая к атомному радиусу углерода и в дефектных областях кристалла. Аустенит обладает высокой пластичностью и сравнительно низкой прочностью.
Цементит (Ц) - карбид железа, имеет сложную орторомбическую решетку. Температура плавления из-за его метастабильности при высоких температурах точно не установлена (1250-15500С). До 2210С (А) ферромагнитен.
Цементит имеет очень высокую твердость (> НВ 800) и практически нулевую пластичность. Он может образовывать твердые растворы замещения и внедрения с другими элементами. При замещении атомов железа атомами других металлов образуется легированный цементит (Fe, W, Сг). Графит - о его строениях свойствах рассказано выше.
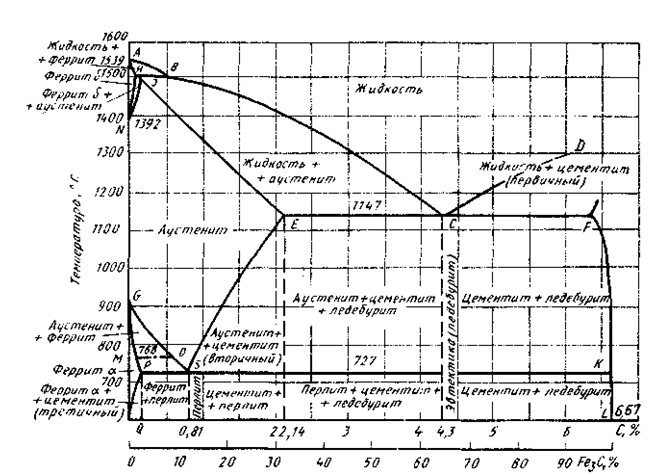 |
Диаграмма Fe-Fe3C
Рис. 6.1. Диаграмма Fe-Fe3C
Ось абсцисс двойная: показано содержание углерода и цементита. Уменьшение содержания углерода на 15% дает содержание цементита в любом сплаве в % по массе. Все сплавы в данной системе можно разбить на две группы: сплавы, содержащие до 2,14% называются сталями, сплавы, содержащие > 2,14% С - чугунами.
Точки А и Д соответствуют температурам плавления железа и цементита. Точки N (13920С) и (9100С) соответствуют полиморфному превращению, в чистом железе.
Линия АВСД - линия ликвидус. Участок АВ показывает температуру начала кристаллизации из жидкого сплава - феррита, ВС - температуру кристаллизации аустенита, СД - температуру кристаллизации первичного цементита (П1).
Линия AHJBECF -линия солидус. Ниже участка АН сплав затвердел и существует только феррит; HJB - линия перетектического превращения (равновесия).
Линия ECF (солидус) - линия эвтектического превращения (равновесия) соответствует кристаллизации из жидкости эвтектики, состоящей из кристаллов А и Ц - ледебурита (Л)
В ледебурите всегда 4,3% углерода, и он образуется при постоянной температуре (11470С). Превращение происходит во всех сплавах, содержащих 2,14 и < 6,67% С (чугунов).
Линии NH и NJ линии первого (высокотемпературного) полиморфного превращения в сплавах. В отличие от чистого железа полиморфные превращения в сплавах происходят в интервале температур.
Линия ES - линия ограниченной растворимости углерода в аустените. Ниже этой линии А пересыщен углеродом и из него выделяется высокоуглеродистая фаза - Ц (цифра II указывает, что Ц выделился из А).
Линия PSK - линия эвтектоидного превращения (равновесия). Это превращение протекает у всех сплавов, при этом аустенит состава S распадается на смесь двух фаз: феррита состава Р и цементита
Аs→ (Фр+Ц)-П
Распад происходит при постоянной температуре (7270С) и в образующемся эвтектоиде - перлите (П), всегда содержится 0,8% углерода.
Линии GS и GP - линии второго полиморфного превращения. Ниже линии GP полиморфное превращение заканчивается и структура сплава ферритная (А Ф).
Линия PQ - линия ограниченной растворимости углерода в феррите. Ниже этой линии феррит пересыщен углеродом и из него выделяется И (цифра III указывает, что Ц выделился из феррита).
На всех горизонтальных линиях в равновесии находятся три фазы, система нонвариатна, т.е. С=0.
Перитектическое превращение наблюдается у сплавов, содержащих от 0,1 до 0,5% С, эвтектическое - от 2,14 до 6,67 С и эвтектоидное - у всех сплавов, содержащих > 0,025 С.
Сплавы, содержащие < 0,8 называются доэвтектоидными, > 0,8%С - заэвтектоидными и 0,8%С эвтектоидными сталями. В зависимости от концентрации углерода сплавы, содержащие < 0,3%С называются низкоуглеродистыми, с 0,3 - 0,6%С - среднеуглеродистым, с > 0,7%С - высокоуглеродистыми сталями.
Кристаллизация стали. Все превращения начинаются в жидкости при некотором переохлаждении, т.е. при температурах ниже равновесной, лежащей на соответствующей линии диаграммы.
Перекристаллизация стали (превращения в твердом состоянии). Основа этих превращений - полиморфное превращение ГЦК - ОЦК и изменение растворимости углерода в аустените и феррите при изменении температуры.
 2014-02-02
2014-02-02 2176
2176








