Литература
Основная:
1. Пащенко А.Л. Физ. химия силикатов. – М.: «Высшая школа», 1986. – 368 с.
Дополнительная:
2. Горшков В.С. и др. Физическая химия силикатов и других тугоплавких соединений. – М.: «Высшая школа», 1988. – 400 с.
«Основы аналитической химии»
Краткое содержание лекции
Аналитическая химия имеет два раздела: качественный и количественный анализы. Химический анализ широко применяется в различных отраслях: металлургии, в биологии, медицине, геохимии, в производстве строительных материалов и др.
Задачей качественного анализа является выяснение качественного состава вещества, т.е. из каких элементов или ионов состоит данное вещество. При изучении состава неорганических веществ в большинстве случаев приходится иметь дело с водными растворами кислот, солей и основании. Эти вещества служат электролитами и в водных растворах диссоциированы на ионы. Поэтому анализ сводится к определению отдельных ионов -катионов и анионов.
Методы качественного анализа делятся на химические, физико-химические и физические. Мы рассматриваем химические методы анализа отдельных групп катионов и анионов в растворах. Анализ вещества, проводимый в растворах, называется мокрым путем. Это основной путь полного определения состава вещества. При этом применяют реакции образования осадка, окрашенных соединений или выделения газа. Эти реакции проводят обычно в пробирках. Ряд качественных реакций проводят на предметных стеклах, и образующиеся кристаллы рассматривают под микроскопом. Это - так называемые микрокристаллоскопические реакции. Иногда прибегают к выполнению реакций капельным методом. Для этого на полоску фильтровальной бумаги наносят каплю испытуемого раствора и каплю реактива и рассматривают окраску пятна на бумаге.
В химическом анализе используется лишь незначительная часть того многообразия реакций, которое свойственно данному иону. Происходящее при этом химическое превращение называется аналитической реакцией. Вещества, с помощью которых выполняется открытие ионов, называются реактивами на соответствующие ионы. Реакции, характерные для какого-либо иона, называются частными реакциями этого иона. Например, желтая кровяная соль K4[Fe (CN)6] является реактивом на ион Fe3+, a реакция 4Fe3+ + [ Fe (CN)6]4- = Fе4 [Fe (CN)6]3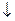 - частной реакцией этого иона.
- частной реакцией этого иона.
Аналитическая реакция должна протекать не слишком медленно и быть достаточно простой по выполнению. Для аналитических реакций важнейшими требованиями служит специфичность и чувствительность. Чем меньшее количество ионов вступает в ре-акцию с данным реактивом, тем более специфична данная реакция. Чем меньшее количество вещества может быть определено с помощью данного реактива, тем более чувствительна эта реакция. Так, реакция открытия ионов Ғе3+ с реактивом K4 [Fe (CN)6] является специфичной, т.к. благодаря образованию характерного темно-зеленого осадка Fe4[Fe (CN)6]3 позволяет открывать ион Fe3+ в присутствии многих других катионов. Реакция очень чувствительна, ибо позволяет открывать незначительные количества солей Fe (III).
Условия проведения аналитических реакций
Выполнение каждой аналитической реакции требует соблюдения
определенных условий се проведения, важнейшими из которых являются:
1) концентрация реагирующих веществ, 2) среда раствора, 3) температура.
Концентрация открываемого иона и реактива имеет большое значение.
Каждая частная реакция характеризуется открываемым минимумом
вещества в данном количестве раствора. Чем чувствительнее реакция, тем
меньше открываемый минимум вещества. Если реакция
малочувствительна, проводить ее можно только в достаточно концентрированных растворах. Для очень многих частных реакций имеет значение концентрация реактива и его количество. Обычно при выполнении качественной реакции добавляют избыток раствора. Однако слишком большого количества реактива надо избегать, т.к. в некоторых случаях может пойти вторичная реакция, и осадок растворится. Так, при добавлении к находящемуся в растворе иону А13+ иона ОН- (реактив NaOH) образуется студнеобразный белый осадок А1(0Н)3
А13++ЗОН-=А1(ОН)3 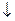
При дальнейшем прибавлении гидроксида натрия осадок А1(ОН)з растворяется вследствие образования гидроксикомплексов, например [А1 (ОН4]-
А1(ОН)3+ОН-=[А1(ОН4)]-.
Реакция среды (кислая, нейтральная, щелочная) - важный фактор проведения аналитических реакций. Это зависит от свойств как анализируемых ионов, так и используемых для анализа веществ с различным значением водородного показателя (рН) раствора.
Третьим фактором является температура. Некоторые трудно растворимые соли выпадают в осадок только при охлаждении. Примером может служить образование осадков Na[Sb(OH)6] и KHC4H4О6
Многие реакции происходят без нагревания, на холоду. Часть реакций приходится проводить при нагревании, т.к. при обычной температуре они протекают слишком медленно. Необходимость соблюдения определенных условий справедлива и для реакций, проводимых сухим путем. Так, окрашивание пламени в характерный для данного иона цвет удается лишь при нагревании в определенной части пламени достаточно летучего соединения.
Реактивы, используемые для выполнения аналитических реакций, делятся на специфические, избирательные (селективные) и групповые. Специфические-образуют характерный осадок или окрашивание только с определенным ионом. Например, реактив K3[Fe (CN)6] образует темно-синий осадок только с ионами Fe2+.
Избирательные (селективные) реактивы реагируют с несколькими ионами, которые могут принадлежать к одной или разным группам.
Например, реактив КJ реагирует с ионами Pb2+, Ag 2+ Hg2+ (II группа), а также с ионами Hg2+ и Сu 2+ (IV группа).
Групповой реактив вступает в реакцию со всеми ионами данной группы. С помощью этого реактива ионы данной группы можно отделить от ионов других групп. Например, групповым реактивом катионов III-й аналитической группы является серная кислота, которая с катионами Ва2+ и Са2+ образует белые трудно растворимые осадки.
Сабақтың қысқаша мазмұны
Аналитикалық химияның мәселелері қарастырылады. Аналитикалық химия екі бөлімнен тұрады: сапалық және сандық. Химиялық анализ әртүрлі салаларда кеңінен қолданылады: құрылыс материалдары өндірісінде, металлургия, биология, медицина, геохимия және т.б.
 2014-02-02
2014-02-02 850
850








