В состав всех органических кислот входит группа
О
II
—С—ОН, или —СООН, которая носит название карб-
оксильной; она содержит подвижный водород. При действии на кислоту металлом из каждой молекулы кислоты вытесняется только тот атом водорода, который входит в состав карбоксильной группы. По числу карбоксильных групп кислоты разделяют на одноосновные, двухосновные и т. д. Например, уксусная кислота (СН3—СООН) является одноосновной кислотой, а щавелевая кислота (НООС—СООН) двухосновной.
Уксусная кислота. Физические и химические
свойства. Уже в глубокой древности был известен уксус, который образовывался при скисании спиртных напитков. Спиртные напитки (ви-
но, пиво и т. д.), хорошо сохраняющиеся в закрытых сосудах, быстро превращаются в уксус при хранении в открытой посуде.
Безводная (или 90%-ная) уксусная кислота при температуре выше 165 °С — бесцветная жидкость, ниже этой температуры представляет собой кристаллическую массу, похожую ни лед, поэтому ее иногда называют ледяной кислотой. Она хорошо растворяется в воде, спирте,
эфире и многих других веществах; 70—80%-ный водный
раствор кислоты называется, уксусной эссенцией.
Уксусная кислота хорошо растворяет серу, фосфор и другие неорганические вещества. При действии на нее некоторых металлов образуется соль и выделяется водород.
Так как уксусная кислота принадлежит к числу сравнительно слабых кислот, водород выделяется медленнее, чем при взаимодействии металлов с соляной или серной кислотой. При взаимодействии уксусной кислоты с основаниями и основными оксидами также образуются соли.
Уксусная кислота самовозгорается при контакте с хромовым ангидридом, перекисью натрия и другими сильными окислителями.
Получение и применение. В настоящее время значительные количества уксусной кислоты получают окислением уксусного альдегида (ацетальдегида) в присутствии катализатора
О О
II 1!
СН3—С—Н +О 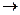 СН3—С—ОН
СН3—С—ОН
Уксусная кислота образуется также при сухой перегонке дерева. Она переходит в подсмольную воду вместе с метиловым спиртом и ацетоном. Подсмоленную воду обрабатывают гашеной известью, образовавшийся
ацетат кальция кипятят с разбавленной серной кислотой
и отгоняют уксусную кислоту.
Применение уксусной кислоты весьма многообразно.
Ее широко используют в пищевой и текстильной промышленности, в производствах искусственного волокна, пластических масс, красителей (например, индиго), лекарственных веществ (например, аспирина), душистых веществ, растворителей для лаков. В последнее время уксусную кислоту стали применять в производстве трудновоспламеняющейся кинопленки.
Непредельные карбоновые кислоты. Среди непредельных одноосновных кислот известны кислоты с одной, двумя и тремя двойными связями. Непредельные кислоты являются более сильными, чем предельные, в чем и сказывается влияние двойной связи.
Олеиновая, линолевая и линоленовая кислоты в виде эфиров глицерина распространены в природе (жиры и масла).
Физические и химические свойства. Непредельные одноосновные карбоновые кислоты — маслянистые жидкости, нерастворимые в воде и легче се. Они, как и все карбоновые кислоты, способны взаимодействовать с солями, щелочами и оксидами металлов.
Непредельные карбоновые кислоты на воздухе при определенных условиях способны к самовозгоранию.
Получение и применение. Практическое применение нашли олеиновая и акриловая кислоты. Олеиновую кислоту получают из жиров как побочный продукт па стеариновых заводах, а также из оливкового, подсолнечного
и других масел. Щелочные соли олеиновой кислоты (мыла) применяют для промывания шерсти, свинцовые соли — в медицине для приготовления свинцового пластыря. Олеат алюминия используют для изготовления на-
палма. Высокомолекулярные соединения, полученные полимеризацией акриловой кислоты (полиакрилаты) и ее эфиров, нашли широкое применение в производстве органического стекла (плексигласа).
 2014-02-02
2014-02-02 2529
2529
