Удельная электропроводность (χ) – это электропроводность 1 см3 раствора, находящегося между электродами с площадью S = 1 см2 и расстоянием между ними l = 1 см.
Единица измерения χ – См/см.
χ – аддитивная величина, она определяется наличием всех ионов в растворе:
χ = α × С ×(z +λ+ + z –λ–),
где α – степень диссоциации;
С – концентрация, моль экв/см3;
z + и z – – заряды ионов;
λ+ и λ– – подвижности ионов.
Таким образом, аналитический сигнал не избирателен, поэтому по величине АС нельзя:
§ получить информацию о качественном составе раствора;
§ определить содержание вещества в смеси.
Величину χ измеряют непосредственно (кондуктометр) или рассчитывают по результатам измерения сопротивления R (мост переменного тока):
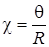 ,
,
| где | θ – константа ячейки. |
Факторы, влияющие на АС:
1. Природа электролита:
· степень диссоциации (α): чем больше α, тем больше χ;
· подвижности ионов электролита (λ+ и λ–): чем больше λ±, тем больше χ;
· диэлектрическая проницаемость(ε):чем больше ε, тем больше χ (т. к. увеличивается α);
· вязкость (η):чем больше η, тем меньше χ (т. к. уменьшаются подвижности ионов λ±);
3. Температура (t о): чем больше t о, тем больше χ (т. к. увеличиваются скорость теплового движения и степень диссоциации α, а также уменьшается η).
Следовательно, измерения надо проводить при постоянной температуре.
4. Концентрация электролита (С):
· в разбавленных растворах зависимость χ = f(С) – линейная;
в концентрированных – наблюдаются отклонения от линейности (рис. 12).
Причины отклонений от линейности в области больших концентраций:
· уменьшение скорости движения ионов из-за усиления межионных взаимодействий;
· для сильных электролитов – усиление тормозящих эффектов (электрофоретического и релаксационного);
· для слабых электролитов – уменьшение α;
· увеличение η;
· ассоциация ионов в ионные пары, которые не проводят ток.
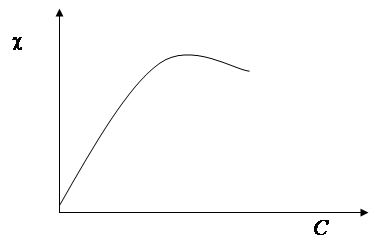
Рис. 12. Зависимость удельной электропроводности от концентрации
Следовательно, измерения надо проводить в разбавленных растворах.
 2014-02-13
2014-02-13 2529
2529








