Вопрос № 2. Механизм химического взаимодействия при горении.
После возникновения горения источником дальнейшего зажигания новых порций горючей смеси обычно является сама зона горения, в которой происходит интенсивное выделение тепла. Это тепло и является причиной непрерывного поддержания процесса горения.
Для возникновения и протекания процесса горения горючее вещество и окислитель должны находиться в определённом количественном соотношении.
Другим необходимым условием того, чтобы между молекулами горючего вещества и окислителя произошло химическое взаимодействие, является их столкновение друг с другом (соударение). То есть молекулы должны сблизиться на столько, чтобы атомы одной из них испытывали бы действие электрических полей, создаваемых атомами другой молекулы. Только при этом возможны переходы электронов и перегруппировки атомов, в результате которых образуются молекулы продуктов горения.
Однако не всякое столкновение молекул реагирующих веществ приводит к образованию продуктов реакции. Для того чтобы произошла реакция необходимо сначала разорвать или ослабить связи между атомами в молекулах горючего вещества и окислителя. На это необходимо затратить определённую энергию. Поэтому молекулы горючего вещества и окислителя должны находиться в активном состоянии, т.е. обладать избыточной энергией - энергией активации.
Энергия активации – минимальная энергия реагентов, достаточная для того, чтобы они вступили в химическую реакцию, то есть преодолели барьер на поверхности потенциальной энергии, через который должна пройти система в ходе элементарного акта химического превращения.
Изменение энергии в ходе экзотермической реакции можно представить следующей схемой.
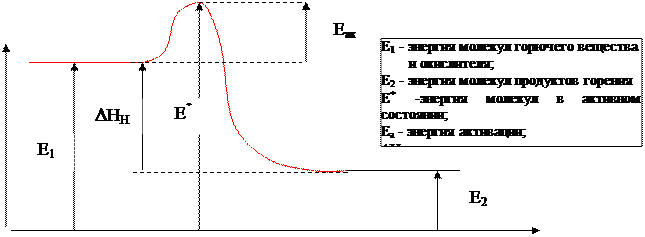 |
Высота потенциального барьера для химической реакции, идущей через переходное состояние, равна потенциальной энергии переходного состояния. Если реакция сложная, проходящая в несколько этапов, то энергия активации равна наибольшей энергии активации.
Чем ниже энергетический уровень молекул горючего вещества и окислителя в активном состоянии, тем меньше необходимо затрачивать энергии для перевода молекул в это состояние. Следовательно, молекулы быстрее взаимодействуют между собой, увеличивая при этом скорость горения.
 2014-02-09
2014-02-09 2228
2228
