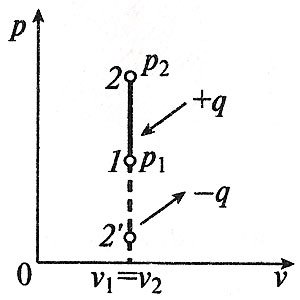
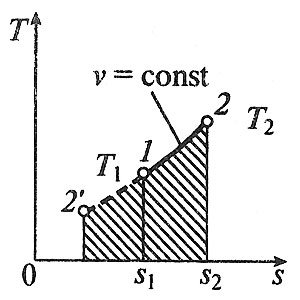

Изохорный процесс в p, v-, T, s- и i, s-координатах (диаграммах)
При изохорном процессе выполняется условие v = const.
Из уравнения состояния идеального газа (pv = RT) следует:
p/T = R/v = const,
т. е. давление газа прямо пропорционально его абсолютной температуре:
p2/p1 = T2/T1.
Работа расширения в изохорном процессе равна нулю (l = 0), так как объем рабочего тела не меняется (Δ v = const).
Количество теплоты, подведенной к рабочему телу в процессе 1-2 при cv = const определяется по формуле:
q = cv(T2 — T1).
Т. к. l = 0, то на основании первого закона термодинамики Δ u = q, а значит изменение внутренней энергии можно определить по формуле:
Δ u = cv(T2 — T1).
Изменение энтропии в изохорном процессе определяется по формуле:
s2 – s1 = Δ s = cv ln(p2/p1) = cv ln(T2/T1).
 2015-01-30
2015-01-30 1100
1100