 |
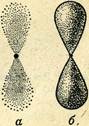
На втором энергетическом уровне атомов, наряду с s-АО, появляются другие атомные орбитали, геометрическая форма которых показана на рис. 5.
Рис. 5.
Объем пространства с 90%-ой вероятностью пребывания в орбитали этого вида состоит из двух половин, расположенных симметрично относительно выбранной оси вращения. Ось расположена в вертикальной плоскости, отделяющей половины объема друг от друга и называемой узловой плоскостью (на рис. 5 ось изображена в виде точки).
Атомную орбиталь, имеющую вращательную (осевую) симметрию принято обозначать как р- орбиталь, а находящиеся в ней электроны это р- электроны.
Каждая атомная р- орбиталь может принять (при максимальном заполнении) два электрона, подобно любой другой АО. Эти электроны сообща занимают обе половины р- орбитали (представление о том, что каждая половина р-АО содержит 1е, является ложным). На каждом атомном энергетическом уровне (кроме первого) имеется три атомных орбитали, которым отвечает максимальное заселение шестью электронами.
Все три р-АО одного энергетического уровня отличаются друг от друга пространственным расположением; их собственные оси, проходящие через обе половины орбитали и перпендикулярные ее узловой плоскости, образуют систему декартовых координат (обозначения собственных осей х, у, z). По этому на каждом энергетическом уровне имеется набор трех атомных р- орбиталей: рх-, ру- и рz-АО. Буквы х, у и z соответствуют магнитному квантовому числу, позволяющему судить о влиянии внешнего магнитного поля на электронную оболочку атома.
В геометрическом представлении три атомные р-орбитали одного энергетического уровня (одного электронного слоя) пронизывают друг друга. В первом приближении граничную поверхность р-АО изображают в виде двух симметрично расположенных лепестков (гантелеобразная форма, рис. 5). С учетом такого приближения взаимное расположение трех р-АО одного энергетического уровня атома показано на рис. 6.
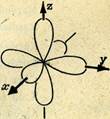 |
Рис. 6.
В атомной модели Бора – Зоммерфельда р-электроны совершают движение по эллиптическим орбитам; оси трех атомных р-орбит в этой модели соответствуют большим осям эллипсов.
В ряду элементов, составленном по возрастанию порядкового номера, р-электрон впервые появляется у элемента бора. Заполнение трех р-АО второго энергетического уровня у атомов элементов от бора до неона протекает в соответствии с записью: Бор – 1s22s22p1, углерод– 1s22s22p2, азот – 1s22s22p3, …, неон – 1s22s22p6.
Заполнение 3s- и 3р- АО протекает идентично заселению второго энергетического уровня (рис. 7). '
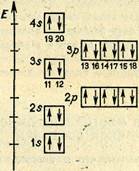 |
рис. 7.
 2015-01-07
2015-01-07 3483
3483
