На границе раздела твердой фазы и раствора, как правило, возникает двойной электрический слой (ДЭС). Его происхождение может быть двояким. Во-первых, возможна ионизация молекул, составляющих поверхностный слой твердой фазы, например, ионизация молекул H2SiO3, образующихся на поверхности SiO2 в воде. Во-вторых, на поверхности твердой фазы может происходить адсорбция одного из ионов, присутствующего в растворе электролита. При этом на поверхности преимущественно адсорбируются ионы, входящие в состав твердой фазы или близкие к ним по природе. Так на поверхности частиц золя AgCl будут адсорбироваться ионы Ag+ или Cl– в зависимости от того, какие из них имеются в растворе в избытке. Ионы, определяющие заряд коллоидной частицы (гранулы) называются потенциалобразующими. К заряженной поверхности частиц будут притягиваться ионы противоположного знака, т.е. противоионы, образуя двойной электрический слой.
Двойной электрический слой на поверхности коллоидных частиц включает так называемый адсорбционный слой и диффузный слой. Адсорбционный слой образован частью противоионов, которые прочно связаны с ядром мицеллы электростатическими силами (притягивание разноименных зарядов) и адсорбционными силами. Остальные противоионы, благодаря тепловому движению и взаимному отталкиванию, уходят на некоторое расстояние от межфазной границы, образуя диффузный слой ионов, который удерживается у поверхности только электростатическими силами (см. рис.).
Каждая точка электрического поля двойного слоя, образованного потенциалопределяющими ионами и противоионами, характеризуется определенным значением электрического потенциала. Причем в адсорбционном слое, т.е. на малых расстояниях от поверхности, падение потенциала происходит круто, а далее в диффузном слое более полого.
Потенциал двойного слоя, отвечающий границе скольжения при движении дисперсной фазы и дисперсионной среды относительно друг друга, называется электрокинетическим или x-потенциалом (дзета-потенциалом). Место границы скольжения определяется действием адсорбционных и электрических сил, а также свойствами раствора, окружающего частицы, в частности, вязкостью прилегающих слоев жидкости. Граница скольжения может совпадать с границей между адсорбционными и диффузным слоями или находиться несколько дальше от поверхности, где-то в диффузном слое.
Строение мицеллы и двойного электрического слоя. 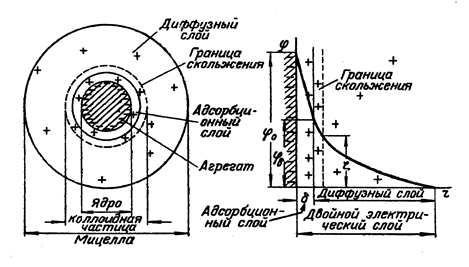 |



Электрофорез находит широкое применение в медико-биологических исследованиях. В клинической практике электрофоретические методы применяются для диагностики многих заболеваний, для разделения аминокислот, нуклеиновых кислот, антибиотиков, ферментов, антител, для определения чистоты белковых препаратов и т.д.







Дзета-потенциал является важной характеристикой коллоидных систем. Во многих случаях отмечается закономерность: чем больше величина x-потенциала, тем выше устойчивость золя. При значениях x-потенциала ниже 0,03 В (критический потенциал) наступает коагуляция золя.

При добавлении раствора электролита к золю противоионы нейтрализуют заряд на поверхности коллоидной частицы (происходит сжатие ДЭС), что позволяет частицам золя легче приближаться друг к другу, и это воздействие тем сильнее, чем больший заряд несет противоион.
Коагулирующий ион несет заряд, противоположный заряду коллоидной частицы, при этом порог коагуляции тем меньше, чем больше заряд (валентность) коагулирующего иона – правило Шульце-Гарди. Порогом коагуляции называется минимальная концентрация электролита, вызывающая коагуляцию.
Порог коагуляции выражается в миллимолях электролита на литр коллоидного раствора (ммоль/л). Порог коагуляции вычисляют по формуле: 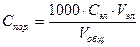 ,
,
где Сэл – концентрация раствора добавленного электролита, моль/л, Vэл – наименьшее число миллилитров раствора электролита, достаточное для коагуляции золя, Vобщ – суммарный объем золя после добавления электролита, мл.
При добавлении некоторых веществ нередко наблюдается повышение устойчивости лиофобных золей к коагулирующему действию электролитов. Такое стабилизирующее действие на дисперсные системы называется коллоидной защитой. Защитными свойствами обладают белковые вещества (желатин, альбумины, казеин), полисахариды (крахмал, декстрин), некоторые поверхностно-активные вещества. Если, например, к золю гидроксида железа (III) добавить некоторое количество желатина, то для коагуляции такого золя требуется значительно больше электролита, чем для коагуляции незащищенного золя. Коллоидную защиту объясняют адсорбцией стабилиаторов на поверхности частиц дисперсной фазы и образованием слоя.
Коллоидная защита широко используется при получении устойчивых лиофобных золей, применяемых в качестве лекарственных препаратов. Например, колларгол и протаргол содержат 8 и 70% высокодисперсного металлического серебра, стабилизированного гидролизатами белков.Коллоидная защита играет существенную роль в физиологических процессах. Содержание карбоната и фосфата кальция в крови значительно превышает их растворимость в воде. Отложению этих солей препятствуют защитные вещества крови, которые не позволяют коллоидным частицам нерастворимых солей объединяться в крупные агрегаты и осаждаться. Образование желчных и мочевых камней в организме связано с уменьшением при патологических состояниях защитного действия определенных веществ по отношению к билирубину, холестерину и уратам.
Задачи для самостоятельного решения:
1. Напишите формулу мицеллы для золя иодида серебра, полученного при добавлении к раствору KI объемом 30 мл с концентрацией 0,006 моль/л раствор AgNO3 объемом 40 мл с концентрацией 0,004 моль/л. Назовите части мицеллы.
2. Напишите формулу мицеллы для золя, полученного смешением 20 мл 0,01 моль/л раствора сульфата натрия и 50 мл 0,004 моль/л раствора хлорида бария.
3. Напишите формулу мицеллы для золя, полученного смешением 30 мл 0,01 моль/л раствора сульфата натрия и 20 мл 0,04 моль/л раствора хлорида бария.
4. Коагуляция золя сульфида золота объемом 650 мл наступила при добавлении раствора сульфата хрома (III) объемом 1,18 мл с концентрацией 0,025 моль/л. Вычислите порог коагуляции золя сульфат-ионами.
5. Золь бромистого серебра получен путем смешивания равных объемов 0,008 н раствора бромистого калия и 0,0096 н раствора азотнокислого серебра. Определить знак заряда частиц золя и написать формулу его мицеллы.
6. Коагуляция гидроксида алюминия объемом 2 л наступила при добавлении раствора гексацианоферрата (II) калия объемом 10,6 мл с концентрацией 0,01 моль/л. Вычислите порог коагуляции золя гексацианоферрат (II)-ионами.
 2015-01-21
2015-01-21 4302
4302