Воспользовавшись формулой пересчета массовой доли (ω′) МgSO4 в нормальную концентрацию (см. табл. 7.2), определим СN разбавленного раствора (М (МgSO4) = 120 г/моль; ω = 2 % = 0,02):
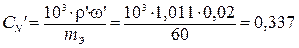 моль-экв/л, или 0,33 н.
моль-экв/л, или 0,33 н.
Объем концентрированного раствора МgSO4 вычислим из соотношения (7.1). Учтем СN = СМ ∙ n (MgSO4) = 1,1∙2 = 2,2 моль-экв/л.
СN′∙V′ = CN∙V,
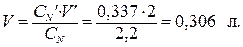
Пример 5. Для нейтрализации 100 мл раствора серной кислоты потребовалось 20 мл 0,5 н раствора гидроксида натрия. Вычислите нормальность раствора Н2SO4 и массу кислоты в этом растворе.
 2015-02-27
2015-02-27 557
557








