Химический анализ – это совокупность методов, с помощью которых определяют химический состав веществ. Химический анализ разделяют на качественный и количественный.
Задача качественного анализа – идентификация веществ, т. е. обнаружение наличия химических элементов в соединениях или химических соединений в смесях. Задача количественного анализа – определение количеств элементов или их соединений в исследуемом веществе.
Химический анализ – сложный многостадийный процесс, состоящий из нескольких этапов: отбор пробы, выбор метода анализа, подготовка пробы к анализу, проведение измерений, обработка результатов измерений.
Одно из ключевых понятий химического анализа – аналитический сигнал, который представляет собой экспериментальную информацию о качественном и количественном составе исследуемого вещества.
Методы идентификации веществ основаны на получении аналитического сигнала в результате проведения химической реакции. Определяемый ион или элемент переводят в другое химическое соединение, обладающее характерными свойствами (выпадение осадка, выделение газа, изменение окраски и т. д.). Данные изменения указывают на присутствие того или иного иона (элемента, групп ионов) в пробе. При проведении качественного анализа используют систематический и дробный методы. Систематический метод основан на разделении смеси ионов на группы и подгруппы с помощью групповых реагентов. Дробный метод основан на определении данного элемента или иона в анализируемом образце с помощью качественной реакции (см. табл. 14.1 и 14.2).
При проведении количественного анализа аналитическим сигналом является физическая величина, функционально связанная с содержанием компонента. По величине этого сигнала (массе осадка, силе тока, интенсивности линий спектра и т. д.) рассчитывают содержание компонента в исследуемом образце.
Для количественного определения концентраций (количеств) химических элементов (соединений) и их форм в анализируемом образце используют методы химические и инструментальные (физико-химические и физические). К химическим методам относятся гравиметрический (весовой) анализ и волюмометрический (объемный) анализ. Волюмометрические методы в зависимости от агрегатного состояния вещества делятся на газоволюмометрические, основанные на измерении объема газа, и титриметрические, основанные на измерении объема жидкого реагента (титранта) с известной концентрацией, взаимодействующего с определяемым веществом
Таблица 14.1
Качественные реакции на катионы
| Катион | Реактив | Аналитический признак реакции | |||
| K+ | Кобальтонитрит натрия Na3[Co(NO2)6] в нейтральной или уксуснокислой среде | Жидкий кристаллический осадок K2Na[Co(NO2)6] | |||
| Гидротартрат натрия (NaHC4H4O6) в нейтральной среде при охлаждении | Белый кристаллический осадок гидротартрата калия | ||||
| Действие на пламя | Фиолетовое окрашивание, видимое через кобальтовое стекло | ||||
| Na+ | Ацетат уранила UO2(CH3COO)2 в уксуснокислой среде | Зеленовато-желтый кристаллический осадок двойной соли | |||
| Дигидроантимонат калия в нейтральной или слабощелочной среде | Белый кристаллический осадок дигидроантимоната натрия | ||||
| Действие на пламя | Желтое окрашивание | ||||
| NH4+ | Едкая щелочь при нагревании | Выделяется аммиак, который обнаруживают по посинению лакмусовой бумаги или по почернению фильтровальной бумаги, пропитанной раствором ртути (II) | |||
| Реактив Несслера (смесь растворов K2[HgI4] и KOH) | Красно-бурый осадок NH2Hg2I3 | ||||
| Ba2+ | Хромат калия (K2CrO4) в уксуснокислой среде или бихромат калия (K2Cr2O7) при добавлении ацетата натрия | Светло-желтый осадок хромата бария | |||
| Действие на пламя | Желто-зеленое окрашивание | ||||
| Ca2+ | Оксалат аммония (NH4)2C2O4 в уксуснокислой среде | Белый кристаллический осадок | |||
| Действие на пламя | Кирпично-красное окрашивание | ||||
| Al3+ | Ализарин красный S в слабокислой среде при отсутствии катионов железа (III) | Красный осадок или красное окрашивание | |||
| Едкая щелочь в избытке хлорида аммония (кипячение) | Белый осадок гидроксида алюминия | ||||
  Fe2+ Fe2+ | Феррицианид калия   K3[Fe(CN)6] (красная кровяная соль) K3[Fe(CN)6] (красная кровяная соль) | Темно-синий осадок феррицианида
Окончание табл. 14.1 железа (II) (турнбулева синь) | |||
| Катион | Реактив | Аналитический признак реакции | |||
| Fe3+ | Ферроцианид калия K4[Fe(CN)6] (желтая кровяная соль) | Темно-синий осадок ферроцианида железа (III) (берлинская лазурь) | |||
| Роданид калия (KSCN) или роданид аммония (NH4CNS) | Кроваво-красное окрашивание | ||||
| Zn2+ | Сероводород (H2S) при pH = 2,5 | Белый осадок сульфида цинка | |||
| Ag+ | Соляная кислота (HCl) | Белый осадок, растворимый в аммиаке и нерастворимый в азотной кислоте | |||
| Pb2+ | Йодид калия (KI) | Желтый осадок йодида свинца, растворимый в горячей воде | |||
| Серная кислота (H2SO4) | Белый осадок, растворимый в щелочи | ||||
| Cu2+ | Избыток аммиака | Раствор темно-синего цвета – аммиакат меди | |||
| Желтая кровяная соль K4[Fe(CN)6] и соляная кислота (HCl) | Кроваво-красный осадок |
Гравиметрический метод основан на точном измерении массы определяемого компонента пробы анализируемого вещества, выделенного в виде соединения определенного состава. Гравиметрическое определение методом осаждения проводят в несколько этапов. Навеску анализируемого вещества растворяют, после чего определяемый элемент осаждают в виде какого-либо малорастворимого соединения, называемого осаждаемой формой. Выпавший осадок отделяют фильтрованием, тщательно промывают и прокаливают. Полученную так называемую гравиметрическую форму взвешивают, и по массе осадка и его химической формуле рассчитывают массовую долю ω определяемого компонента в анализируемом веществе:
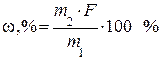 , , | (14.1) |
где m 1 – масса навески вещества, взятого для анализа;
m 2 – масса гравиметрической формы;
F – гравиметрический фактор.
Гравиметрическим фактором называют отношение молярной массы M 1 определяемого компонента к молярной массе M 2 гравиметрической формы.
Таблица 14.2
Качественные реакции на анионы
| Анион | Реактив | Аналитический признак реакции |
| Cl– | Нитрат серебра в азотно-кислой среде | Белый осадок хлорида серебра, растворимый в избытке аммиака |
| Br– | Хлорная вода | Окисление бромид-иона до Br2, который окрашивает органический растворитель в желтый цвет |
| I– | Хлорная вода или нитрат калия | Окисление йодид-иона до I2, который окрашивает крахмал в синий цвет, а органический растворитель в красно-фиолетовый |
| CO32– | Разбавленные кислоты | Выделение CO2 обнаруживается по помутнению известковой воды |
| SO42– | Хлорид бария | Белый осадок, нерастворимый в азотной кислоте |
| PO43– | Магнезиальная смесь (MgCl2 + NH4OH + NH4Cl) | Белый осадок |
| NO3– | Дифениламин | Синее окрашивание |
 2015-02-27
2015-02-27 12688
12688

