Теория Хюккеля сыграла выдающуюся роль в формировании теоретических основ органической химии. Множество концептуально важных понятий современной химии восходят к простому методу Хюккеля. Однако простота хюккелевской вычислительной схемы – оборотная сторона её недостатков. Среди основных недостатков метода – неучёт межчастичных взаимодействий. Это приводит к тому, что например изомеры, описываемые одной топологической матрицей и, как следствие, имеющие один и тот же набор молекулярных орбиталей, при расчётах оказываются неразличимыми. Так, ранее нами уже были рассмотрены приближения, присущие методу молекулярных орбиталей. Метод Хюккеля, помимо этих, содержит ряд дальнейших приближений, приемлемость которых в рамках более строгих теорий становится весьма сомнительной. Возникает вполне резонный вопрос, до какой степени можно оправдать эти приближения? Прежде всего, метод Хюккеля практически полезен потому, что не ставит перед собой слишком далеко идущих целей. В силу этого обстоятельства, в рамках метода Хюккеля практически невозможно получить количественное согласие экспериментальных и расчётных характеристик молекул. Действительно, метод Хюккеля не применяется для последовательного теоретического вычисления, каких – либо отдельных величин; он лишь позволяет установить связь одних экспериментальных данных с другими. Вычисляемые энергии, электронные плотности и другие величины выражены через параметры 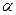 и
и  . Формально эти параметры определены как интегралы, содержащие одноэлектронный гамильтониан
. Формально эти параметры определены как интегралы, содержащие одноэлектронный гамильтониан 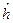 , однако связь этого гамильтониана с полным гамильтонианом не конкретизируется. Если в молекуле нет гетероатомов, то все относительные энергии в приближении Хюккеля выражаются через один параметр
, однако связь этого гамильтониана с полным гамильтонианом не конкретизируется. Если в молекуле нет гетероатомов, то все относительные энергии в приближении Хюккеля выражаются через один параметр  . Это означает, что должно существовать линейное соотношение между экспериментальными значениями энергии и энергиями Хюккеля, а тангенс угла наклона соответствующей прямой определяется значением
. Это означает, что должно существовать линейное соотношение между экспериментальными значениями энергии и энергиями Хюккеля, а тангенс угла наклона соответствующей прямой определяется значением  . Перенос значений
. Перенос значений 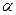 и
и  , полученных для одного класса соединений в другой (например, из полиенов в ароматические соединения), недопустим и приводит к ошибкам. Внутри же одного класса соединений такой перенос возможен и даёт при расчёте приемлемые результаты. Так, в пределах одного класса соединений, имеет место хорошая корреляция экспериментальных и теоретически рассчитанных характеристик молекул. Однако значения
, полученных для одного класса соединений в другой (например, из полиенов в ароматические соединения), недопустим и приводит к ошибкам. Внутри же одного класса соединений такой перенос возможен и даёт при расчёте приемлемые результаты. Так, в пределах одного класса соединений, имеет место хорошая корреляция экспериментальных и теоретически рассчитанных характеристик молекул. Однако значения  , получающиеся во всех случаях, довольно сильно различаются между собой. Причина такого расхождения заключается в следующем: для вычисления энергии нужно использовать полный гамильтониан молекул, а не одноэлектронный гамильтониан метода Хюккеля. Если это учесть, то оказывается, что такие величины как энергии возбуждения, сродства к электрону и энергии диссоциации, выражаются не только через одни электронные интегралы типа
, получающиеся во всех случаях, довольно сильно различаются между собой. Причина такого расхождения заключается в следующем: для вычисления энергии нужно использовать полный гамильтониан молекул, а не одноэлектронный гамильтониан метода Хюккеля. Если это учесть, то оказывается, что такие величины как энергии возбуждения, сродства к электрону и энергии диссоциации, выражаются не только через одни электронные интегралы типа 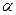 и
и  , но зависят также от интегралов, описывающих межэлектронное взаимодействие. Принимая
, но зависят также от интегралов, описывающих межэлектронное взаимодействие. Принимая  как электрический параметр, можно в некоторых случаях (но не всегда) компенсировать пренебрежение этими интегралами. Но теперь при описании различных свойств молекул
как электрический параметр, можно в некоторых случаях (но не всегда) компенсировать пренебрежение этими интегралами. Но теперь при описании различных свойств молекул  представляет собою различные комбинации интегралов, и потому значения
представляет собою различные комбинации интегралов, и потому значения  , приводящие к согласию вычислений с экспериментальными данными в одном случае, могут отличаться от значений, являющихся наиболее подходящими для результатов экспериментов в другом случае. Именно поэтому не существует единых для всех молекул с гетероатомами значений параметров
, приводящие к согласию вычислений с экспериментальными данными в одном случае, могут отличаться от значений, являющихся наиболее подходящими для результатов экспериментов в другом случае. Именно поэтому не существует единых для всех молекул с гетероатомами значений параметров 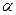 и
и  . Значение
. Значение 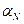 , при котором лучше всего описывается основность содержащих азот гетероциклов, не обязательно является наилучшим для предсказания плотности неспаренного электрона в азотсодержащих радикалах, потому что
, при котором лучше всего описывается основность содержащих азот гетероциклов, не обязательно является наилучшим для предсказания плотности неспаренного электрона в азотсодержащих радикалах, потому что 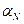 при вычислении этих двух характеристик молекул выражает различные комбинации одно - и двухэлектронных интегралов. Изначально метод Хюккеля был разработан для изучения строения и свойств плоских сопряжённых углеводородов, и попытки его обобщения для расчёта более широкого набора молекулярных структур, к сожалению, оказались не столь удачными. Однако даже для случая сопряжённых систем известны молекулы, когда метод Хюккеля в его простейшей форме даёт довольно плохие результаты. Например, частота возбуждения молекулы бутадиена, вычисленная в рамках хюккелевского расчёта, составляет 35300 см-1, а экспериментальное значение равно 46100 см-1. Причина такого расхождения состоит в том, что не все длины связей в молекуле бутадиена одинаковы, а потому использование одного и того же значения
при вычислении этих двух характеристик молекул выражает различные комбинации одно - и двухэлектронных интегралов. Изначально метод Хюккеля был разработан для изучения строения и свойств плоских сопряжённых углеводородов, и попытки его обобщения для расчёта более широкого набора молекулярных структур, к сожалению, оказались не столь удачными. Однако даже для случая сопряжённых систем известны молекулы, когда метод Хюккеля в его простейшей форме даёт довольно плохие результаты. Например, частота возбуждения молекулы бутадиена, вычисленная в рамках хюккелевского расчёта, составляет 35300 см-1, а экспериментальное значение равно 46100 см-1. Причина такого расхождения состоит в том, что не все длины связей в молекуле бутадиена одинаковы, а потому использование одного и того же значения  для всех связей является грубым приближением. Хотя параметр
для всех связей является грубым приближением. Хотя параметр  не достаточно хорошо определён как величина, всё же ясно, что он должен быть приближённо связан с перекрыванием включённых в связь двух атомных орбиталей и с увеличением длины связи происходит его уменьшение по экспоненте. Для молекул, где имеет место сильное альтернирование связей, как, например, в сопряжённых полиенах, существенно, чтобы зависимость
не достаточно хорошо определён как величина, всё же ясно, что он должен быть приближённо связан с перекрыванием включённых в связь двух атомных орбиталей и с увеличением длины связи происходит его уменьшение по экспоненте. Для молекул, где имеет место сильное альтернирование связей, как, например, в сопряжённых полиенах, существенно, чтобы зависимость  от длины связи была учтена. Другой случай, когда нужно учитывать изменение
от длины связи была учтена. Другой случай, когда нужно учитывать изменение  , представляют молекулы, в которых участвующие в сопряжении атомы углерода не лежат в одной плоскости. Интересно отметить, что результаты, получаемые в рамках метода Хюккеля для альтернантных углеводородов, лучше, чем те, что получают для неальтернантных. Подведём некоторые итоги. Метод Хюккеля есть установления корелляционных связей между экспериментальными данными для классов родственных соединений. Это особенно полезно, когда рассматриваемый класс содержит большое число соединений (например, все ароматические углеводороды), а число используемых параметров мало. При переходе к системам, содержащим гетероатомы, как наблюдается, число параметров, которые следует определить на основе эксперимента, быстро растёт, и в то же время число молекул в каждом классе становится меньшим. Поэтому параметры, характеризующие гетероатомы, до сих пор твёрдо не установлены. Параметры в методе Хюккеля заменяют собою сложные интегралы, появляющиеся в любом неэмпирическом расчётном методе. По этой причине лучшие значения параметров зависят от того, какая экспериментально наблюдаемая характеристика исследуется. В целом же, при объяснении строения и свойств сопряжённых систем (ароматических углеводородов, их замещённых, линейных полиенов, радикальных частиц), объяснения их реакционной способности, интерпретации спектров, метод Хюккеля даёт вполне удовлетворительные результаты. По этим причинам, не смотря на развитие более точных полуэмпирических методов и расчётов ab initio, необходимо ознакомиться с методом Хюккеля. Кроме всего прочего, все другие полуэмпирические методы в той или иной степени имеют черты, сходные с методом Хюккеля, и знакомство с ним даёт общее представление о полуэмпирических методах квантовохимических расчётов и может облегчить понимание этих методов. Значение хюккелевской теории прекрасно охарактеризовали Вудворд и Хофман. Они писали, что последние годы «были отмечены плодотворным симбиозом органической химии и теории молекулярных орбиталей. По необходимости это был брачный союз плохой теории с хорошим экспериментом. В руках умных экспериментаторов эти идеи трансформировались в новые молекулы с необычными свойствами». На сегодняшний день в связи с бурным развитием вычислительной техники и широким внедрением более совершенных вычислительных схем квантовой химии метод Хюккеля перестал играть заметную роль в исследовании структуры и свойств органических соединений. На передний план выдвинулись методики, явно учитывающие межэлектронное взаимодействие.
, представляют молекулы, в которых участвующие в сопряжении атомы углерода не лежат в одной плоскости. Интересно отметить, что результаты, получаемые в рамках метода Хюккеля для альтернантных углеводородов, лучше, чем те, что получают для неальтернантных. Подведём некоторые итоги. Метод Хюккеля есть установления корелляционных связей между экспериментальными данными для классов родственных соединений. Это особенно полезно, когда рассматриваемый класс содержит большое число соединений (например, все ароматические углеводороды), а число используемых параметров мало. При переходе к системам, содержащим гетероатомы, как наблюдается, число параметров, которые следует определить на основе эксперимента, быстро растёт, и в то же время число молекул в каждом классе становится меньшим. Поэтому параметры, характеризующие гетероатомы, до сих пор твёрдо не установлены. Параметры в методе Хюккеля заменяют собою сложные интегралы, появляющиеся в любом неэмпирическом расчётном методе. По этой причине лучшие значения параметров зависят от того, какая экспериментально наблюдаемая характеристика исследуется. В целом же, при объяснении строения и свойств сопряжённых систем (ароматических углеводородов, их замещённых, линейных полиенов, радикальных частиц), объяснения их реакционной способности, интерпретации спектров, метод Хюккеля даёт вполне удовлетворительные результаты. По этим причинам, не смотря на развитие более точных полуэмпирических методов и расчётов ab initio, необходимо ознакомиться с методом Хюккеля. Кроме всего прочего, все другие полуэмпирические методы в той или иной степени имеют черты, сходные с методом Хюккеля, и знакомство с ним даёт общее представление о полуэмпирических методах квантовохимических расчётов и может облегчить понимание этих методов. Значение хюккелевской теории прекрасно охарактеризовали Вудворд и Хофман. Они писали, что последние годы «были отмечены плодотворным симбиозом органической химии и теории молекулярных орбиталей. По необходимости это был брачный союз плохой теории с хорошим экспериментом. В руках умных экспериментаторов эти идеи трансформировались в новые молекулы с необычными свойствами». На сегодняшний день в связи с бурным развитием вычислительной техники и широким внедрением более совершенных вычислительных схем квантовой химии метод Хюккеля перестал играть заметную роль в исследовании структуры и свойств органических соединений. На передний план выдвинулись методики, явно учитывающие межэлектронное взаимодействие.
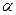 и
и  . Формально эти параметры определены как интегралы, содержащие одноэлектронный гамильтониан
. Формально эти параметры определены как интегралы, содержащие одноэлектронный гамильтониан 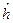 , однако связь этого гамильтониана с полным гамильтонианом не конкретизируется. Если в молекуле нет гетероатомов, то все относительные энергии в приближении Хюккеля выражаются через один параметр
, однако связь этого гамильтониана с полным гамильтонианом не конкретизируется. Если в молекуле нет гетероатомов, то все относительные энергии в приближении Хюккеля выражаются через один параметр  . Это означает, что должно существовать линейное соотношение между экспериментальными значениями энергии и энергиями Хюккеля, а тангенс угла наклона соответствующей прямой определяется значением
. Это означает, что должно существовать линейное соотношение между экспериментальными значениями энергии и энергиями Хюккеля, а тангенс угла наклона соответствующей прямой определяется значением  . Перенос значений
. Перенос значений 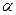 и
и  , полученных для одного класса соединений в другой (например, из полиенов в ароматические соединения), недопустим и приводит к ошибкам. Внутри же одного класса соединений такой перенос возможен и даёт при расчёте приемлемые результаты. Так, в пределах одного класса соединений, имеет место хорошая корреляция экспериментальных и теоретически рассчитанных характеристик молекул. Однако значения
, полученных для одного класса соединений в другой (например, из полиенов в ароматические соединения), недопустим и приводит к ошибкам. Внутри же одного класса соединений такой перенос возможен и даёт при расчёте приемлемые результаты. Так, в пределах одного класса соединений, имеет место хорошая корреляция экспериментальных и теоретически рассчитанных характеристик молекул. Однако значения  , получающиеся во всех случаях, довольно сильно различаются между собой. Причина такого расхождения заключается в следующем: для вычисления энергии нужно использовать полный гамильтониан молекул, а не одноэлектронный гамильтониан метода Хюккеля. Если это учесть, то оказывается, что такие величины как энергии возбуждения, сродства к электрону и энергии диссоциации, выражаются не только через одни электронные интегралы типа
, получающиеся во всех случаях, довольно сильно различаются между собой. Причина такого расхождения заключается в следующем: для вычисления энергии нужно использовать полный гамильтониан молекул, а не одноэлектронный гамильтониан метода Хюккеля. Если это учесть, то оказывается, что такие величины как энергии возбуждения, сродства к электрону и энергии диссоциации, выражаются не только через одни электронные интегралы типа 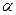 и
и  , но зависят также от интегралов, описывающих межэлектронное взаимодействие. Принимая
, но зависят также от интегралов, описывающих межэлектронное взаимодействие. Принимая  как электрический параметр, можно в некоторых случаях (но не всегда) компенсировать пренебрежение этими интегралами. Но теперь при описании различных свойств молекул
как электрический параметр, можно в некоторых случаях (но не всегда) компенсировать пренебрежение этими интегралами. Но теперь при описании различных свойств молекул  представляет собою различные комбинации интегралов, и потому значения
представляет собою различные комбинации интегралов, и потому значения  , приводящие к согласию вычислений с экспериментальными данными в одном случае, могут отличаться от значений, являющихся наиболее подходящими для результатов экспериментов в другом случае. Именно поэтому не существует единых для всех молекул с гетероатомами значений параметров
, приводящие к согласию вычислений с экспериментальными данными в одном случае, могут отличаться от значений, являющихся наиболее подходящими для результатов экспериментов в другом случае. Именно поэтому не существует единых для всех молекул с гетероатомами значений параметров 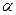 и
и  . Значение
. Значение 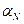 , при котором лучше всего описывается основность содержащих азот гетероциклов, не обязательно является наилучшим для предсказания плотности неспаренного электрона в азотсодержащих радикалах, потому что
, при котором лучше всего описывается основность содержащих азот гетероциклов, не обязательно является наилучшим для предсказания плотности неспаренного электрона в азотсодержащих радикалах, потому что 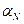 при вычислении этих двух характеристик молекул выражает различные комбинации одно - и двухэлектронных интегралов. Изначально метод Хюккеля был разработан для изучения строения и свойств плоских сопряжённых углеводородов, и попытки его обобщения для расчёта более широкого набора молекулярных структур, к сожалению, оказались не столь удачными. Однако даже для случая сопряжённых систем известны молекулы, когда метод Хюккеля в его простейшей форме даёт довольно плохие результаты. Например, частота возбуждения молекулы бутадиена, вычисленная в рамках хюккелевского расчёта, составляет 35300 см-1, а экспериментальное значение равно 46100 см-1. Причина такого расхождения состоит в том, что не все длины связей в молекуле бутадиена одинаковы, а потому использование одного и того же значения
при вычислении этих двух характеристик молекул выражает различные комбинации одно - и двухэлектронных интегралов. Изначально метод Хюккеля был разработан для изучения строения и свойств плоских сопряжённых углеводородов, и попытки его обобщения для расчёта более широкого набора молекулярных структур, к сожалению, оказались не столь удачными. Однако даже для случая сопряжённых систем известны молекулы, когда метод Хюккеля в его простейшей форме даёт довольно плохие результаты. Например, частота возбуждения молекулы бутадиена, вычисленная в рамках хюккелевского расчёта, составляет 35300 см-1, а экспериментальное значение равно 46100 см-1. Причина такого расхождения состоит в том, что не все длины связей в молекуле бутадиена одинаковы, а потому использование одного и того же значения  для всех связей является грубым приближением. Хотя параметр
для всех связей является грубым приближением. Хотя параметр  не достаточно хорошо определён как величина, всё же ясно, что он должен быть приближённо связан с перекрыванием включённых в связь двух атомных орбиталей и с увеличением длины связи происходит его уменьшение по экспоненте. Для молекул, где имеет место сильное альтернирование связей, как, например, в сопряжённых полиенах, существенно, чтобы зависимость
не достаточно хорошо определён как величина, всё же ясно, что он должен быть приближённо связан с перекрыванием включённых в связь двух атомных орбиталей и с увеличением длины связи происходит его уменьшение по экспоненте. Для молекул, где имеет место сильное альтернирование связей, как, например, в сопряжённых полиенах, существенно, чтобы зависимость  от длины связи была учтена. Другой случай, когда нужно учитывать изменение
от длины связи была учтена. Другой случай, когда нужно учитывать изменение  , представляют молекулы, в которых участвующие в сопряжении атомы углерода не лежат в одной плоскости. Интересно отметить, что результаты, получаемые в рамках метода Хюккеля для альтернантных углеводородов, лучше, чем те, что получают для неальтернантных. Подведём некоторые итоги. Метод Хюккеля есть установления корелляционных связей между экспериментальными данными для классов родственных соединений. Это особенно полезно, когда рассматриваемый класс содержит большое число соединений (например, все ароматические углеводороды), а число используемых параметров мало. При переходе к системам, содержащим гетероатомы, как наблюдается, число параметров, которые следует определить на основе эксперимента, быстро растёт, и в то же время число молекул в каждом классе становится меньшим. Поэтому параметры, характеризующие гетероатомы, до сих пор твёрдо не установлены. Параметры в методе Хюккеля заменяют собою сложные интегралы, появляющиеся в любом неэмпирическом расчётном методе. По этой причине лучшие значения параметров зависят от того, какая экспериментально наблюдаемая характеристика исследуется. В целом же, при объяснении строения и свойств сопряжённых систем (ароматических углеводородов, их замещённых, линейных полиенов, радикальных частиц), объяснения их реакционной способности, интерпретации спектров, метод Хюккеля даёт вполне удовлетворительные результаты. По этим причинам, не смотря на развитие более точных полуэмпирических методов и расчётов ab initio, необходимо ознакомиться с методом Хюккеля. Кроме всего прочего, все другие полуэмпирические методы в той или иной степени имеют черты, сходные с методом Хюккеля, и знакомство с ним даёт общее представление о полуэмпирических методах квантовохимических расчётов и может облегчить понимание этих методов. Значение хюккелевской теории прекрасно охарактеризовали Вудворд и Хофман. Они писали, что последние годы «были отмечены плодотворным симбиозом органической химии и теории молекулярных орбиталей. По необходимости это был брачный союз плохой теории с хорошим экспериментом. В руках умных экспериментаторов эти идеи трансформировались в новые молекулы с необычными свойствами». На сегодняшний день в связи с бурным развитием вычислительной техники и широким внедрением более совершенных вычислительных схем квантовой химии метод Хюккеля перестал играть заметную роль в исследовании структуры и свойств органических соединений. На передний план выдвинулись методики, явно учитывающие межэлектронное взаимодействие.
, представляют молекулы, в которых участвующие в сопряжении атомы углерода не лежат в одной плоскости. Интересно отметить, что результаты, получаемые в рамках метода Хюккеля для альтернантных углеводородов, лучше, чем те, что получают для неальтернантных. Подведём некоторые итоги. Метод Хюккеля есть установления корелляционных связей между экспериментальными данными для классов родственных соединений. Это особенно полезно, когда рассматриваемый класс содержит большое число соединений (например, все ароматические углеводороды), а число используемых параметров мало. При переходе к системам, содержащим гетероатомы, как наблюдается, число параметров, которые следует определить на основе эксперимента, быстро растёт, и в то же время число молекул в каждом классе становится меньшим. Поэтому параметры, характеризующие гетероатомы, до сих пор твёрдо не установлены. Параметры в методе Хюккеля заменяют собою сложные интегралы, появляющиеся в любом неэмпирическом расчётном методе. По этой причине лучшие значения параметров зависят от того, какая экспериментально наблюдаемая характеристика исследуется. В целом же, при объяснении строения и свойств сопряжённых систем (ароматических углеводородов, их замещённых, линейных полиенов, радикальных частиц), объяснения их реакционной способности, интерпретации спектров, метод Хюккеля даёт вполне удовлетворительные результаты. По этим причинам, не смотря на развитие более точных полуэмпирических методов и расчётов ab initio, необходимо ознакомиться с методом Хюккеля. Кроме всего прочего, все другие полуэмпирические методы в той или иной степени имеют черты, сходные с методом Хюккеля, и знакомство с ним даёт общее представление о полуэмпирических методах квантовохимических расчётов и может облегчить понимание этих методов. Значение хюккелевской теории прекрасно охарактеризовали Вудворд и Хофман. Они писали, что последние годы «были отмечены плодотворным симбиозом органической химии и теории молекулярных орбиталей. По необходимости это был брачный союз плохой теории с хорошим экспериментом. В руках умных экспериментаторов эти идеи трансформировались в новые молекулы с необычными свойствами». На сегодняшний день в связи с бурным развитием вычислительной техники и широким внедрением более совершенных вычислительных схем квантовой химии метод Хюккеля перестал играть заметную роль в исследовании структуры и свойств органических соединений. На передний план выдвинулись методики, явно учитывающие межэлектронное взаимодействие. 2015-03-22
2015-03-22 616
616







