Для выполнения задач необходимо помнить, что решение задачи начинается с написания химического уравнения реакции.
Химическое уравнение – это изображение химической реакции посредством химических формул. В химическом уравнении формула каждого вещества отражает качественный состав молекул, количественной соотношение элементов в этой молекуле, а также молярную массу. Коэффициенты в уравнениях реакций указывают в каких молярных соотношениях вещество взаимодействует.
Например: уравнение синтеза метанола с обозначением количества исходного и образующегося веществ можно изобразить следующим образом.
 СО + 2Н2 СН3ОН
СО + 2Н2 СН3ОН
Число молей 1м 2м 1м
Молярная масса 28г/моль 2*2г/моль 32г/моль
Составив уравнение химической реакции и определив по нему число молей реагирующих и образующих веществ можно производить различные расчеты по определению количеств нужного вещества.
Массу веществ, участвующих в реакции, рассчитывают исходя из величин молярных масс.
Молярная масса М – производная величина, связывающая массу и количество.
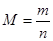 ;
;
где m – масса вещества; г,кг,т
n – количество вещества; моль, кмоль
М – молярная масса; г/моль, кг/моль.
Например: Масса СН4 количеством вещества 1 моль определяется по формуле.
m = n * M
m = 1 моль * 16 г/моль = 16 г
Масса С6Н6 количеством вещества 1 моль определяется по формуле:
m = n * M
m = 1 моль * 78 г/моль = 78 г
Если в реакции участвуют газообразные вещества, то по уравнению этой реакции можно выразить не только отношение масс этих газов, но и отношение объемов.
 СО + 2Н2 СН3ОН
СО + 2Н2 СН3ОН
Число молей 1м 2м 1м
газа
Объем газа 1*22,4л/моль 2*22,4л/моль 1*22,4л/моль
при нормальных условиях
л/моль, м3/моль
Объемы реагирующих в процессе химической реакции веществ вычисляют исходя из молярных количеств этих веществ и молярных объемов.
Молярный объем Vм – производная величина, связывающая объем и количество вещества.
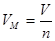
где V – объем вещества, л, м3
n – количество вещества, моль, кмоль
VM – молярный объем, л/моль, м3/моль.
Например: Масса СН4 количеством вещества 1 моль определяется по формуле.
V = n * VM
V = 1 моль * 22.4 л/моль = 22,4л
Масса С6Н6 количеством вещества 1 моль определяется по формуле:
V = n * VM
V = 1 моль * 22.4 л/моль = 22,4л
Так как по закону Авогадро молярные объемы газов при нормальных условиях равны между собой, то соотношение объемов газов, вступивших в реакцию, пропорционально соотношению их коэффициентов в уравнении реакции. Поэтому объем газа можно вычислить непосредственно по уравнению химической реакции, не рассчитывая его массу.
Например: Какой объем кислорода потребуется для сжигания 25 литров этана?
Решение:
25л Х


 2С2Н6 + 7О2 4СО2 + 6Н2О
2С2Н6 + 7О2 4СО2 + 6Н2О
2м 7м
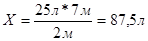

При решении задач по химическим уравнениям необходимо соблюдать определенную последовательность:
 2015-03-07
2015-03-07 386
386








