Задача 1. В крови больного обнаружены патологические белки, не существующие в нормальных условиях. Как называется это состояние? О каком заболевании свидетельствует появление миеломных белков?
Ответ. Появление в плазме крови «патологических белков» называют парапротеинемией, с ней часто связано увеличение общего содержания белков до 100-160 г/л. Так, у больных миеломной болезнью в сыворотке крови появляются специфические миеломные белки (тяжелые или легкие цепи иммуноглобулинов). Они могут преодолевать почечный барьер и появляются в моче, при этом их называют белковыми телами Бенс-Джонса.
Задача 2. Дикумарол и варфарин являются структурными аналогами витамина К и применяются в клинике как антикоагулянты для профилактики тромбозов. Почему эти лекарства не влияют на свертывание крови invitro(в пробирке)? При ответе: а) укажите, коферментом какого фермента является витамин К; б) перечислите плазменные факторы свертывания крови, в посттрансляционной модификации которых принимает участие витамин К.
Подготовьте к предстоящему занятию протокол лабораторных работ: выпишите кратко принципы методов и техники их выполнения, показатели нормы, оставляя место для расчетов и выводов.
Ответ.
Поступивший в организм витамин К (нафтохинон) восстанавливается в печени НАДФН-зависимой витамин К-редуктазой с образованием дигидрохинона витамина К, служащего коферментом глутамат-карбоксилазы, катализирующей карбоксилирование остатков глутаминовой кислоты в проферментах прокоагулянтного пути (фф.II, VII, IX,X) в γ-карбоксиглутаминовую. Остатки γ-карбоксиглутаминовой кислоты в факторах IIa,VIIa, IXa,Xa обеспечивают их взаимодействие посредством Са2+ с отрицательно заряженными фосфолипидами клеточных мембран и другими белками. Факторы VIIa иIXa участвуют в превращении фX →фXa (I фаза), фХа – в превращении фII→фIIa, а последний – в III фазе (образовании фибрина). Таким образом, витамин К необходим для созревания некоторых плазменных факторов свертывания крови в печени и непосредственного участия в процессах гемокоагуляции не принимает и, следовательно, его структурные аналоги дикумарол и варфарин не могут тормозить свертывание крови в пробирке
Задача 3. В странах Средиземноморья в пищу используют конские бобы. Однако их потребление может привести к развитию тяжелого гемолиза у лиц, страдающих дефицитом глюкозо-6-фосфатдегидрогеназы. Клинически состояние таких больных выражается в бледности кожных покровов, гемоглобинурии, желтухе и тяжелой форме анемии в течение 24–48 часов после употребления конских бобов в пищу. Конские бобы содержат гликозид вицин и изоурамил, которые, как считается, разрушают глюкозо-6-фосфатдегидрогеназу. Такая патология имеет название «фавизм».
Объясните молекулярную основу гемолиза при данной патологии.
Для этого:
а) представьте метаболический путь в эритроцитах, в котором участвует глюкозо-6-фосфатдегидрогеназа;
б) опишите, как в норме нейтрализуются активные формы кислорода (АФК) в эритроцитах и последствия воздействия АФК на клетку?
Ответ.
а) Пентозофосфатный способ превращения глюкозы происходит в цитозоле клеток и выполняет следующие основные функции:
• образование NADPH;
• источник рибозо-5-фосфата для синтеза нуклеотидов.
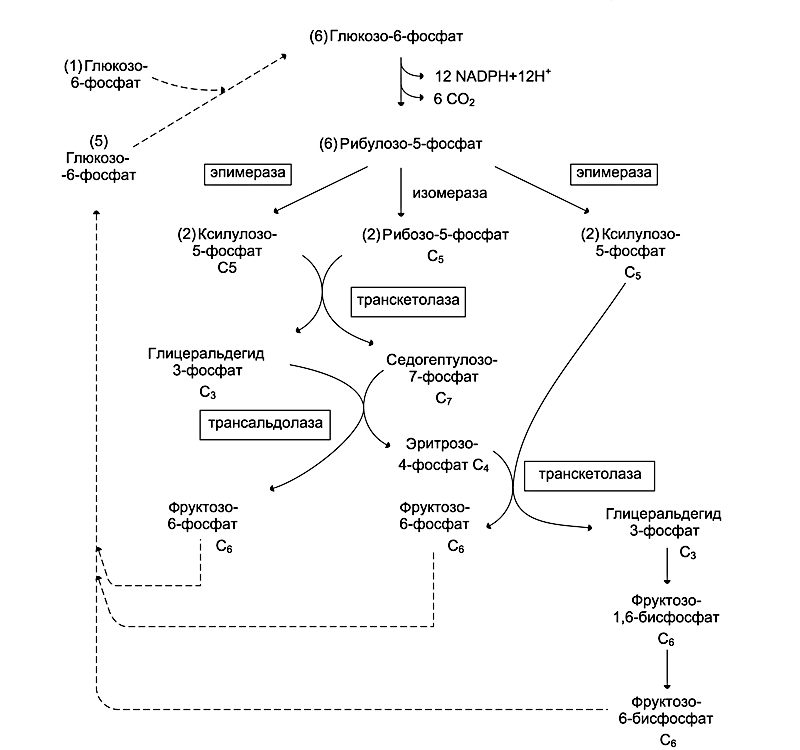
Рисунок 53.Пентозофосфатный способ превращения глюкозы
б) Дефицит глюкозо-6-фосфат-дегидрогеназы (Глк-6Ф-ДГ) может привести к гемолитической анемии. Известно около 400 различных мутаций в гене Глк-6Ф-ДГ. Такие заболевания рецессивны и связаны с Х-хромосомой.
Красные кровяные тельца содержат большое количество кислорода и способны спонтанно генерировать активные формы кислорода, которые могут повредить белки и липиды в клетке. В присутствии активных форм кислорода гемоглобин может преципитировать, образую тельца Хайнца, а мембранные липиды подвергаться пероксидации, в результате чего мембрана клетки разрушается и происходит гемолиз. По мере образования пероксидов они быстро разрушаются системой глутатионпероксидаза/глутатионредуктаза в эритроцитах, предотвращая разрушительные последствия. NADPH, который требуется для глутатион-редуктазы, образуется в пентозофосфатном пути превращения глюкозы в эритроците.
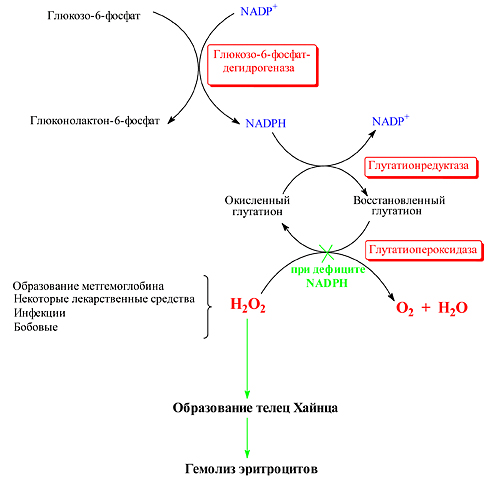
Рисунок 54. Пути, приводящие к гемолитической анемии
Задача 3. У детей, перенесших сердечно-легочную реанимацию, при контроле системы гемостаза отмечали угнетение Хагеман-зависимого фибринолиза.
К каким последствиям приведет нарушение Хагеман-зависимого фибринолиза?
Для ответа:
а) опишите механизмы активации фактора ХII;
б) объясните значение фактора ХII в свертывании крови и фибринолизе.
Ответ.
а) Фактор ХII участвует в контактном пути свертывания крови. Он последовательно активируется двумя способами: сначала в результате изменения конформации при взаимодействии с отрицательно заряженной поверхностью поврежденного эндотелия, затем частичным протеолизом мембранным комплексом калликреин-ВМК.
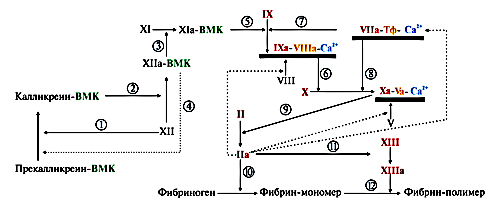
Рисунок 55. Путь свёртывания крови
б) Активированный фактор ХII инициирует образование мембранных ферментных комплексов контактной фазы свертывания. Фактор XIIa вызывает ряд последовательных реакций, в которые вовлекаются присутствующие в плазме крови факторы от XI-го по V-й включительно. В итоге образуется кровяной тромбопластин, или протромбиназа.
Фактор ХIIа участвует в фибринолизе. Он активирует превращение неактивного плазминогена в активный плазмин.
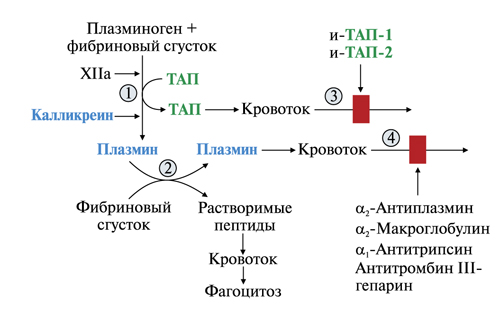
Рисунок 56.Участие фактора ХIIа в фибринолизе
Таким образом, фактор ХII участвует и свертывании крови, и в фибринолизе. При недостатке фактора ХII свертывание крови не нарушается, т.к. его обеспечивает внешний путь свертывания крови, где фактор ХII не участвует, а контактный путь не требуется для инициации свертывания. Фактор ХII имеет важное значение в фибринолизе для превращения плазминогена в плазмин. Его недостаток сопровождается тромбозами, эмболией.
Задача 4. Широкое распространение среди гормональных контрацептивов приобрел препарат «Диане-35», в состав которого входит синтетический аналог эстрогена – этинилэстрадиол. Данное вещество, помимо основного механизма действия, индуцирует синтез протромбина, Х-го фактора свертывания крови, а также понижает тонус стенок сосудов. Длительное применение препарата способно вызвать у женщин тромбоз маточных артерий.
Почему развивается эта патология?
Для ответа:
а) напишите схему прокоагулянтного пути свертывания крови;
б) объясните роль протромбина и Х-го фактора;
в) назовите этапы образования фибринового тромба.
ОТВЕТ:
а)
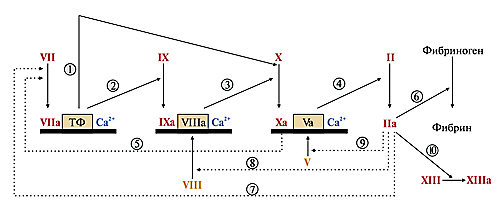
Рисунок 58. Прокоагулянтный путь свертывания крови
б) Протромбин синтезируется в печени, его молекула содержит остатки γ-карбоксиглутаминовой кислоты. Он фиксируется на мембранном ферментном комплексе Ха-Vа-Са2+. Фактор Ха, активированный этинилэстрадиолом, гидролизует пептидные связи в молекуле протромбина. В результате образуется тромбин, который частичным протеолизом превращает фибриноген в фибрин, активирует факторы VII, VIII, V по принципу положительной обратной связи, а также фактор XIII.
в) В процессе формирования фибринового тромба выделяют следующие этапы:
• превращение фибриногена в мономер фибрина в результате отщепления тромбином А- и В-фибринопептидов;
• образование нерастворимого геля фибрина. В результате изменения конформации в доменах фибрина-мономера открываются комплементарные участки – центры связывания. Из-за чего возникают нековалентные связи между молекулами фибрина и его дальнейшие полимеризации;
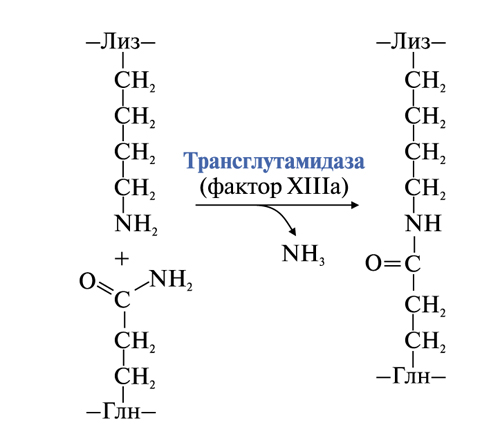
Рисунок 59. Образование амидной связи между молекулами фибрина
• стабилизация геля фибрина. Фермент трансглутаминаза (фактор XIIIа) катализирует образование амидных связей между радикалами глутамина и лизина мономеров фибрина, а также между фибрином и фибринонектином.
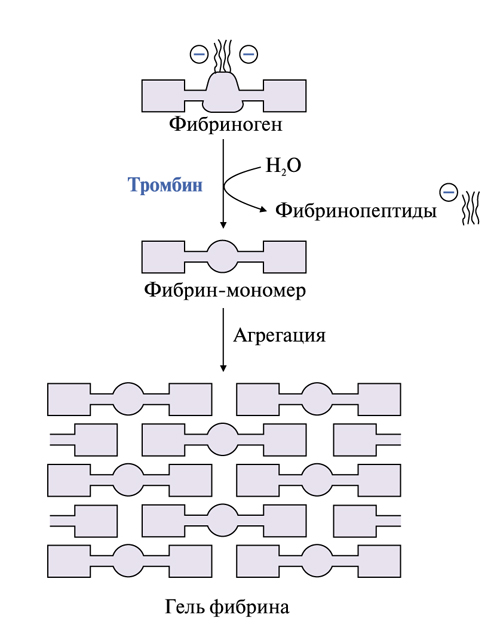
Рисунок 60. Образование геля фибрина
• ретракция фибринового сгустка. Сжатие геля обеспечивает актомиозин тромбоцитов – сократительный белок тромбостенин, обладающий АТФ-азной активностью. Тромбостенин участвует в активации и агрегации тромбоцитов. Ретракция кровяного сгустка предупреждает полную закупорку сосудов, создавая возможность для восстановления кровотока.
Таким образом, на фоне длительного применения препарата «Диане-35» возможно развитие тромбоза маточных артерий вследствие активации II, X факторов прокоагулянтного пути свертывания крови.
Задача 5. К концу XIX в. у гемофилии сложилась «приличная королевская родословная». Этой болезнью страдали итальянские князья, французские короли, а затем через английскую королеву Викторию и ее детей – испанские инфанты и, наконец, наследник российского престола цесаревич Алексей.
Охарактеризуйте это заболевание.
Для ответа:
а) назовите причину разных видов гемофилий;
б) укажите роль недостающих факторов в прокоагулянтном и контактном путях свертывающей системы крови, объяснив механизм образования тромбина;
в) изложите, какие способы лечения этого заболевания вам известны.
ОТВЕТ:
а) Гемофилия – наследственная болезнь снижения свертываемости крови, передаваемая по рецессивному, сцепленному с Х-хромосомой типу, проявляющаяся повышенной кровоточивостью. Болеют мальчики (гемофилия С встречается и у девочек). Выделяют 3 формы гемофилии — А, В и С.
Гемофилия А – наследственное заболевание, вызванное дефицитом фактора VIII свертывания крови (антигемофильный глобулин А). Наследуется по рецессивному, сцепленному с полом типу.
Гемофилия С – наследственное заболевание, обусловленное дефицитом фактора XI свертывания крови (предшественник плазменного тромбопластина). Наследуется по аутосомно-рецессивному либо аутосомно-доминантному типу.
Гемофилия В – наследственное заболевание, связанное с дефицитом фактора IX свертывания крови (плазменный компонент тромбопластина). Наследуется по рецессивному, сцепленному с полом типу.
б) В механизме образования тромба есть 3 функционально разных этапа: внешний (прокоагулянтный), внутренний (контактный) пути свертывания и антикоагулянтная фаза, препятствующая распространению тромба.
Инициация образования сгустка в ответ на повреждение ткани осуществляется по внешнему пути свертывания, а формирования красного тромба в области замедленного кровотока или на аномальной сосудистой стенке при отсутствии повреждения ткани – по внутреннему. На этапе активации фактора X объединяются оба пути и образуется конечный путь свертывания крови.
На каждом из путей последовательно образующиеся ферменты активируют соответствующие проферменты, из-за чего растворимый белок плазмы фибриногена превращается в нерастворимый белок фибрин, который и образует сгусток. Это превращение катализирует протеолитический фермент тромбин путем частичного протеолиза. Он образуется из своего предшественника протромбина при кровопотере. Эта реакцию катализирует протеолитический фермент – фактор Ха в составе мембранного комплекса Ха-Vа-Са2 + .
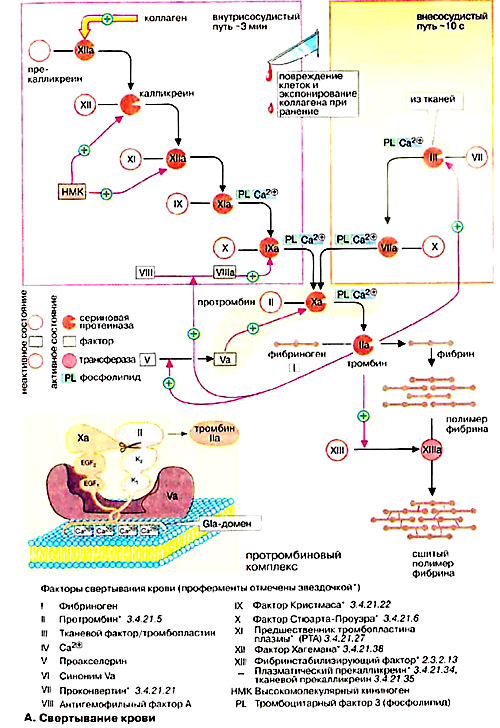
Рисунок 61. Свертывание крови
Все ферменты мембранных комплексов свертывающей системы служат протеазами и активируются частичным протеолизом. Активированный в результате контакта с субэндотелием фактор Х превращает прекалликреин в калликреин; калликреин мембранного комплекса калликреин-HMK активирует фактор ХII; фактор ХIIа активирует фактор ХI; активированный частичным протеолизом фактор ХIIа превращает прекалликреин в калликреин по принципу положительной обратной связи; фактор ХIа мембранного комплекса ХIа-HMB активирует фактор IХ; фактор IХа мембранного комплекса IХа-VIIа-Са2+ активирует фактор Х; фактор VIIа мембранного комплекса VIIа-Тф- Са2+ активирует факторы IХ и Х; фактор Ха протромбиназного комплекса активирует фактор II; тромбин(факторII) превращает фибриноген в фибрин и активирует фактор ХIII; фактор ХIIIа катализирует образование амидных связей в геле фибрина.
в) Основной метод лечения гемофилии заключается в заместительной терапии препаратами, приготовленными из донорской плазмы, которые содержат дефицитные факторы свертывания крови. Используют переливание крови: при гемофилии А переливают свежую кровь, т.к. при хранении в консервированной крови быстро инактивируется фактор VIII, при гемофилии В можно переливать обычную донорскую кровь – она содержит достаточное количество тромбопластина. Применяются методы генной инженерии, с помощью которой синтезируется фактор VIII. Это позволяет избежать осложнений переливания крови.
Задача 6. Ген фактора V находится в 1-й хромосоме рядом с геном антитромбина. Точечная мутация в гене фактора V (лейденовская мутация) ведет к замене аминокислоты аргинина на глутамин в позиции 506. Именно эта точка – место действия активного протеина С (Са) на фактор V.
К каким последствиям может привести данная мутация?
Для ответа:
а) укажите роль факторов Vа и фактор VIIIа в свертывании крови;
б) назовите схему путей свертывания крови;
в) объясните значение протеина С в гемостазе.
ОТВЕТ:
а) Фактор V и фактор VIII – доменные белки, циркулирующие в крови. Фактор V синтезируется в печени, а фактор VIII – эндотелиальными клетками. Оба фактора активируются частичным протеолизом под действием тромбина (фактор IIа). Факторы Va и VIIIa служат белками-активаторами факторов VIIa и Xa. При связывании с белками-активаторами в результате конформационных изменений активность этих ферментов повышается.
б) Существует 2 пути свертывания крови – прокоагулянтный (внешний) и контактный (внутренний). Для инициации реакций внешнего пути необходимо появление тканевого фактора (фактор III) на внешней поверхности плазматической мембраны клеток, соприкасающихся с кровью. Внутренний путь начинается с активации фактора XII при его контакте с поврежденной поверхностью эндотелия сосудов и взаимной активации ферментов прекалликреина и фактора XII.
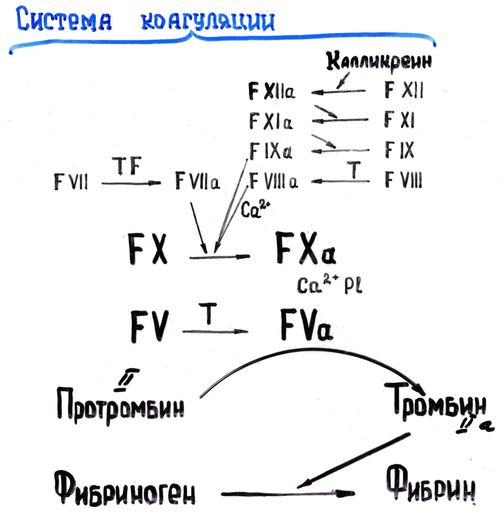
Рисунок 62. Система коагуляции
В прокоагулянтном и контактном путях свертывания крови последовательное образование мембранных ферментных комплексов активируется фактора Х и образуются протромбиназы. Этапы, одинаковые для обоих путей свертывания крови, называются общим путем свертывания крови.
в) Протеин С участвует в процессе антикоагуляции. Тромбин в мембранном комплексе с тромбомодулином и кальцием активирует частичным протеолизом протеин С. Активированный протеин С (Са) образует с белком-активатором S мембраносвязанный комплекс Са-S-Са2+. Протеин Са в составе этого комплекса гидролизует в факторах Va и VIIIa по 2 пептидные связи и инактивирует эти факторы.
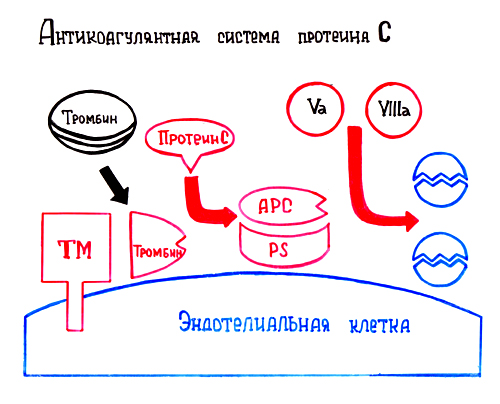
Рисунок 63. Антикоагулянтная система протеина С
ТМ – тромбомодулин
АРС – активированный протеин С
PS – протеин S
Антикоагулянтная фаза тормозит каскад реакций свертывания крови. Мутация фактора V (лейденовская мутация, резистентность к протеину С) приводит к синтезу фактора V, резистентного к протеину С. Больные с такой генетической мутацией страдают тромбофилией.
 2015-03-08
2015-03-08 5672
5672
