Цель работы: 1. Измерить ЭДС Cu-Zn гальванического элемента и электродные потенциалы отдельных электродов, сравнить ЭДС Cu-Zn элемента с вычисленной по значениям измеренных электродных потенциалов и по уравнению Нернста. 2. Измерить ЭДС концентрационного элемента и сравнить ее с вычисленной по уравнению Нернста.
I. Измерение ЭДС Cu-Zn гальванического элемента потенциометром.
1. Составить для работы медно-цинковый гальванический элемент. С этой целью налить в сосуды с медным и цинковым электродами растворы CuSO4 и ZnSO4 , соответственно. Стеклянный соединительный мостик заполнить насыщенным раствором KCl, избегая появления пузырьков. В соединительную пробирку налить насыщенный раствор КСl.
2. Подключить медно-цинковый элемент к потенциометр:медный электрод подключит к клемме «+» потенциометра, цинковый к «-»
3. Измерить ЭДС Cu-Zn элемента с помощью потенциометра. Результаты измерений записать в таблицу 4.1.
3. Вычислить ЭДС Cu-Zn элемента по формуле (4.20) и результат вычислений записать в таблицу 4.1.
Таблица 4.1 Определение ЭДС Cu-Zn элемента.
E0Cu2+/ Cu = …………………….. E0Zn2+/ Zn=................ E0г.э. =.........................
| CuSO4 | ZnSO4 | Еизм (В) | Евыч (В) | ||||
| Смоль/л | γ +- | а | С моль/л | γ+ - | а | ||
| 0,1 | 0,1 | ||||||
| 0,1 | 1,0 | ||||||
| 1,0 | 0,1 |
II. Определение потенциалов Zn- и Си - электродов.
1. Определить электродный потенциал Zn -электрода. Для этого составить гальванический элемент из цинкового и хлорсеребряного электродов и с помощью потенциометра измерить его ЭДС. Записать в тетради электродные реакции, протекающие в этом элементе.
Zn │ ZnSO4 ││Klнасыщ │ AgCl │ Ag
Величину потенциала Zn -электрода рассчитать по формуле (4.21). Значение потенциала хлорсеребряного электрода ЕАg найти по формуле (4.18).
Eг.э. =EAg – EZn и EZn = EAg - Eг.э. (4.21)
2. Определить потенциал Cu -электрода, составив гальванический элемент из медного и хлорсеребряного электродов и измерив его ЭДС. Записать в тетради электродные реакции, протекающие в этом элементе.
Ag │ AgCl │ Klнасыщ ││ CuSO4 │ Cu
3. Рассчитать электродный потенциал Cu -электрода, учитывая, что Cu -электрод является положительным:
Eг.э. =EСu – EAg и ECu = Eг.э. + EAg
4. Вычислить по формуле Нернста (4.15) электродные потенциалы Zn- и Си- электродов. Значения стандартных потенциалов и коэффициентов активности взять из справочных таблиц. Результаты вычислений записать в таблицу 4. 2.
Таблица 4.2 Определение электродных потенциалов Zn- и Сu- электродов.
t0C………… EAg………………………………
| электрод | MeS04 | Ег.э (В) | Е г.э(изм) | Е в | ||
| С | γ + - | а | ||||
| Zn2+/Zn | 0,1 | |||||
| 1,0 | ||||||
| Cu2+/Cu | 0,1 | |||||
| 1,0 |
III. Измерение ЭДС концентрационного элемента.
1. Подготовить для работы один из двух указанных ниже концентрационных гальванических элементов
(-)Zn│ZnSO4││ZnSO4│Zn(+) или
С1 С2
(-)Cu │CuSO4│CuSO4│Cu(+)
С1 С2
с концентрациями солей С1= 0,1 моль/л и С2 = 1,0 моль/л, подключить элемент к потенциометру и измерить его ЭДС.
2.Рассчитать ЭДС концентрационного элемента по формуле:
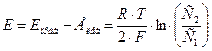 для комнатной температуры
для комнатной температуры
Результаты записать в таблицу 4.3
Таблица 4.3
| элемент | MeSO4 | Ег.э.выч | Ег.эизм | ||||||
| C1 | γ+- | a1 | C2 | γ+- | a2 | ||||
| Сu | |||||||||
| Zn |
Контрольные вопросы
Перед выполнением работы:
1. Какова цель данной работы?
2. Как производится измерение ЭДС медно-цинкового и концентрационного гальванических элементов?
3. Как измерить потенциалы Си- и Zn - электродов?
4. Какие электроды используются в данной работе?
5. Запишите схемы гальванических элементов, используемых в работе.
6. Как вычислить ЭДС медно-цинкового гальванического элемента по уравнению Нернста?
7. Как вычислить потенциалы Си- и Zn - электродов?
К защите работы:
1. Поясните термины: электрод, электродная реакция, гальванический элемент, ЭДС, электродный потенциал, стандартный электродный потенциал.
2. Если в гальваническом элементе протекает самопроизвольный процесс, а) на каком электроде происходит окисление; б) какой из электродов считается отрицательным; в) каков знак ЭДС.; г) каков знак изменения энергии Гиббса данной реакции?
3. Запишите электродные реакции для используемых в работе гальванических элементов.
4. Как по величине электродных потенциалов рассчитать ЭДС элемента определить направление реакции, протекающей в этом элементе?
5. Какие электроды используют в качестве электродов сравнения?
6. Какой элемент называется концентрационным?
 2015-03-20
2015-03-20 1930
1930
