СИЛЫ
Возникновение разности потенциалов на границе металл-раствор.
При контакте металлической пластины с водой катионы, расположенные на поверхности металла, взаимодействуют с диполями воды (рис.4.1 а). Выделяющаяся при этом энергия гидратации идет на разрыв связи катионов с кристаллической решеткой металла, и часть ионов переходит в раствор. В результате этого процесса поверхность металла заряжается отрицательно, а раствор около пластинки - положительно. Образующийся при этом двойной электрический слой (ДЭС), схематически показанный на рис.4.1б, приводит к возникновению разности потенциалов на границе раздела двух фаз металл-раствор. Система, состоящая из металла, погруженного в раствор соли, содержащей катионы этого металла, называют электродом.
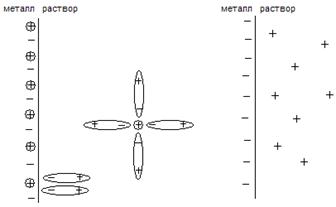
Рис 4.1 а) взаимодействие катионов металла с диполями воды и б) образование двойного электрического слоя на границе металл-вода.
С ростом заряда поверхности скорость перехода ионов в раствор (VМ→р-р) уменьшается и увеличивается скорость обратного процесса (V р-р →Ме) до тех пор, пока не установится состояние динамического равновесия, при котором VМ→р-р = V р-р →М .
При погружении металла(проводник Ιрода) в раствор его соли(проводникΙΙ рода), заряд металла будет зависеть от начального соотношения скоростей перехода катионов в раствор и обратно, что определяется химической природой металла.
Mn+ + ne = M (4.1)
(раствор) (электрод)
Если в начальный момент времени VМ→р >V р →М, металл окисляется и заряжается отрицательно, в случае VМе→р < Vр →М, (металл восстанавливается) поверхность металла приобретает положительный заряд. Так при погружении цинка в раствор его соли металл заряжается отрицательно, в то время как контакт меди с раствором соответствующей соли сопровождается образованием положительного заряда на металле. Направление самопроизвольного перехода ионов определяется убылью энергии Гиббса в этих процессах (∆G<0).
Двойной электрический слой на границе металл-раствор может возникать не только за счёт перехода ионов металла в раствор, но также за счет поверхностных химических реакций, сопровождающихся переходом заряженных частиц с поверхности металла в раствор и обратно. Так, например, водород, адсорбируясь на поверхности платины (инертного металла), диссоциирует на ионы по реакции
2Hp-р+ + 2е= 1/2Н2 (4.2)
Образующийся ион Н+ переходит в раствор, при этом платина заряжается отрицательно. Если концентрация Н+ в растворе велика, возможен обратный процесс, и Pt заряжается положительно. Такой электрод называется водородным. Изменение давления водорода и концентрации ионов Нр+ приводит к смещению равновесия реакции (4.2) и изменению заряда электрода.
Водородный электрод при давлении водорода равном 1 атм и активности ионов водорода равной 1 называют стандартным водородным электродом и используют для определения величины скачка потенциала на границе металл-раствор, абсолютное значение которого измерить невозможно. Потенциал стандартного водородного электрода ∆φ0 H+/ H2 условно принят за нуль.
В лабораториях часто используют электроды, состоящие из металла, покрытого слоем его труднорастворимой соли, погруженного в раствор хорошо растворимой соли с тем же анионом. К таким электродам относится, например, хлорсеребряный электрод, представляющий собой серебряную проволоку, покрытую слоем AgCI и погруженную в раствор KCI.  Электродный потенциал такого электрода возникает за счет реакции
Электродный потенциал такого электрода возникает за счет реакции
AgCl=Ag+ + Cl -
Ag+ + e=Ag0
Суммарная реакция AgClтв+ e=Ag0+ Cl- (4.3),
Если инертный металл (например, Pt) погрузить в раствор, содержащий окисленную и восстановленную форму одного вещества (например, раствор FeCl2 и FeCl3), то такой электрод называют окислительно-восстановительным или редокс-электродом.
Потенциал, который возникает в данной окислительно-восстановительной системе, называется окислительно-восстановительным или редокс-потенциалом. Редокс-потенциал возникает в результате того, что на поверхности Pt протекает окислительно-восстановительная реакция, например:
Fe3+ + е = Fe2+ (4.4),
Платина в электродных реакциях не участвует, а является лишь переносчиком электронов для протекающей на ее поверхности реакций и в зависимости от направления процесса является акцептором или донором электронов. В рассмотренном выше примере при избытке окисленной формы в растворе CFe3+> CFe2+ поверхность Pt заряжается положительно. В случае CFe3+< CFe2+ поверхность Pt заряжается отрицательно.
Во всех рассмотренных выше примерах (реакции (4.1) - (4.4)) скачок потенциала на границе электрод-раствор возникает вследствие окислительно-восстановительных реакций, протекающих на поверхности металла. Если окисленную форму вещества обозначить ох, а восстановленную red, то в общем виде электродную реакцию можно записать в виде:
ох + ne = red
Величина скачка потенциала определяется температурой, природой окислительно-восстановительной системы и соотношением активностей окисленной и восстановленной форм:
∆φ=∆φ0 + 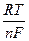 ln(aox/ ared) (4.5),
ln(aox/ ared) (4.5),
где ∆φ0 - скачок потенциала при аox = ared = 1, R - газовая постоянная, F -число Фарадея. Эту формулу называют уравнением Нернста.
Химическая энергия, выделяющаяся в результате реакций окисления и восстановления, протекающих на электродах, может быть превращена в электрическую в гальваническом элементе, который составляют из двух электродов или полуэлементов. Условием работы подобного источника тока является пространственное разделение процессов окисления и восстановления. В качестве примера такого устройства на рис.4.2 показан медно-цинковый элемент Даниэля-Якоби.
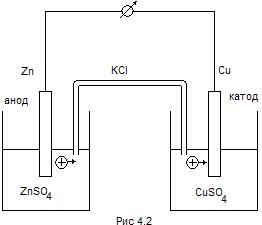
На цинковом электроде протекает реакция окисления и цинк заряжается отрицательно:
1. Znтв -2 е-→Zn2+р-р ∆G= - 146 кДж/моль (4.6)
На медном – реакция восстановления, поверхность меди заряжается положительно:
2. Cu2+p-р + 2e-→ Cuтв ∆G= - 66 кДж/моль (4.7)
Суммарная реакция, протекающая в элементе,
Znтв + Cu2+p = Zn2+p + Cuтв ∆G= - 212 кДж/моль (4.8)
Эту же реакцию можно провести внеся кусочек цинка в раствор CuSO4, однако тока в этом случае не получим.
Медно-цинковый элемент схематически можно записать следующим образом
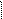
 (-)Cu │ Zn │ZnSO4р-р КСl CuSO4p │ Сu(+)
(-)Cu │ Zn │ZnSO4р-р КСl CuSO4p │ Сu(+)
или Cu │ Zn │ZnSO4 ││ CuSO4 │ Сu (4.9)
Отрицательный электрод, на котором протекает реакция окисления (анод) принято записывать слева. Сплошной вертикальной чертой (│) обозначают границу раздела фаз, на которой возникает скачок потенциалов,границы между электролитами обычно обозначают пунктирной вертикальной чертой.
Электродвижущую силу (ЭДС), которая численно равна максимальной работе по перемещению заряда рассчитывают как
E=ECu2+|Cu- EZn2+|Zn+φk+φD, (4.10)
где φk- скачок потенциала на границе контакта двух металлических проводников(этот потенциал в данной цепи равен нулю); φD- скачок потенциала на границе раздела проводников второго рода:р-р ZnSO4|р-р KCl| р-р CuSO4.На этих границах раздела возникают двойные электрические слои. Однако подвижности ионов K- и Cl- близки, поэтому эти скачки потенциала пренебрежительно малы. Практически ЭДС гальванического элемента равна:
E=ECu2+|Cu- EZn2+|Zn (4.11)
Величина ЭДС связана с изменением изобарного потенциала для реакции, протекающей в гальваническом элементе, по уравнению:
∆G = -EnF (4.12)
где n - число электронов, участвующих в реакции; F - число Фарадея (96485 Кл/моль).
Так как экспериментально невозможно измерить разность потенциалов между двумя точками, находящимися в разных фазах, например между металлом и раствором его соли, для определения потенциала исследуемого электрода составляют гальванический элемент из исследуемого электрода и стандартного водородного электрода, при этом последний всегда стоит слева. Например:
M│Pt │ H2 │ H+││Mn+│M
Электродвижущая сила такого элемента называется э лектроднымпотенциалом. Электродный потенциал обозначают как ЕMen+/Me всегда к электродной реакции восстановления.
Mn+ + пе- = М°
EMn+/M =∆φ0H 2/H+ + ∆φM n+/M =∆φMn+ /M (4.13)
Подставляя в (4.13) уравнение (4.5) получим зависимость электродного потенциала от природы металла, активности его ионов и температуры
E = E 0 + 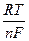 ln(aox/ ared) = E 0 +
ln(aox/ ared) = E 0 + 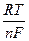 ln(aMn+/ aM0) (4.14)
ln(aMn+/ aM0) (4.14)
где E0Mn+/M -стандартный электродный потенциал.
Для металлического электрода aM 0 = const и
E = E 0 + 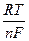 ln aMn+ (4.15)
ln aMn+ (4.15)
Для окислительно-восстановительных электродов величина электродного потенциала определяется соотношением окисленной и восстановленной форм и уравнение Нернста записывается в виде:
E = E 0 + 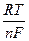 ln(aox/ ared) (4.16)
ln(aox/ ared) (4.16)
Стандартный электродный потенциал Е° считается положительным, если электрод заряжен более положительно, чем стандартный водородный электрод и отрицательным в противоположном случае.
В случае медного электрода на нем идет реакция восстановления и знак электродного потенциала будет положительным.
Cu2+ + 2e→ Cu0 E0Cu2+/ Cu = 0, 34 B
Если на электроде протекает реакция окисления, как на цинковом электроде, то знак электродного потенциала противоположный. Например,
Zn2+ + 2e = Zn0 E0Zn2+/ Zn= - 0,76 B
Значения стандартных электродных потенциалов (E0Mn+/M ) приведены в справочнике.
Величина стандартного электродного потенциала характеризует стремление электродной реакции протекать в направлении восстановления иона. Чем больше значение потенциала, тем больше способность окисленной формы вещества присоединить электроны и перейти в восстановленную, тем более сильным окислителем она является, и наоборот. Для сравнения:
E0Mg2+/ Mg = - 2, 37 B, E0F-/F 2 /Pt = 2,87 B.
На практике для измерения электродного потенциала обычно используют электроды сравнения, более простые в употреблении, чем водородный. В качестве электродов сравнения используют такие электроды, потенциал которых известен, точно воспроизводим и остается постоянным во время измерений.
К таким электродам относится хлорсеребряный электрод, описанный выше (см. уравнения (4.3)). Потенциал этого электрода определяется активностью ионов хлора
∆ E = ∆ E 0 - 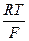 ln aCl - (4.17)
ln aCl - (4.17)
Значения электродного потенциала хлорсеребряного электрода приведены в справочнике.
В нашем практикуме используется хлорсеребряный электрод с насыщенным раствором КСl. Потенциал такого электрода зависит только от температуры и его величина, выраженная в вольтах, рассчитывается по формуле:
E = 0, 2224 – 0, 00065(t – 25). (4.18)
Зная величины стандартных электродных потенциалов можно рассчитать ЭДС любого гальванического элемента. При этом удобно пользоваться следующими правилами:
1. Реакция, протекающая у левого электрода, записывается как реакция окисления, а реакция у правого электрода - как реакция восстановления. Суммарная реакция в гальваническом элементе представляет собой сумму обеих реакций.
2. Стандартная ЭДС элемента равна стандартному электродному потенциалу правого электрода минус стандартный электродный потенциал левого электрода
E0 = E0 прав – Е0 лев (4.19)
Для Сu-Zn гальванического элемента ЭДС можно вычислить следующим образом:
E= ECu – EZn = E 0Cu – E0 Zn + 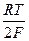 ln aCu2+-
ln aCu2+- 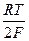 ln aZn2+=
ln aZn2+=
=E0 - 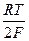 ln (aZn2+/aCu2+) (4.20)
ln (aZn2+/aCu2+) (4.20)
 2015-03-20
2015-03-20 1675
1675
