Механика имеет дело с отдельными телами (обычно описывает движение не более трех тел). Молекулярная физика изучает системы, состоящие из огромного числа N ~(NA =6,02×1023 моль-1) непрерывно хаотически движущихся частиц.
Исследовать процессы в таких системах с помощью законов механики практически невозможно. Однако молекулярная физика и термодинамика выработали свои особые методы изучения таких систем. Существует два общих подхода (метода):
- статистический – основывается на квантовой теории строения вещества и использует новые – статистические – закономерности, проявляющиеся только в коллективном поведении частиц системы; оперирует характеристиками отдельных частиц (скорость, энергия), используя их усреднение (наиболее вероятные значения) для описания всей системы;
- термодинамический (ТД) – изучает общие свойства макросистем (не вдаваясь в строение, происходящее внутри), находящихся в состоянии термодинамического равновесия; устанавливает соотношения между макропараметрами: обычно Р (давлением), V (объемом) и T (температурой) системы на основе обобщения большого числа опытных данных. Поэтому термодинамику часто называют феноменологической (от греч. «являющееся») теорией.
|
|
|
Оба подхода тесно связаны и хорошо дополняют, а в ряде случаев дублируют друг друга.
Дадим ряд определений.
Термодинамической системой (ТДС) называют мысленно выделенную совокупность тел (макросистему), которая рассматривается на основе ТД подхода. Открытая ТДС – ТДС, обменивающаяся с окружающей средой веществом и энергией, закрытая – только энергией. Напротив, изолированная ТДС (или з амкнутая ТДС) – ТДС, не способная к обмену веществом и энергией с окружающей средой (идеальный случай, т.к. энергия может излучаться и поглощаться без соприкосновения изолированных тел, для замкнутой имеется ввиду неспособность обмениваться энергией через совершение механической работы). Адиабатная ТДС – замкнутая ТДС, не способная к обмену энергией с окружающей средой посредством теплообмена (реальные теплоизолированные системы с малым рассеянием теплоты).
ТД параметры делятся: на интенсивные, не зависящие от количества вещества в ТДС (P, T), и экстенсивные, зависящие и пропорциональные ему (V); на внешние, зависящие от положения и свойств внешних по отношению к ТДС тел (например, стенок сосуда – V), и внутренние, зависящие еще и от координат и скоростей частиц самой системы (Р, энергия).
В 1866г. австрийский физик Л.Больцман (1844–1906), будучи студентом, доказал, что величиной, характеризующей состояние ТДС независимо от ее микроскопической структуры, может быть средняя кинетическая энергия поступательного движения одной молекулы:
|
|
|
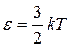 , (9.1)
, (9.1)
где k – постоянная Больцмана, k =1,38×10-23 Дж/К; Т – термодинамическая температура (по шкале Кельвина (англ. У. Томсон (1824–1907), за научные заслуги лорд Кельвин)) – мера кинетической энергии (теплового движения) частиц вещества. В настоящее время в международной практике, наряду с термодинамической шкалой, принято использовать международную практическую шкалу Цельсия (швед. A. Celsius (1701–1744)) Т =[ t (°C)+273,15°]К. Считается, что при T=0 K – «нуль кельвин» – прекращается всякое движение. Такая температура не достижим а, хотя возможно сколь угодно близкое приближение к ней.
ТД равновесием называется состояние системы, характеризующееся при постоянных внешних условиях неизменностью параметров (P, V, T) и отсутствием потоков вещества и энергии в системе.
Равновесное состояние системы характеризуется следующими свойствами:
1) оно не зависит от предыстории системы (от предшествующих состояний);
2) переход системы в равновесное состояние необратим;
3) в равновесном состоянии реализуется определенное стационарное (не зависящее от времени) распределение молекул по скоростям.
ТД процессом называется любое изменение состояния системы, связанное с изменением хотя бы одного термодинамического параметра. ТД процесс называется равновесным, если изменение состояния ТДС происходит при t ®¥ (время), т.е. каждое предыдущее состояние характеризуется мало отличающимися от последующего ТД параметрами (P, V, T). Реальные процессы имеют конечную скорость (время) протекания и не являются равновесными, но могут быть приближенными к ним – квазиравновесными.
Модель идеального газа (ИГ) основывается на трех допущениях:
– собственный объем молекул пренебрежимо мал по сравнению с объемом сосуда;
– силы взаимодействия между молекулами отсутствуют;
– столкновение молекул друг с другом и со стенками сосуда в процессе хаотического теплового движения носит упругий характер.
Модель ИГ с успехом применяется для описания реальных газов при нормальных условиях (н.у.): P0 =101325 Па=760 мм.рт.ст., Т0 =273,15 К, а также при высоких температурах и низких давлениях. При иных условиях от уравнения ИГ можно перейти к теории реальных газов, вводя в эти уравнения поправки, учитывающие собственный объем молекул и силы взаимодействия между ними.
Простейшие примеры ТД процессов – изопроцессы (постоянной остается масса газа m =const и один из ТД параметров P, V или T). Они описываются экспериментально установленными законами:
а) изотермический (m =const, T =const) (рис.9.1, а) закон Бойля–Мариотта (англ. Р. Бойль (1627–1691), фр. Э. Мариотт (1620–1684)):
PV = const; (9.2)
б) изобарный (m =const, P =const) (рис. 9.1, б) закон Ж.Л. Гей-Люссака (1778–1850):
V=V0 (1+ a×t). (9.3)
При н.у. (Р0 и Т0) a =1/273,15 K-1;
в) изохорный (m =const, V =const) (рис. 9.1, в) закон Ж.Л. Гей-Люссака (1778–1850):
P=P0 (1+ a×t). (9.4)
Выражая время t через температуру T законы Гей-Люссака можно переписать в виде:
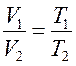 и
и 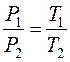 . (9.5)
. (9.5)
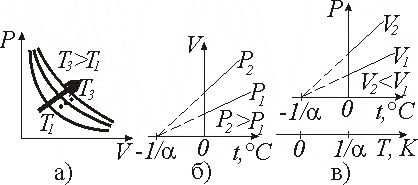
Рис. 9.1
Закон А. Авогадро (1776–1856): 1 моль любых газов при одинаковых температуре и давлении занимают одинаковый объем.
При н.у. молярный объем Vm =22,41×10-3 м3 (22,41 литра), а число частиц в одном моле любого газа NA =6,02×1023 моль-1.
Закон Дж. Дальтона (1766–1844): давление смеси газов равно сумме парциальных давлений газов, входящих в эту смесь: 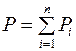 .
.
Парциальное давление – то, которое производил бы газ, входящий в состав смеси, если бы занимал сам весь объем, занимаемый смесью.
 2015-05-05
2015-05-05 1252
1252








