Лабораторная работа № 19
Цель работы – определить массу меди (II) в пробе, г.
Сущность работы. Определение меди (II) основано на взаимодействии ионов Cu2+ с иодид-ионами и последующем титровании выделившегося иода стандартным раствором тиосульфата натрия:
2Cu2+ + 4I– = I2 + 2CuI↓;
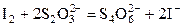 .
.
Значение стандартного потенциала пары I2/2I– (0,54 В) заметно превышает соответствующее значение пары Cu2+/Cu+ (0,16 В), поэтому окисление иодида ионами меди (II) представляется нереальным. Однако на самом деле реакция между Cu2+ и I– протекает количественно. Это обусловлено образованием малорастворимого осадка CuI, что существенно повышает потенциал пары Cu2+/Cu+. Реакцию следует проводить в кислой среде для подавления гидролиза ионов меди (II).
Лабораторная посуда: мерная колба; бюретка, пипетка Мора, мерные цилиндры (100 мл, 10-20 мл), конические колбы.
Реактивы: стандартный раствор Na2S2O3 (C =), 5%-ный раствор KI, 2 н. раствор H2SO4, раствор крахмала.
Выполнение работы. Получают у лаборантов анализируемый раствор в мерную колбу
(_________ мл), доводят объем водой до метки и перемешивают. Переносят пипеткой аликвотную часть (10,0 мл) этого раствора в коническую колбу, добавляют ~3 мл 2 н. раствора H2SO4 и
~10 – 15 мл раствора KI. Накрыв колбу часовым стеклом, оставляют смесь в темноте на 5 мин для завершения реакции.
Промывают и заполняют бюретку раствором Na2S2O3 и устанавливают уровень жидкости на нуле.
Извлекают колбы с реакционной смесью из темного места. Снимают часовое стекло и ополаскивают его над колбой дистиллированной водой.
Выделившийся I2 оттитровывают тиосульфатом. Когда окраска раствора станет бледно-желтой, добавляют раствор крахмала до появления темно-синего окрашивания и продолжают титрование до исчезновения окраски (записывают только конечный объем титранта).
Титрование повторяют не менее 3 раз.
V1 = V2 = V3 = Vср =
По полученным результатам рассчитывают массу Cu2+ в анализируемом растворе, г.
С(Cu2+) = 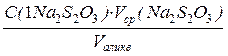 =
=
m(Cu) = C(Cu2+) · Vколбы· M(Cu) · fэкв =
d =
Ответ:
Работу выполнил(а):
| Студент(ка) | |
| Фак-т, курс, № гр. |
 2015-05-14
2015-05-14 513
513






