1. Изохорический процесс. Если нагревание вещества происходит при постоянном объеме, то согласно (6) система не совершает работы над окружающими телами, а все полученное количество теплоты расходуется на изменение ее внутренней энергии. Из (7) следует, что
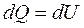 .
.
Получим выражение для молярной теплоемкости одного моля идеального газа при V = const:
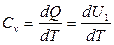 . (12)
. (12)
Подставим (2) в (12):

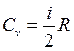 . (13)
. (13)
Тогда внутреннюю энергию моля идеального газа можно вместо (2) записать в виде:
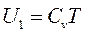 . (14)
. (14)
2. Изобарический процесс. Запишем первое начало термодинамики (7) для одного моля идеального газа:
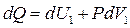 . (15)
. (15)
При 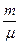 =1 моль - уравнение Менделеева - Клапейрона
=1 моль - уравнение Менделеева - Клапейрона
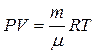 (16)
(16)
приводится к виду:
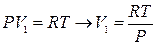 . (17)
. (17)
При подстановке (14) и (17) в (15) молярная теплоемкость при постоянном давлении может быть записана в виде:
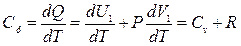 ,
,
т.е. 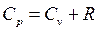 . (18)
. (18)
Выражение (18) называется уравнением Майера. Из сопоставления (18) и (15) следует физический смысл универсальной газовой постоянной. Она численно равна работе, совершаемой молем идеального газа при повышении его температуры на один Кельвин в изобарическом процессе (Р = const). Ср всегда больше Сv на R, так как при нагревании газа при постоянном давлении требуется дополнительное количество теплоты на совершение работы расширения газа, чтобы обеспечить постоянство давления увеличением объема газа.
Выразим Ср через число степеней свободы i, подставив (13) в (18):
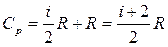 . (19)
. (19)
Согласно молекулярно-кинетической теории газов теплоемкость зависит от числа степеней свободы молекул и не должна зависеть от температуры. Но это оказывается справедливым только в пределах отдельных температурных интервалов.
Участки монотонного возрастания теплоемкости наблюдаются при изменении числа степеней свободы молекул. При низких температурах молекулы двигаются поступательно. С ростом температуры включаются степени свободы вращательного движения. При еще более высоких температурах к ним добавляются колебательные степени свободы. Поэтому при нормальных условиях следует учитывать только поступательные и вращательные степени свободы.
Как видно из монотонного характера графика во вращательное, а затем и колебательное движение молекулы вовлекаются постепенно. Объяснение такого поведения теплоемкости дает квантовая механика.
 Сv
Сv




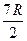





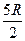



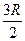
0 100 200 2000 5000 Т, К
 |
Рисунок 2- Температурная зависимость молярной теплоемкости водорода при постоянном объеме.
 2015-05-14
2015-05-14 2946
2946
