Электрохимия
В таблице приведены значения стандартных электродных потенциалов (Е0) при температуре 250С и нормальном атмосферном давлении 101,3 кПа. Все величины выражены по отношению к потенциалу стандартного водородного электрода.
Если условия отличаются от стандартных (250С, 101,3 кПа, концентрации окисленной и восстановленной формы равны 1), то электродный потенциал рассчитывают по уравнению Нернста:

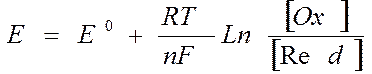 , где:
, где:
Е- электродный потенциал при заданных условиях;
Е0-стандартный электродный потенциал(из справочника);
R-универсальная газовая постоянная(3,14);
Т- заданная температура
[Ox]-концентрация окисленной формы вещества;
[Red]-концентрация восстановленной формы вещества
| Элемент | Электродный процесс | Е0, В |
| Азот | 3N2+2e=2N3- 3N2+2H++2e=2HN3 N2+4H2O+2e=2NH2OH+2OH- N2+2H2O+4H++2e=(2NH2OH)H+ N2+4H2O+4e=N2H4+4OH- N2+8H2O+6e=NH4OH+6OH- N2+5H++4e=(N2H4)H+ N2+6H++6e=2NH3 N2+8H++6e=2NH4+ | -3,400 -3,100 -3,040 -1,870 -1,160 -0,740 -0,230 +0,057 +0,260 |
| N3-+7H2O+6e=N2H4+NH3+7OH- HN3+11H++8e=3NH4+ | -0,620 +0,690 | |
| Элемент | Электродный процесс | Е0, В |
| Азот | N2H4+4H2O+2e=2NH4OH+2OH- (N2H4)H++3H++2e=NH4+ | +0,100 +1,270 |
| NH2OH+2H2O+2e=NH4OH+2OH- (NH2OH)H++2H++2e=NH4++H2O H2N2O2+6H++4e=(2NH2OH)H+ | +0,420 +1,350 +0,500 | |
| H2N2O2+2H++2e=N2+2H2O NO2-+H2O+e=NO+2OH- | +2,650 -0,460 | |
| NO2-+6H2O+6e=NH4OH+7OH- 2NO2-+4H2O+6e=N2+8OH- 2HNO2+4H++4e=H2N2O2+2H2O HNO2+7H++6e=NH4++2H2O HNO2+H++e=NO+H2O 2HNO2+4H++4e=N2O+3H2O 2HNO2+6H++6e=N2+4H2O | -0,150 +0,410 +0,830 +0,860 +0,990 +1,290 +1,440 | |
| N2O+H2O+2e=N2+2OH- N2O+2H++2e=N2+H2O | +0,940 +1,770 | |
| 2NO+2H2O+4e=N2+4OH- 2NO+4H++4e=N2+2H2O | +0,850 +1,680 | |
| N2O4(2NO2)+4H2O+8e=N2+8OH- N2O4(2NO2)+2e=2NO2- N2O4(2NO2)+2H++2e=2HNO2 N2O4(2NO2)+8H++8e=N2+4H2O | +0,530 +0,880 +1,070 +1,350 | |
| NO3-+H2O+e=NO2+2OH- NO3-+2H2O+3e=NO+4OH- | -0,860 -0,140 | |
| NO3-+7H2O+8e=NH4OH+9OH- NO3-+H2O+2e=NO2-+2OH- NO3-+8H++6e=(NH2OH)H++2H2O NO3-+2H++e=NO2+H2O 2NO3-+17H++14e=(N2H4)H++6H2O NO3-+10H++8e=NH4++3H2O NO3-+3H++2e=HNO2+H2O NO3-+4H++3e=NO+2H2O 2NO3-+12H++10e=N2+6H2O | -0,120 +0,010 +0,730 +0.800 +0,840 +0,870 +0,940 +0,960 +1,240 | |
| Элемент | Электродный процесс | Е0, В |
| Актиний | Ac3++3e=Ac | -2,600 |
| Алюминий | A1O2-+2H2O+3e=A1+4OH- [A1(OH)4]-+3e=A1+4OH- A1(OH)3+3e=A1+3OH- A1F63-+3e=A1+6F- A13++3е=A1 A1(OH)3(т)+3H++3e=A1+3H2O | -2,350 -2,336 -2,310 -2,070 -1,660 -1,538 |
| Барий | Ba2++2e=Ba | -2,900 |
| Бериллий | Be2O32-+3H2O+4e=2Be+6OH- Be2++2e=Be | -2,620 -1,850 |
| Бор | H2BO3-+H2O+3e=B+4OH- BF4-+3e=B+4F- H3BO3+3H2O+4e=B+3H2O | -1,790 -1,040 -0,870 |
| Бром | Br3-+2e=3Br- Br2 + 2e =2 Br− Br2 (р-р) + 2e = 2 Br− | +1,050 +1,066 +1,087 |
| 2BrO2-+2H2O+2e=Br2+4OH- BrO-+H2O+2e=Br-+2OH- HBrO + H2O + 2e = Br− + 2OH− HBrO +H+ + 2e = Br− + H2O 2HBrO +H+ + 2e =Br2 (р-р) + H2O | +0,450 +0,760 +0,761 +1,331 +1,574 | |
| 2BrO3− + 6H2O + 10е = Br2 + 12OH− BrO3-+2H2O+4e=BrO-+4OH- BrO3− + 3H2O + 6е = Br− + 6OH− BrO3− +6H+ + 6е =Br− + 3H2O BrO3-+5Н++4е=HBrO+2H2O 2BrO3− +6H+ + 5е =Br2 + 3H2O | +0,500 +0,540 +0,610 +1,440 +1,450 +1,520 | |
| Ванадий | V2++2e=V | -1,175 |
| V3++3e=V2+ | -0,255 | |
| VO2++e=VO+ VO+ + 2H+ + е =V3+ + H2O VO2++4H++5e=V+2H2O VO2++4H++3e=V2++2H2O VO2++4H++2e=V3++2H2O V2O5+6H++2e=2VO2++3H2O VO2++2H++e=VO2++3H2O | -0,044 +0,337 -0,250 +0,360 +0,668 +0,958 +1,004 | |
| Элемент | Электродный процесс | Е0, В |
| Ванадий | VO43-+6H++2e=VO++3H2O H2VO4-+4H++e=VO2++3H2O Bi+3H++3e=BiH3 | +1,256 +1,314 <-0,800 |
| Висмут | Bi2O3+3H2O+6e=2Bi+6OH- BiOC1+2H++3e=Bi+H2O+C1- BiC14-+3e=Bi+3C1- | -0,460 +0,160 +0,160 |
| Bi2O4+H2O+2e=Bi2O3+2OH- Bi2O4+4H++2e=2BiO++2H2O NaBiO3+4H++2e=BiO++Na++2H2O | +0,560 +1,590 >+1,800 | |
| Водород | H2+2e=2H- | -2,250 |
| 2H2O+2e=H2+2OH- 2H+(10-7M)+2e=H2 2H++2e=H2 HO2-+H2O+2e=3OH- H2O2+2H++2e=2H2O | -0,828 -0,414 0,000 +0,880 +1,770 | |
| Вольфрам | WO2(ТВ) + 4H+ + 4е= W(ТВ) + 2H2O | -0,120 |
| W2O5(ТВ) +2H++2е= 2WO2(ТВ) + H2O W(CN)83- + е = W(CN)84 - | -0,031 +0,457 | |
| WO42-+4H2O+6e=W+8OH- 2WO3.(ТВ)+6H+ + 6e =W(ТВ) + 3H2O 2WO3.(ТВ)+2H+ + 2e = W205 (ТВ)+H2O WO42-+8H++6e=W+4H2O WO42- + 4H+ + e= W02(ТВ) + 2H2O 2WO42- + 6H+ + 2e= W205(ТВ) + 3H2O | -1,050 -0,090 -0,029 +0,049 +0,386 +0,801 | |
| Гадолиний | Gd3++3e=Gd | -2,397 |
| Галлий | H2GaO3-+H2O+3e=Ga+4OH-Ga3++3e=Ga | -1,220 -0,530 |
| Гафний | HfO(OH)2+H2O+4e=Hf+4OH- Hf+4+4e=Hf HfO2+4H++4e=Hf+2H2O | -2,500 -1,700 -1,570 |
| Германий | Ge+4H++4e=GeH4 | <-0,300 |
| GeO+2H++2e=Ge+H2O Ge2++2e=Ge | -0,200 0,000 | |
| HGeO3-+2H2O+4e=Ge+5OH- GeO2+4H++4e=Ge+2H2O | -1,000 -0,150 | |
| Элемент | Электродный процесс | Е0, В |
| Германий | H2GeO3+4H++4e=Ge+3H2O GeO2+2H++2e=GeO(коричневый)+H2O | -0,130 -0,120 |
| Гольмий | Ho3++3e=Ho | -2,319 |
| Диспрозий | Dy3++3e=Dy | -2,353 |
| Европий | Eu2++2e=Eu Eu3++e=Eu2+ | |
| Железо | FeS+2e=Fe+S2- Fe(OH)2+2e=Fe+2OH- FeCO3+2e=Fe+CO32- Fe2++2e=Fe Fe(OH)2+2H++2e=Fe+2H2O | -0,950 -0,877 -0,756 -0,440 -0,047 |
| Fe(OH)3+e=Fe(OH)2+OH- Fe2O3+H2O+2H++2e=2Fe(OH)2 Fe2O3+6H++6e=2Fe+3H2O Fe3++3e=Fe Fe(OH)3+3H++3e=Fe+3H2O Fe(OH)3+H++e=Fe(OH)2+H2O Fe(CN)63-+3e=Fe(CN)64- Fe3++e=Fe2+ Fe(C12H8N2)33++e= Fe(C12H8N2)32+ | -0,560 -0,057 -0,051 -0,037 +0,059 +0,271 +0,356 +0,770 +1,060 | |
| Fe3O4+8H++8e=3Fe+4H2O Fe3O4+8H++2e=3Fe3++4H2O FeO42-+8H++3e=Fe3++4H2O | -0,085 +0,980 +1,700 | |
| Золото | Au(CN)2-+e=Au+2CN- Au(CNS)2-+e=Au+2CNS- AuBr2-+e=Au+2Br- AuC12-+e=Au+2C1- Au++e=Au | -0,610 +0,690 +0,960 +1,110 +1,680 |
| Au(CNS)4-+2e=Au(CNS)2-+2CNS- AuBr4-+2e=AuBr2-+2Br- AuC14-+2e=AuC12-+2C1- | +0,640 +0,870 +0,930 | |
| Au(CNS)4-+3e=Au+4CNS- H2AuO3-+H2O+3e=Au+4OH- AuBr4-+3e=Au+4Br- AuC14-+3e=Au+4C1- | +0,660 +0,700 +0,820 +0,990 | |
| Элемент | Электродный процесс | Е0, В |
| Золото | Au3++2e=Au+ Au3++3e=Au | +1,410 +1,500 |
| Йод | I2+2e=2I- I2+2e=2I- | +0,536 +0,621 |
| I3-+2e=3I- | +0,545 | |
| ICN+2e=I-+CN- 2IO-+H2O+2e=I2+4OH- 2ICN+2H++2e=I2+2HCN 2IBr2-+2e=I2 +4Br- IO-+H2O+2e=I-+2OH- HIO+H++2e=I-+H2O 2IBr+2e=I2+2Br- 2IC12-+2e=J2+4C1- 2IC1+2e=I2+2C1- 2HIO+H++2e=I2+2H2O | +0,300 +0,450 +0,630 +0,870 +0,890 +0,990 +1,020 +1,060 +1,190 +1,450 | |
| 2IC13+6e=I2+6C1- IO3-+2H2O+4e=IO-+4OH- 2IO3-+6H2O+10e=I2+12OH- JO3-+3H2O+6e=I-+6OH- IO3-+6H++6e=I-+3H2O IO3-+5H++4e=HIO+2H2O 2IO3-+12H++10e=I2+6H2O | +1,280 +0,140 +0,210 +0,260 +1,080 +1,140 +1,190 | |
| H3IO62-+3H2O+8e=I-+9OH- H2IO62-+2e=JO3-+3OH- | +0,370 +0,700 | |
| H5IO6+7H++8e=I-+6H2O H5IO6+H++2e=IO3-+3H2O | +1,240 +1,600 | |
| Иридий | Ir2O3+3H2O+6e=2Ir+6OH- IrC163-+3e=Ir+6C1- Ir+3+3e=Ir | +0,100 +0,770 +1,150 |
| IrO2+2H2O+4e=Ir+4OH- IrC162-+4e=Ir+6C1- IrO2+4H++4e=Ir+H2O IrC162-+e=IrC163 | +0,100 +0,830 +0,930 +1,020 | |
| Иттербий | Yb3++e=Yb2+ | -1,205 |
| Иттрий | Y3++3e=Y | -2,327 |
| Элемент | Электродный процесс | Е0, В |
| Кадмий | CdS+2e=Cd+S2- Cd(CN)42-+2e=Cd+4CN- Cd(OH)2+2e=Cd+2OH- | -1,175 -1,090 -0,810 |
| CdCO3+2e=Cd+CO32- Cd(NH3)42++2e=Cd+4NH3 Cd2++2e=Cd | -0,740 -0,610 -0,403 | |
| Cd(OH)2+2H++2e=Cd+2H2O CdO+2H++2e=Cd+H2O | 0,005 0,063 | |
| Калий | K++e=K | -2,925 |
| Кальций | Ca(OH)2+2e=Ca+2OH- Ca2++2e=Ca | -3,030 -2,866 |
| Кислород | O2+H2O+2e=HO2-+OH- O2+2H2O+4e=4OH- O2+2H++2e=H2O2 O2+4H+(10-7M)+4e=2H2O O2+4H++4e=2H2O | -0,076 +0,401 +0,682 +0,815 +1,229 |
| O3+H2O+2e=O2+2OH- O3+6H++6e=3H2O | +1,240 +1,511 | |
| HO2-+H2O+2e=3OH- H2O2+2H+=3OH- | +0,880 +1,770 | |
| Кобальт | СоS(β)+2e=Co+S2- CoS(α)+2e=Co+S2- Co(OH)2+2e=Co+2OH- CoCO3+2e=Co+CO32- Co(NH3)62++2e=Co+6NH3 | -1,070 -0,900 -0,730 -0,640 -0,420 |
| Co2++2e=Co Co(OH)2+2H++2e=Co+2H2O CoO+2H++2e=Co +H2O | -0,277 +0,095 +0,170 | |
| Co(NH3)63++e=Co(NH3)62+ Co(OH)3+e=Co(OH)2+OH- Co3++e=Co Co3++e=Co2+ | +0,100 +0,170 +0,330 +1,808 | |
| Кремний | Si+4H2O+4e=SiH4+4OH- Si++4H++4e=SiH4 | -0,730 +0,100 |
| SiO32-+3H2O+4e=Si+6OH- | -1,700 | |
| Элемент | Электродный процесс | Е0, В |
| Кремний | SiF62-+4e=Si+6F- SiO2(кварц)+4H++4e=Si+2H2O H2SiO3(водн)+4H++4e=Si+3H2O SiO32-+6H++4e=Si+3H2O | -1,200 -0,857 -0,789 -0,455 |
| Лантан | La(OH)3+3e=La+3OH- La3++3e=La | -2,900 -2,520 |
| Литий | Li++e=Li | -3,030 |
| Магний | Mg(OH)2+2e=Mg+2OH- Mg2++2e=Mg Mg(OH)2+2H++2e=Mg+2H2O | -2,690 -2,363 -1,862 |
| Марганец | MnCO3+2e=Mn+CO32- Mn2++2e=Mn Mn(OH)2+2e=Mn+2OH- Mn(OH)2+2H++2e=Mn+2H2O | -1,480 -1,190 -1,180 -0,727 |
| Mn(CN)63-+3e=Mn+6CN- Mn(OH)3+e=Mn(OH)2+OH- Mn2O3+6H++2e=2Mn2++3H2O Mn3++e=Mn2+ | -0,244 +0,100 +1,443 +1,510 | |
| MnO2+4H++2e=Mn2++2H2O | +1,230 | |
| MnO42-+2H2O+2e=MnO2+4OH- MnO42-+4H++2e=MnO2+2H2O | +0,600 +2,260 | |
| MnO4-+e=MnO42- MnO4-+2H2O+3e=MnO2+4OH- MnO4-+8H++5e=Mn2++4H2O MnO4-+4H++3e=MnO2+2H2O | +0,560 +0,600 +1,510 +1,690 | |
| Медь | Cu2S+2e=2Cu+S2- Cu(CN)2-+e=Cu+2CN- Cu2O+H2O+2e=2Cu+2OH- CuCNS+e=Cu+CNS- CuI+e=Cu+I- Cu(NH3)2++e=Cu+2NH3 CuI22-+e=Cu+2I- CuBr+e=Cu+Br- CuC1+e=Cu +C1- Cu++e=Cu | -0,890 -0,430 -0,360 -0,270 -0,185 -0,120 +0,030 +0,137 +0,520 |
| Элемент | Электродный процесс | Е0, В |
| Медь | CuS+2e=Cu+S2- Cu(OH)2+2e=Cu+2OH- 2Cu(OH)2+2e=Cu2O+2OH-+H2O Cu(NH3)42++2e=Cu+4NH3 Cu(NH3)42++e=Cu(NH3)2++2NH3 Cu2++e=Cu+ 2Cu2++H2O+2e=Cu2O+2H+ Cu2++2e=Cu Cu2++C1-+e=CuC1 CuO+2H++2e=Cu+H2O Cu2++Br-+e=CuBr 2CuO+2H++2e=Cu2O+H2O Cu2++I-+e=CuI | -0,710 -0,220 -0,080 -0,070 -0,010 +0,153 +0,203 +0,340 +0,538 +0,609 +0,640 +0,669 +0,860 |
| Молибден | Mo+3+3e=Mo | -0,200 |
| MoO2+4H++4e=Mo+2H2O | -0,072 | |
| MoO2++4H++2e=Mo3++2H2O Mo(CN)83-+e=Mo(CN)84- | 0,000 +0,730 | |
| H2MoO4+2H++2e=MoO2+2H2O MoO42-+4H2O+6e=Mo+8OH- H2MoO4+6H++6e=Mo+4H2O MoO42-+8H++6e=Mo+4H2O MoO3+2H++2e=MoO2+H2O MoO22++e=MoO2+ MoO42-+4H++2e=MoO2+2H2O | -1,091 -1,050 0,000 +0,154 +0,320 +0,480 +0,606 | |
| Натрий | Na++e=Na | -2,714 |
| Неодим | Nd3++3e=Nd | -2,431 |
| Нептуний | Np3++3e=Np | -1,856 |
| Np4++e=Np3+ | +0,152 | |
| NpO2++4H++2e=Np3++2H2O | +0,451 | |
| Никель | NiSγ+2e=Ni+S2- NiSα+2e=Ni+S2- Ni(OH)2+2e=Ni+2OH- Ni(NH3)62++2e=Ni+6NH3 NiCO3+2e=Ni+CO32- Ni(CN)42-+2e=Ni+4CN- Ni2++2e=Ni | -0,990 -0,760 -0,720 -0,490 -0,450 -0,400 -0,230 |
| Элемент | Электродный процесс | Е0, В |
| Никель | Ni(OH)2+2H++2e=Ni+2H2O NiO+2H++2e=Ni+H2O NiO2+2H2O+2e=Ni(OH)2+2OH- NiO2+4H++2e=Ni2++2H2O NiO42-+8H++4e=Ni+4H2O | +0,110 +0,116 +0,490 +1,680 >+1,800 |
| Ниобий | NbO+2H++2e=Nb+H2O Nb3++3e=Nb | -0,733 -1,100 |
| NbO2+2H++2e=NbO+H2O | -0,625 | |
| Nb2O5+10H++10e=Nb+5H2O NsO(SO4)2-+2H++5e=Nb+H2O+2SO42- NbO3++2H++2e=Nb3++H2O Nb2O5+2H++2e=2NbO2+H2O NbO(SO4)2-+2H++2e=Nb3++H2O+2SO42- | -0,650 -0,630 -0,340 -0,289 -0,100 | |
| Олово | SnS+2e=Sn+S2- HSnO2-+H2O+2e=Sn+3OH- Sn2++2e=Sn SnO+2H++2e=Sn+H2O Sn(OH)2+2H++2e=Sn+H2O | -0,940 -0,910 -0,136 -0,104 -0,091 |
| Sn(OH)62-+2e=HSnO2-+3OH-+H2O SnF62-+4e=Sn+6F- SnO2+2H++2e=SnO+H2O SnO2+4H++4e=Sn+2H2O Sn4++4e=Sn Sn4++2e=Sn2+ | -0,930 -0,250 -0,108 -0,106 +0,010 +0,151 | |
| Осмий | Os2++2e=Os | +0,850 |
| OsC162-+3e=OsC163- | +0,850 | |
| Осмий | OsC163-+e=Os2++6C1- OsC163-+3e=Os+6C1- | +0,400 +0,710 |
| HOsO5-+4H2O+8e=Os+9OH- OsO4+8H++8e=Os+4H2O OsO4+6C1-+8H++4e=OsC162-+4H2O | +0,020 +0,850 +1,000 | |
| Палладий | Pd(OH)2+2e=Pd+2OH- PdC142-+2e=Pd+4C1- PdO+2H++2e=Pd+H2O Pd2++2e=Pd PdI62-+2e=PdI42-+2I- | +0,070 +0,623 +0,896 +0,987 +0,623 |
| Элемент | Электродный процесс | Е0, В |
| Палладий | Pd(OH)4+2e=Pd(OH)2+2OH- PdC162-+4e=Pd+6C1- PdBr62-+2e=PdBr42-+2Br- PdO2+2H++2e=PdO+H2O PdC162-+2e=PdC142-+2C1- | +0,730 +0,960 +0,993 +1,283 +1,290 |
| Платина | PtS+2e=Pt+S2- Pt(OH)2+2e=Pt+2OH- PtBr42-+2e=Pt+4Br- PtC142-+2e=Pt+4C1- Pt(OH)2+2H++2e=Pt+H2O Pt2++2e=Pt | -0,950 +0,150 +0,580 +0,730 +0,980 +1,188 |
| PtS2+2e=PtS+S2- PtI62-+2e=PtI42-+2I- PtBr62-+2e=PtBr42-+2Br- PtC162-+2e=PtC142-+2C1- PtO2+2H++2e=PtO+H2O | -0,640 +0,393 +0,590 +0,720 +1,045 | |
| Плутоний | Pu(OH)3+3e=Pu+3OH- Pu3++3e=Pu Pu2O3+6H++6e=2Pu+3H2O | -2,420 -2,031 -1,592 |
| Pu(OH)4+3=Pu(OH)3+OH- 2PuO2+2H++2e=Pu2O3+H2O Pu4++e=Pu3+ Pu(OH)4+4H++e=Pu3++4H2O | -0,950 -0,455 +0,967 +1,182 | |
| PuO22++e=PuO2+ PuO22++4H++3e=Pu3++2H2O PuO22++4H++2e=Pu4++2H2O | +0,916 +1,017 +1,040 | |
| Плутоний | Pu22++2e=PuO2 PuO3+H2O+2H++2e=Pu(OH)4 PuO3+2H++2e=PuO2+H2O | +1,092 +1,325 +1,485 |
| Празеодим | Pr3++3e=Pr | -2,462 |
| Прометий | Pm3++3e=Pm | -2,423 |
| Рений | Re+e=Re- | -0,400 |
| Re++2e=Re- | -0,230 | |
| Re3++3e=Re | +0,300 | |
| ReO2+4H++e=Re3++2H2O ReO2+4H++4e=Re+2H2O | +0,157 +0,260 | |
| Элемент | Электродный процесс | Е0, В |
| Рений | ReO3+2H++2e=ReO2+H2O ReO42-+8H++3e=Re3++4H2O | +0,400 +0,795 |
| ReO4-+2H2O+3e=ReO2+4OH- ReO4-+4H2O+7e=Re+8OH- | -0,595 -0,584 | |
| ReO4-+8H++7e=Re+4H2O ReO4-+8H++4e=Re3++4H2O ReO4-+4H++3e=ReO2+2H2O ReO4-+2H++e=ReO3+H2O | +0,370 +0,422 +0,510 +0,770 | |
| Родий | RhC163-+3e=Rh+6C1- Rh3++3e=Rh Rh2O3+6H++6e=2Rh+3H2O | +0,440 +0,800 +0,870 |
| RhO2+4H++6C1-+e=RhC163-+2H2O RhO2++2H++e=Rh3++H2O | +1,400 +1,400 | |
| RhO42-+6H++2e=RhO2++3H2O | +1,460 | |
| Ртуть | Hg2I2+2e=2Hg+2I- Hg2Br2+2e=2Hg+2Br- Hg2C12+2e=2Hg+2C1- Hg2(IO3)2+2e=2Hg+2IO3- Hg2C2O4+2e=2Hg+C2O42- Hg2(CH3COO)2+2e=2Hg+2CH3COO- Hg2SO4+2e=2Hg+SO42- Hg22++2e=2Hg | -0,041 +0,140 +0,268 +0,394 +0,415 +0,510 +0,615 +0,788 |
| HgS(красный)+2e=Hg+S2- HgS(черный)+2e=Hg+S2- Hg(CN)42-+2e=Hg+4CN- HgI42-+2e=Hg+4I- | -0,700 -0,690 -0,370 -0,040 | |
| Ртуть | HgO(красная)+H2O+2e=Hg+2OH- HgBr42-+2e=Hg+4Br- HgC14-+2e=Hg+4C1- Hg2++2e=Hg 2Hg2++2e=Hg22+ HgO+2H++2e=Hg+H2O | +0,098 +0,210 +0,480 +0,850 +0,920 +0,926 |
| Рубидий | Rb++e=Rb | -2,925 |
| Рутений | Ru2++2e=Ru | +0,450 |
| RuC13+3e=Ru+3C1- | +0,680 | |
| RuC15-+2e=Ru2++5C1- | +0,300 | |
| Элемент | Электродный процесс | Е0, В |
| Рутений | RuO2+4H++4e=Ru+2H2O RuC15OH2-+H++e=RuC152-+H2O | +0,790 +1,300 |
| RuO4-+e=RuO42- | +0,600 | |
| RuO4+e=RuO4- | +1,000 | |
| Самарий | Sm3++3e=Sm | -3,121 |
| Свинец | PbS+2e=Pb+S2- PbO+H2O+2e=Pb+2OH- HPbO2-+H2O+2e=Pb+3OH- PbCO3+2e=Pb+CO32- PbI2+2e=Pb+2I- PbSO4+2e=Pb+SO42- PbF2+2e=Pb+2F- PbBr2+2e=Pb+2Br- PbC12+2e=Pb+2C1- Pb2++2e=Pb PbO+2H++2e=Pb+H2O Pb(OH)2+2H++2e=PbO+2OH- | -0,930 -0,580 -0,540 -0,506 -0,365 -0,356 -0,350 -0,280 -0,268 -0,126 +0,248 +0,277 |
| PbO32-+H2O+2e=PbO22-+2OH- PbO2+H2O+2e=PbO+2OH- Pb4++4e=Pb Pb3O4+2H++2e=3PbO+H2O PbO2+4H++2e=Pb2++2H2O PbO2+SO42-+4H++2e=PbSO4+2H2O Pb4++2e=Pb2+ | +0,200 +0,280 +0,840 +0,972 +1,449 +1,685 +1,694 | |
| Селен | Se+2e=Se2- Se+2H++2e=H2Se | -0,920 -0,400 |
| SeO32-+3H2O+4e=Se+6OH- H2SeO3+4H++4e=Se+3H2O | -0,366 +0,741 | |
| SeO42-+H2O+2e=SeO32- SeO42-+4H++2e=H2SeO3+H2O | +0,050 +1,150 | |
| Сера | S+2e=S2- 2S+2e=S22- 5S+2e=S52- S +H++2e=HS- S +2H++2e=H2S | -0,480 -0,476 -0,340 -0,065 +0,170 |
| Элемент | Электродный процесс | Е0, В |
| Сера | S22-+2e=2S2- S4O62-+2e=2S2O32- | -0,524 +0,090 |
| 2SO32-+2H2O+2e=S2O42-+4OH- 2SO32-+3H2O+4e=S2O32-+6OH- 2H2SO3+H++2e=HS2O4-+2H2O SO32-+6H++6e=S2-+3H2O H2SO3+4H++4e=S+3H2O 2SO32-+6H++4e=S2O32-+3H2O | -1,120 -0,580 -0,080 +0,231 +0,449 +0,705 | |
| SO42-+H2O+2e=SO32-+2OH- 2SO42-+5H2O+8e=S2O32-+10OH- SO42-+4H2O+2e=SO32-+2OH- SO42-+4H2O+6e=S+8OH- S2O32-+6H++8e=2S2-+3H2O SO42-+8H++8e=S2-+4H2O SO42-+4H++2e=H2SO3+H2O 2SO42-+10H++8e=S2O32-+5H2O SO42-+10H++8e=H2S+4H2O SO42-+8H++6e=S+4H2O S2O32-+6H++4e=2S+3H2O S2O82-+2e=2SO42- | -0,930 -0,760 -0,750 -0,750 -0,006 +0,149 +0,170 +0,290 +0,311 +0,357 +0,500 +2,010 | |
| Серебро | Ag2S+2e=2Ag+S2- Ag(CN)32-+e=Ag+3CN- Ag(CN)2-+e=Ag+2CN- AgI+e=Ag+I- AgCN+e=Ag+CN- Ag(S2O3)23-+e=Ag+2S2O32- AgBr+e=Ag +Br- AgCNS+e=Ag+CNS- AgC1+e=Ag+C1- AgN3+e=Ag +N3- Ag2O+H2O+2e=2Ag+2OH- AgJO3+e=Ag+IO3- Ag(SO3)22-+e=Ag+2SO32- Ag2CrO4+2e=2Ag+CrO42- Ag2CO3+2e=2Ag+CO32- Ag2C2O4+2e=2Ag+C2O42- | -0,710 -0,510 -0,290 -0,152 -0,040 +0,010 +0,071 +0,090 +0,224 +0,293 +0,344 +0,350 +0,430 +0,447 +0,460 +0,472 |
| Элемент | Электродный процесс | Е0, В |
| Серебро | Ag2MoO4+2e=2Ag+MoO42- Ag2WO4+2e=2Ag+WO42- AgBrO3+e=Ag+BrO3- AgNO2+e=Ag+NO2- Ag2SO4+2e=2Ag+SO42- Ag++e=Ag Ag2O+2H++2e=2Ag+H2O | +0,490 +0,530 +0,550 +0,590 +0,635 +0,799 +1,173 |
| 2AgO+H2O+2e=Ag2O+2OH- 2AgO+2H++2e=Ag2O+H2O Ag2++e=Ag+ | +0,600 +1,398 2,000 | |
| Ag2O3+H2O+2e=2AgO+2OH- AgO++2H++e=Ag2++H2O | +0,740 +2,100 | |
| Скандий | Sc3++3e=Sc | -2,077 |
| Стронций | Sr2++2e=Sr | -2,888 |
| Сурьма | Sb+3H++3e=SbH3 | -0,510 |
| SbO2-+2H2O+3e=Sb+4OH- Sb2O3+6H++6e=2Sb+3H2O SbO++2H++3e=Sb+H2O SbO2-+4H++3e=Sb+2H2O | -0,675 +0,152 +0,212 +0,446 | |
| SbO3-+H2O+2e=SbO2-+2OH- SbO3-+2H++2e=SbO2-+H2O Sb2O5+6H++4e=2SbO++3H2O Sb2O5+4H++4e=Sb2O3+2H2O Sb2O4+4H++2e=2SbO++2H2O | -0,430 +0,353 +0,580 +0,671 +0,680 | |
| Таллий | Tl2S+2e=2Tl+S2- TlI+e=Tl+I- TlBr+e=Tl+Br- TlC1+e=Tl+C1- TlOH+e=Tl+OH- Tl++e=Tl TlOH+H++e=Tl+H2O | -0,930 -0,753 -0,658 -0,557 -0,344 -0,336 +0,778 |
| Tl(OH)3+2e=TlOH+2OH- Tl2O3+3H2O+4e=2Tl++6OH- Tl3++3e=Tl+ | -0,050 +0,020 +1,252 | |
| Тантал | Ta2O5+10H++10e=2Ta+5H2O | -0,750 |
| Элемент | Электродный процесс | Е0, В |
| Теллур | Te+2e=Te2- Te+2H++2e=H2Te | -1,140 -0,720 |
| Теллур | TeO32-+3H2O+4e=Te+6OH- TeO2+4H++4e=Te+2H2O TeO2H++3H++4e=Te+2H2O | -0,570 +0,530 +0,560 |
| TeO42-+H2O+2e=TeO32-+2OH- TeO42-+2H++2e=TeO32-+H2O H6TeO6+2H++2e=TeO2+4H2O | +0,400 +0,892 +1,020 | |
| Тербий | Tb3++3e=Tb | -2,391 |
| Технеций | Tc2++2e=Tc | +0,400 |
| TcO2+4H++2e=Tc2++H2O TcO2+4H++4e=Tc+2H2O | +0,144 +0,272 | |
| TcO3+2H++2e=TcO2+H2O | +0,757 | |
| TcO4-+8H++5e=Tc2++4H2O TcO4-+2H++2e=TcO3+H2O | +0,500 +0,700 | |
| Титан | Ti2++2e=Ti TiO+2H++2e=Ti+H2O | -1,630 -1,306 |
| Ti3++e=Ti2+ | -0,368 | |
| TiF62-+4e=Ti+6F- TiO2++2H++4e=Ti+H2O TiO2+4H++4e=Ti+2H2O TiO2(рутил)+4H++e=Ti3++2H2O TiO2(рутил)+4H++2e=Ti2++2H2O TiO2++2H++2e=Ti2++H2O TiO2++2H++e=Ti3++H2O | -1,190 -0,880 -0,860 -0,666 -0,502 -0,135 +0,100 | |
| Торий | Th(OH)4+4e=Th+4OH- Th4++4e=Th ThO2+4H++4e=Th+2H2O | -2,480 -1,899 -1,789 |
| Тулий | Tm3++3e=Tm | -2,278 |
| Углерод | С(графит)+4H++2e=HCOOH | -0,132 |
| CO+6H++6e=CH4+H2O HCOO-+2H2O+2e=HCHO+3OH- CNO-+H2O+2e=CN-+2OH- 2CO2+2H++2e=H2C2O4 CO2+2H++2e=HCOOH | +0,497 -1,070 -0,970 -0,490 -0,200 | |
| Элемент | Электродный процесс | Е0, В |
| Углерод | CO2+2H++2e=CO+H2O CH3COOH+2H++2e=CH3CHO HCOOH+2H++2e=HCHO+H2O CO2+N2+6H++6e=CO(NH2)2+H2O HCOOH+4H++4e=CH3OH+H2O HCOO-+3H++2e=HCHO+H2O CH3CHO+2H++2e=C2H5OH CO32-+6H++4e=HCHO+2H2O HCOO-+5H++4e=CH3OH+H2O CO32-+8H++6e=CH3OH+2H2O CO32-+3H++2e=HCOO-+H2O HCHO+2H++2e=CH3OH 2HCNO+2H++2e=(CN)2+2H2) (CN)2+2H++2e=2HCN 2CO32-+4H++2e=C2O42-+2H2O C2H5OH+2H++2e=C2H6+H2O CO32-+6H++4e=C(графит)+3H2O CH3OH+2H++2e=CH4+H2O C6H4O2(хинон)+2H++2e=C6H4(OH)2(гидрохинон) | -0,120 -0,120 -0,010 +0,100 +0,145 +0,167 +0,190 +0,197 +0,199 +0,209 +0,227 +0,232 +0,330 +0,370 +0,441 +0,460 +0,475 +0,590 +0,699 |
| Уран | U(OH)3+3e=U+3OH- U3++3e=U U2O3+6H++6e=2U+3H2O | -2,170 -1,798 -1,346 |
| UO2+2H2O+4e=U+4OH- UO2+4H++4e=U+2H2O U4++e=U3+ UO2+4H++e=U3++2H2O | -2,390 -1,444 -0,607 -0,382 | |
| UO2++4H++e=U4++2H2O | +0,55 | |
| UO22++4H++2e=U4++2H2O UO3+H2O+2H++2e=UO2+2H2O UO22++2e=UO2 UO3+2H++2e=UO2+H2O | +0,333 +0,368 +0,450 +0,657 | |
| Фосфор | P+3H2O+3e=PH3+3OH- P+3H++3e=PH3 | -0,890 +0,060 |
| H3PO2-+e=P+2OH- H3PO2+H++e=P+2H2O HPO32-+2H2O+2e=H2PO2-+3OH- | -2,050 -0,510 -1,570 | |
| Элемент | Электродный процесс | Е0, В |
| Фосфор | H3PO3+3H++3e=P(белый)+3H2O H3PO3+2H++2e=H3PO2+H2O H3PO3+3H++3e=P(красный)+3H2O | -0,502 -0,500 -0,454 |
| PO43-+2H2O+2e=HPO32-+3OH- 2H3PO4+2H++2e= H4P2O6+2H2O H3PO4+5H++5e=P(белый)+4H2O H3PO4+4H++4e=H3PO2+2H2O H3PO4+5H++5e=P(красный)+4H2O H3PO4+2H++2e=H3PO3+H2O H4P2O6+2H++2e=2H3PO3 | -1,120 -0,940 -0,411 -0,390 -0,383 -0,276 +0,380 | |
| Фтор | F2O+2H++4e=2F-+H2O | +2,100 |
| F2+2e=2F- | +2,870 | |
| Хлор | С12+2e=2C1- | +1,359 |
| 2ClO-+2H2O+2e=C12+4OH- C1O-+H2O+2e=C1-+2OH- C12O+4H++4e=2HC1+H2O HC1O+H++2e=C1-+H2O 2HC1O+2H++2e=C12+H2O | +0,400 +0,880 +1,351 +1,500 +1,630 | |
| C1O2-+H2O+2e=C1O-+2OH- C1O2-+2H2O+4e=C1-+4OH- HC1O2+3H++4e=C1-+2H2O 2HC1O2+6H++6e=C12+4H2O HC1O2+2H++2e=HC1O+H2O | +0,660 +0,770 +1,560 +1,630 +1,640 | |
| C1O2+2H2O+5e=C1-+4OH- C1O2+H++e=HC1O2 C1O2+5H++5e=HC1+2H2O | +0,850 +1,270 +1,436 | |
| C1O2+4H++5e=C1-+2H2O 2С1O2+8H++8e=C12+4H2O | +1,500 +1,570 | |
| C1O3-+H2O+2e=C1O2-+2OH- C1O3-+3H2O+6e=C1-+6OH- C1O3-+2H++e=C1O2+H2O C1O3-+3H++2e=HC1O2+H2O C1O3-+6H++6e=C1-+3H2O 2C1O3-+12H++10e=C12+6H2O C1O4-+H2O+2e=C1O3-+2OH- C1O4-+4H2O+8e=C1-+8OH- | +0,330 +0,630 +1,150 +1,210 +1,450 +1,470 +0,360 +0,560 | |
| Элемент | Электродный процесс | Е0, В |
| Хлор | C1O4-+2H++2e=C1O3-+H2O C1O4-+8H++8e=C1-+4H2O 2C1O4-+16H++14e=C12+8H2O | +1,190 +1,380 +1,390 |
| Хром | Cr(OH)2+2e=Cr+2OH- Cr2++2e=Cr | -1,400 -0,913 |
| Cr(OH)3+3e=Cr+3OH- CrO2-+2H2O+3e=Cr+4OH- Cr3++3e=Cr Cr(OH)3+3H++3e=Cr+3H2O Cr3++e=Cr2+ CrO2-+4H++3e=Cr+2H2O CrO2-+4H+e=Cr2++2H2O | -1,300 -1,200 -0,744 -0,654 -0,407 -0,213 +1,188 | |
| CrO42-+4H2O+3e=Cr(OH)3+5OH- C2O72-+14H++12e=2Cr+7H2O CrO42-+8H++6e=Cr+4H2O CrO42-+4H++3e=CrO2-+2H2O C2O72-+14H++6e=2Cr3++7H2O CrO42-+8H++3e=Cr3++4H2O | -0,130 +0,294 +0,366 +0,945 +1,333 +1,477 | |
| Цезий | Cs++e=Cs | -2,923 |
| Церий | Ce3++3e=Ce | -2,480 |
| Ce4++e=Ce3+ | +1,610 | |
| Цинк | ZnS(ТB) + 2e = Zn(ТВ) + S2 – Zn(CN)42+ +2e = Zn(ТВ)+4CN- Zn(OH)2(ТВ) + 2e = Zn(ТВ) +2ОH- ZnО22–+ 2H2О + 2e = Zn(ТВ) +4ОH– HZnO2¯+ 3H+ + 2e = Zn(ТВ) + 2H2О | -1,405 —1,260 —1,245 —1,216 —1,216 |
| ZnCO3+2e=Zn+CO32- Zn(NH3)42+ +2e = Zn(ТВ) +4NH3 Zn2+ +2 e= Zn(ТВ) ZnО22- + 4H+ +2e = Zn(ТВ) +2H2О | -1,060 -1,040 —0,763 +0,441 | |
| ZrO2 . 2Н2О(ТВ)+ 4H+ + 4e = Zr(ТВ) +4H2O ZrO2 . Н2О(ТВ)+ 4H+ + 4e = Zr(ТВ) +3H2O | —1,553 —1,533 | |
| Элемент | Электродный процесс | Е0, В |
| Цирконий | H2ZrO3+H2O+4e=Zr+4OH- ZrO2++2H++4e=Zr+H2O ZrO2+4H++4e=Zr+2H2O Zr4++4e=Zr ZrO2+4H++4e=Zr+2H2O | -2,360 -1,570 -1,553 -1,539 -1,430 |
| Эрбий | Er3++3e=Er | -2,296 |
 2015-05-10
2015-05-10 494
494