Химическая кинетика или кинетика химических реакций - раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Для понимания механизма взаимодействия исходныхкомпонентов эксперементальные данные следует проанализировать по уравнениям формальной кинетики, исходя из того, что лимитирующей стадией взаимодействия является:
- химическое взаимодейсвие ZnO и MoO3:
(1 – G)-2/3 – 1 = k1 * τ, (1)
- диффузия реагентов через слой ZnMoO4, разделяющий исходные реагенты:
(1 – (1 – G)-1/3)2 = k2 * τ, (2)
1 – 2/3 * G – (1- G)2/3 = k3 * τ, (3)
Скорость химической реакции твердофазного взаимодействия двух веществ может быть выражена уравнением:
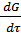 = k * C1m * C2n * S, (4)
= k * C1m * C2n * S, (4)
где: С1 и С2 – концентрации реагирующих веществ на поверхности контакта;
m и n – коэфициенты химической реакции;
S – площадь контакта.
При изменении площади контакта и m = n соотношение (4) превращается в следующее:
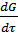 = k1 * (1 – G)5/3, (5)
= k1 * (1 – G)5/3, (5)
Интегрируя последнее при начальных условиях G = 0, t = 0 получаем уравнение:
(1 – G)-2/3 – 1 = k`τ (6)
Для различных моментов времени определяют значение функции и строят график временной зависимости рассматриваемых функций.
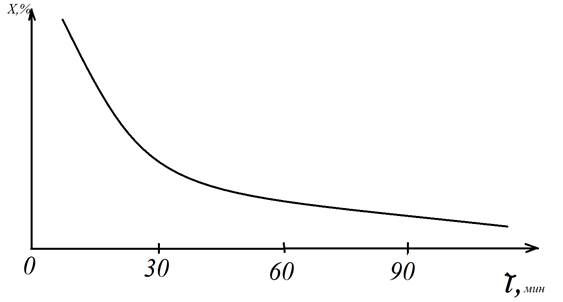
Рис. 5.1 Зависимость количества свободного оксида цинка в смеси ZnO – MoO3
Наиболее приемлемым считается уравнение, которое дает прямолинейную зависимость. Как правило, одно уравнение справедливо при более низких температурах, другие – при более высоких. в случае получения линейной зависимости находят константу скорости по тангенсу угла наклона прямой к оси абсцисс и далее из соотношения (7) аналитически определяют знергию активации процесса:
Lg 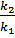 =
= 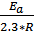 * (
* (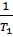 -
- 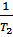 ) (7)
) (7)
Графически Еа (в кДж/моль) определяют по тангенсу угла наклона прямой линии, выражающей зависимость Lgk от 1/T.
 2015-05-10
2015-05-10 189
189






