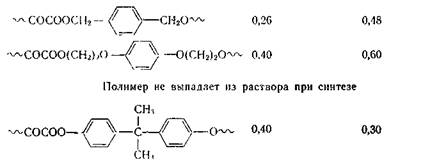
ПОЛИКОНДЕНСАЦИЯ В РАСТВОРЕ
Поликонденсация в растворе широко применяется как в лабораторной, так и в промышленной практике для получения полимеров различных классов. По использованию в промышленности этот способ уступает лишь поликонденсации в расплаве.
Особенно интенсивное развитие поликонденсации в растворе наблюдается в последние годы в связи с потребностью в получении высокомолекулярных термостойких полимеров, которые невозможно синтезировать поликонденсацией в расплаве из-за их высоких температур плавления.
Это привело к созданию новых вариантов поликонденсации в расплаве с применением совершенно новых растворителей, использованием быстропротекающих реакций, проведением поликонденсации в термодинамически невыгодных средах и т. д.
Иногда трудно провести грань между поликонденсацией в растворе и расплаве, поскольку в последнем случае (особенно на ранних стадиях) процесс можно рассматривать как поликонденсацию в растворе обоих или одного из мономеров (олигомеров). Поэтому в данной книге поликонденсацией в растворе называется способ поликонденсации, при котором в системе помимо исходных мономеров присутствует еще один компонент (растворитель).
Назначение растворителя
Ранее было показано, что основным фактором, обусловливающим высокую молекулярную массу образующегося полимера, является большая глубина превращения реакционных центров. Поэтому растворитель, используемый при поликонденсации, должен создавать такие условия, которые обеспечивали бы протекание реакции между реакционными центрами на большую глубину d.
Для различных систем это достигается разными путями, и поэтому назначение растворителя в рассматриваемом способе поликонденсации многообразно.
Растворение исходных мономеров.
Мономеры, как правило, должны дозироваться в реакционную систему в виде растворов. При дозировании в твердом виде их следует растворять в применяемом растворителе. Реакционная способность мономеров в твердом виде гораздо ниже, чем в растворенном.
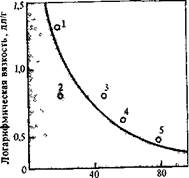
В качестве примера на рис. 5.1 приведены данные о поликонденсации дигидрохлорида п-фенилендиамина и дихлорангидрида терефталевой кислоты в амидном растворителе. Кривая / соответствует мономеру, находящемуся в осадке (нерастворившемуся) после добавления его в эквимольном количестве к другому реагенту. Из рис. 5.1 видно, что логарифмическая вязкость полимера (а значит, и молекулярная масса) изменяется антибатно количеству мономера в осадке, т. е. симбатно количеству мономера, находящемуся в растворе.
Растворение образующегося полимера. Это одна из наиболее важных функций растворителя при поликонденсации. Дело в том, что поскольку образование макромолекулы при поликонденсации происходит путем взаимодействия концевых функциональных групп олигомеров и макромолекул, то, если эти группы блокированы и «запрятаны» внутрь плотного полимерного клубка (в виде которого можно представить себе осадок полимера), вероятность проникновения концевых функциональных групп внутрь «чужого» клубка весьма мала. Таким образом, полимерные осадки менее реакционноспособны, чем макромолекулы, находящиеся в растворе. Поэтому для успешного протекания поликонденсации желательно, чтобы применяемый растворитель полностью растворял образующийся полимер (подробнее см. с. 151).
РИС. 5.1. Зависимость количества дегндро-хлорида ле-фенилендиалшна, выпавшего в осадок (1), и логарифмической вязкости (2) поди-лс-фенидеиизофталанида при синтезе в диметидацетамиде от содержания дн-хдорангядрпда. введенного на первой стадии при двухстадийной его загрузке [1].
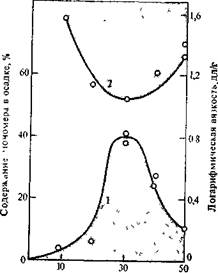
Содержание дихлорангидрида, %
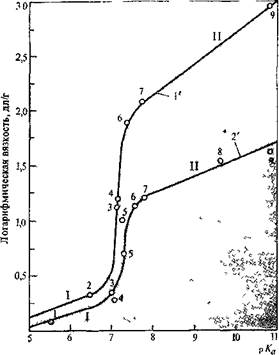
РИС. 5.2. Зависимость логарифмической вязкости полимера от \>Ка акцептора НС1 при полиами-а даровании в хлороформе в присутствии различных акцепторов —»пз>амс-2,В-диметилпиперазнн
6 терефталилхлоридом (!') и «г^>аме-2,5-диметилпи110разнва с себацилхло[)идом (£') [по 2]: 1—пиридин; s—диэтиланилин; з —N-аллилдиэтил-л-толуидин; б—N-метилморфолин; г—N-этилморфолиы; s—N-аллилииперазин; 9 —триэтиламин. Участок/ соответствует выпадению полимера при синтезе; участок II—нахождению полимера в растворе.
. Удаление низкомолекулярных продуктов при обратимой поликонденсации можно интенсифицировать, подбирая соответствующий растворитель. Так, при поликонденсации, сопровождаемой выделением воды, часто используют растворители, образующие с водой низкокипящие азеотропные смеси. Если добавить к реакционной смеси толуол (темп. кип. —110,8°С), то при нагревании вода будет отгоняться в виде 20%-ного (по воде) азеотропа при температуре 84,1°С. Благодаря этому удается добиться быстрого и полного удаления воды из системы и, следовательно, сдвинуть поликонденсационное равновесие в сторону образования высокомолекулярного полимера. Такой вариант проведения поликонденсации получил название азеотропной поликонденсации.
Удаление низкомолекулярных продуктов при необратимой поликонденсации. Применяя специально подобранные растворители, можно подавитьТфотекание побочных реакций с участием низкомолекулярного продукта реакции. Например, при поликонденсации диаминов с дихлорангидридами образующийся НС1 может вступать в реакцию с диамином, образуя нереакционноспособный ангидрохлорид: нН2М— R— \Н2 +
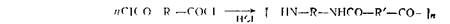
В таких случаях применяют растворители, которые способны связывать низкомолекулярный продукт поликонденсации, превращая его в неактивное по отношению к мономерам соединение. Иногда эти соединения (связывающие выделяющийся низкомолекулярный продукт) добавляют к другому, основному растворителю. При выделении в процессе поликонденсации НС1 в качестве такого растворителя можно использовать амидные соединения (например, диметилацетамид), третичные амины (например, пиридин). В этом случае IIC1 образует гидрохлорид с растворителем, и диамин полностью вступает в реакцию поликонденсации, образуя высокомолекулярный продукт; связывание же выделяющегося НС1 растворителем тем полнее, чем более основен растворитель. На рис. 5.2 приведены данные о синтезе полиамидов в хлороформе в присутствии различных третичных аминов. Из рисунка видна четкая связь между логарифмической вязкостью получающихся полимеров и основностью (рКа) применяемого амина — акцептора НС1 (излом кривых соответствует выпадению полимера).
Ускорение реакции образования макромолекулы также приводит к повышению глубины превращения реакционных центров. Следовательно, применяя растворитель, ускоряющий основную реакцию, можно (при прочих равных условиях) получать полимер с более высокой молекулярной массой.
Имеется много данных, свидетельствующих о том, что природа растворителя весьма существенно влияет на скорость реакций, в том числе и реакций, которые могут составлять процесс поликонденсации.
В табл. 5.1 приведены значения констант скорости модельной реакции — ацилирование моноамина (м-нитроанилина) бензоилхлоридом в различных растворителях. Из таблицы видно, что разные растворители могут изменять скорость реакции в сотни „раз. Следовательно, подбирая растворитель, обеспечивающий высокие скорости образования макромолекул, можно получать высокомолекулярные полимеры.
ТАБЛИЦА 5.1
Константы скорости реакции м-нитроанилина и бензоилхлорида в различных растворителях, Т = 100оС
| Растворитель | Ы02, л'моль-с | Е. кДж'моль | IK в |
| Четыреххлормстый уг лерод | 0,36 | 57. 1 | 5,5 |
| Изопропиловый эфир | 1,00 | 45,8 | 4,4 |
| Бензол | 1,41 | 45,7 | 4,2 |
| Нитробензол | 31,6 | 38,5 | 5,0 |
| Бензонитрил | 45,6 | 6,4 |
* Приведены к температуре 100 °С.
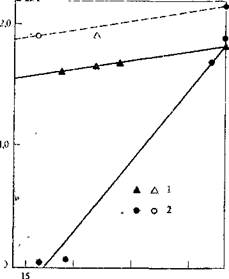
РИС. 5.3. Зависимость констаит скорости реакции поликондрнспции бис-Фенола А и бисхлорформната от ди. Электрической проницаемости смешанного растворителя [по 7]:
1—смесь»-дихлорбензол—нитробензол; г—смесь декалин—нитробензол.
Пунктирная линия соответствует модельной реакции в обеих смесях.
20 25 30
Взаимосвязь молекулярной массы образующегося полимера и константы скорости основной реакции показана на рис. 3.3. Из рисунка видно, что чем быстрее основная реакция, тем больше молекулярная масса образующегося полимера.
Высокие скорости реакций в растворе (в том числе по сравнению со скоростями тех же реакций в газовой фазе) обусловлены, во-первых, «эффектом клетки», т. е. множественности столкновений молекул реагентов за счет окружения («клетки») других молекул, и, во-вторых, протеканием реакций через промежуточные соединения ионного типа.
К сожалению, несмотря на большое число работ [4—6], посвященных кинетике химических реакций в жидких средах, в настоящее время нельзя предсказать скорость реакции в том или ином растворителе. Поэтому растворители, обеспечивающие быстрое протекание поликонденсации, подбирают экспериментально, изучая модельные реакции, т. е. реакции соответствующих монофункциональных соединений.
При использовании данных о скоростях модельных реакций при проведении поликонденсации следует учитывать возможность уменьшения константы скорости реакции образования макромолекулы (по сравнению с константой скорости модельной реакции)
за счет сворачивания макромолекул в растворителях и блокирования таким образом концевых функциональных групп внутри плотно свернутого полимерного клубка, что наиболее вероятно в «плохих» растворителях. На рис. 5.3 сравниваются константы скорости поликонденсации и константы скорости модельных реакций, проведенных в средах с разной растворяющей силой. К раствору мономеров в нитробензоле добавляли два растворителя: дихлорбензол, изменяющий только диэлектрическую проницаемость среды и не влияющий на поведение полимера в растворе, и декалин, изменяющий диэлектрическую проницаемость и сворачивающий молекулы полимера в клубок, так как он является для полимера осадителем *.
Из рис. 5.3 видно, что е.сли реакционная, среда хорошо растворяет полимер, то" константы скорости ноликонденсации и модельной реакции низкомолекулярных соединений примерно совпадают; если же полимер в данной среде сворачивается в клубок, то константа скорости поликонденсации значительно меньше константы скорости соответствующей модельной реакции.
Подавление реакции циклизации также достигается проведением поликонденсации в подходящем растворителе. Так, в табл. 5.2 приведены данные о выходе полимера и циклического продукта (лактама) при поликонденсации 4-тио-е-аминокапроата. Из данных видно, что путем подбора соответствующих растворителей можно существенно понизить выход побочных циклических продуктов (с 50 до 5%).
Приведенными данными не исчерпываются примеры влияния растворителя на поликонденсацию. Так, растворитель может
ТАБЛИЦА 5.2
Влияние растворителя на выход полимерных и циклических продуктов при поликонденсации 4-тио-е-аминокапроата [8]
| Растворитель | Выход лактама, % | Выход полимера, % |
| Метилацетофенон | 5.1 | 94.9 |
| Циклогексанон | 12.9 | 87.1 |
| Диметилацетамид | 17.4 | 82.6 |
| N-метилпирролидон | 25.8 | 74.2 |
| Метанол | 35.8 | 64.2 |
| Тетрагидрофуран | 46.1 | 53.9 |
| Диметилформамид | 49.2 | 50.8 |
* Поскольку мономеры не сворачиваются в клубок, то добавление декалина не влияет на константу скорости модельной реакции.
изменять константу полпконденсацпонного равновесия, интенсив-пост!) побочных реакций с мономерам)! и т. п. Его влияние на ход иоликонденсации весьма многообразно. Выяснение этого влияния на поликонденсационный процесс является важной задачей, поскольку позволяет сознательно регулировать его протекание и таким образом получать полимеры с требуемой молекулярной массой и другими характеристиками, обусловливающими их ценные свойства.
Как будет показано ниже, влияние растворителя обусловлено его свойствами. В этой связи отметим, что общие сведения о физико-химических константах растворителей даны в [9—12], кислотно-основные свойства растворителей описаны в [13], донорное число приведено в [11], параметр растворимости дан в [14], эмпирический параметр полярности—в [12], толкование различных эмпирических параметров приведено в [10].
5.2. Влияние основных факторов на характеристики полимера при поликонденсации в растворе
Закономерности поликонденсации в растворе во многом близки к закономерностям поликонденсации в расплаве, рассмотренным в гл. 2.
Ниже описывается влияние основных факторов на гомогенную поликонденсацию в растворе, т. е. поликонденсацию, при которой образовавшийся полимер полностью растворяется в реакционной среде. Особые случаи самопроизвольного выделения (выпадения) полимера из раствора описаны на с. 151.
50 100
Выход полимера, %
Содержание мономеров, %
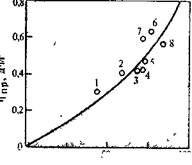
РИС. 5.4. Зависимость приведенная вязкость — выход полимера при поликонденсации дифенилолпропана и дихлорангидрида терефталевой кислоты в дитолилметане при 220°С:
концентрация мономера увеличивается от I до 8.
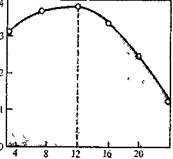
РИС. 5.5. Зависимость логарифмической вязкости полиоксадиазола от исходной концентрации терефталевой кислоты и гидразинсульфата при поликонденсации в 80%-ном олеуме.
Избыток, % (MO;I.J
Диамин
Дихлорангидрид
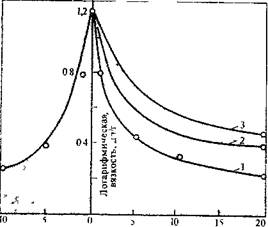
РИС. 5.6. Зависимость логарифмической вязкости полиамида от соотношения м-фенилендиамина и дихлорангидрида изофталевой кислоты при поликонденсации в диметилацетамиде при различном времени дозирования:
1 — быстро; 2 — 20 мин; 3 — 40 мин.
Зависимость вязкость — выход полимера. Эта зависимость отражает влияние глубины протекания, процесса на молекулярную массу полТТмеров при" поликонденсации в растворе: приведенная вязкость полимера возрастает при увеличении его выхода (рис. 5.4). Следовательно, для получения высокомолекулярных полимеров поликонденсацией в растворе необходимо обеспечить условия для протекания основной реакции на значительную глубину.
Примеси монофункциональных соединений. Присутствие даже небольших количеств добавок этих соединений jiesKo снижает молекулярную массу образующегося полимера при поликонден-сацни в растворе. Поскольку обычно роль таких добавок играют примеси в мономерах и растворителе, то становится очевидной необходимость их тщательной очистки.
Концентрация мономеров. Зависимость молекулярной массы от концентрации мономеров при~пол"ик"онденсации в растворе описывается^ как правило, криво'и'"с7мЩсШумЬм."*Типичная кривая этой зависимости приведена на рис. 5.5. Такой вид кривой обычно объясняется снижением (по сравнению с точкой максимума) молекулярной массы полимера за счет возрастания удельной концентрации примесей при малых концентрациях мономеров и прекращением процесса при больших концентрациях мономеров вследствие высокой вязкости системы.
Соотношение мономеров при гетерополиконденсации. При быстром одновременном дозировании мономеров для гетерополиконденсации в растворе наблюдается резкая зависимость молекулярной массы полимера, от их соотношения (рис. 5.6). В ряде случаев ветви этой зависимости не являются симметричными вследствие протекания побочных реакций или из-за эффекта саморегулирования при медленном дозировании одного из мономеров (подробнее см. гл. 3).
При получении полимеров с максимальной молекулярной массой при обратимых процессах поликонденсации в растворе скорость и порядок дозирования мономеров не имеют значения. При необратимых реакциях поликонденсации эти факторы играют существенную роль (см. гл. 3).
Температура. В зависимости от температурного режима проведения процесса различают высокотемпературную и низкотемпературную поликонденсацию в растворе.
Высокотемпературная поликонденсация протекает при температурах дыще. 100°С. Используемые при этом мономеры имеют низкую реакционную способность, что и определяет необходимость проведения процесса при повышенных температурах. Примеры
ТАБЛИЦА 5.3
Получение полимеров высокотемпературной поликонденсацией в растворе
| Процесс | Исходные мономеры | Растворитель | Температура синтеза, °С |
| Полиэтерификация | Бисфенолы и дихлорангидриды карбоновых кислот | Динил, дитолилметан, тетралин, совол, нитробензол, хлорнафталин, хлорбензолы | 160-220 |
| Образование полисульфонов | Бисфеноляты и дихлордиарилы | Диметилсульфоксид | 170-180 |
| Образование полифениленсульфида | К2S + дихлорбензол | N-Метил-a -пирролидон | 220-250 |
| Поликонденсация с циклодегидратацией | Дикарбоновые кислоты и производные гидразина | Олеум | 120-150 |
| Поликонденсация с циклодегидратацией | Диаминодикарбоксиарилы и различные производные дикарбоновых кислот и другие соединения | Полифосфорная кислота | 140-160 (до 200) |
| Поликонденсация с циклодегидратацией | Тетракарбоновые кислоты и тетраамины | Расплавы смесей солей — кислот Льюиса (SbCl5, BiCl3, AIC13, SnC12 и др.) | ~180 |
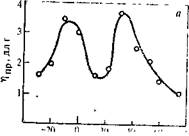
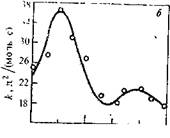
20 0 20 40" 60 SO Температура,°С
РИС. 5.7. Зависимость приведенной вязкости полимера и константы скорости реакции от температуры синтеза: а— терефталоилхлорид + дихлордиан; б—модельные соединения: п -хлорбензоилхлорид + о-хлорфенол.
получения некоторых полимеров высокотемпературной поликонденсацией приведены в табл. 5.3.
Низкотемпературная поликонденсация в растворе проводится при температурах ниже 100°С с использованием высокореакционных систем или катализаторов.
Такое деление в значительной степени условно и введено в основном по технологическим соображениям.
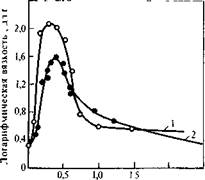
В более узком интервале влияние температуры на поликонденсацию в растворе может быть весьма разнообразным:,..молекулярная масса полимера может уменьшаться или увеличиваться с повышением температуры синтеза, причем наблюдались даже случаи экстремальной зависимости. Рядом авторов были получены кривые с двумя максимумами (рис. 5.7). Все зависит от температурной зависимости скоростей реакций, составляющих процесс поликонденсации. Так, данные, приведенные на рис. 5.7, можно объяснить [18] аналогичным температурным ходом константы скорости реакции роста, которая определяется тремя реакциями: некаталитической реакцией, каталитической за счет основного катализа и каталитической за счет нуклеофильного катализа. Изменение соотношения этих трех реакционных потоков дает бимодальную кривую зависимости общей скорости от температуры, что «копируется» температурной зависимостью вязкости полимера от температуры.
5.3. Поликонденсация в бинарных растворителях
При использовании растворителей в процессах поликонденсации в ряде случаев бывает целесообразным применять..бинарные и многокомпонентные растворители. При этом та или иная функция растворителя может выполняться различными компонентами
Температура,°Г
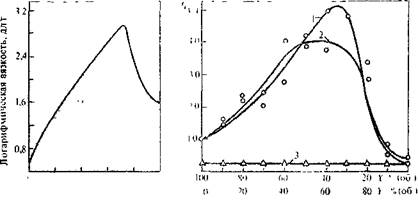
О 20 40 60 80 100
Содержание tei раме шлеи -
сульфона.'" ("об)
РИС. 5.8. Зависимость логарифмической вязкости нолииочовины на основе З^-диметялиипера-зина и (/ио(4-нзоцианатфеиил)мс>тапи от состава бинарной смеси тстраметилснсульфоп — хлороформ [»].
РИС. 5.9. Зависимость удельной вязкости полв.п-фениденторефталамнда от состава бинарной
смеси [10]:
1—гексаметилфосфорчриаыид (ж)—N-метилпирролидон (у); s—гексаметилфогфортриамид (ж) — диметилацетамид (у); 3—N-метил-а-пирролидон (х)—диметилацетамид (у).
сложного растворителя. Поэтому в бинарных или многокомпонентных растворителях создаются наиболее благоприятные (оптимальные) условия для получения высокомолекулярных продуктов. Зависимость молекулярной массы полимера от состава бинарного растворителя описывается, как правило, кривой с максимумом.
Бинарные растворители находят все более широкое применение в лабораторной и промышленной практике. Ниже кратко рассмотрены наиболее важные случаи поликонденсации в бинарных растворителях.
Смеси двух растворителей. В качестве примера можно привести синтез полимочевины из г/эанс-2,5-диметилпиперазина и бис-(4-изоцианатфенил)метана в присутствии тетраметиленсульфона и хлороформа [2] (рис. 5.8).
Из рисунка видно, что полимер с максимальной молекулярной массой получается при определенном составе реакционной смеси.
Повышение молекулярной массы (вязкости) полимочевины при увеличении содержания тетраметиленсульфона автор объясняет увеличением растворяющей способности растворителя, а снижение вязкости при 70% тетраметиленсульфона — сильным увеличением вязкости реакционной системы и ухудшением растворимости одного из мономеров (диамина). Кстати, повышение растворяющей способности является одной из наиболее частых причин возрастания молекулярной массы полимера при синтезе в бинарном растворителе.
Смеси неполярных растворителей и третичных аминов. Эти
смеси широко используются для синтеза многих полимеров. Наиболее изученной является реакция получения ароматических полиэфиров
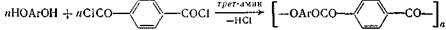
Эти смеси выполняют сложную функцию, так как третичный амин является и акцептором выделяющегося НС1, и катализатором основной реакции, причем катализ также является очень сложным, поскольку протекает по двум механизмам: основному и нуклеофилыюму. Поэтому естественно, что в таких растворителях в зависимости от природы и количества третичного амина изменяются некоторые закономерности поликонденсации.
Смеси амидных растворителей. Эти смеси могут быть использованы для синтеза высокомолекулярных ароматических полиамидов. Так, на рис. 5.9 приведены зависимости удельной вязкости поли-л-фенилеитерефталамида от состава смеси амидных растворителей. Из рисунка видно, что в смеси двух амидных растворителей (гексаметилфосфортриамид — N-метил-а-пирролидон и гек-саметилфосфортриамид — диметилацетамид) полимер получается с очень высокими молекулярными массами. В то же время смеси других амидных растворителей такого эффекта не дают (например, диметилацетамид— N-метил-а-пирролидон). Это объясняется тем [19], что в растворах с гексаметилфосфортриамидом образуется комплекс между компонентами растворителя, который обладает большей растворяющей способностью к полимеру. Кроме того, это подтверждается ЯМР-спектрами смешанных растворов и растворимостью тримеров.
Амидно-солевые системы. Эти системы широко применяются для синтеза, например, ароматических полиамидов и некоторых полиуретанов. Было показано, что введение в амидный растворитель неорганических солей (LiCl, СаС12, MgCl2 и др.) значительно увеличивает удельную вязкость получающегося полимера.
Влияние неорганических солей при синтезе полимеров в амид-но-солевых растворителях двояко. Положительное влияние (увеличение молекулярной массы при введении солей) можно объяснить увеличением растворяющей способности амидно-солевого растворителя и ускорением основной реакции поликонденсации. Так, в работе [21] показано, что реакция ацилирования анилина изофталилхлоридом ускоряется солями металлов: в присутствии LiCl (1,77 моль/л) константа скорости возрастает примерно в 560 раз. Для некоторых других реакций, например образования полиуретанов, каталитического эффекта вводимых солей обнаружено не было [22].
В ряде случаев введение солей в амидный растворитель может отрицательно повлиять на ход поликонденсации вследствие интенсификации протекания побочных реакций. Этим объясняется [23]
Содержание tei раме шлеи -сульфона.'" ("об)
различное влияние солей при синтезе растворимых и нерастворимых полиамидов: молекулярная масса нерастворимых полимеров увеличивается, а растворимых уменьшается. В первом случае эффект введения соли является суммарным, г.е. увеличение молекулярной массы за счет увеличения растворяющей способности оказывается большим, чем влияние ускорения побочных реакций.
Водно-органические смеси. Эти смеси также могут использоваться в качестве реакционных сред при различных реакциях поли-Лонденсации. Примеры успешного использования водно-органических сред для получения жирноароматически.х полиамидов приве дены на рис. 5.10.
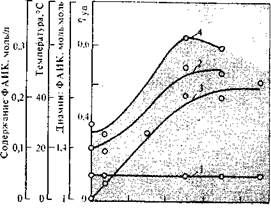
Исследование поликонденсации в водно-органических смесях показало, что оптимальные условия синтеза (соотношение и концентрация мономеров, температура и т.д.) изменяются в зависимости от состава смеси (рис. 5.11). Из рис. 5.11 видно, что с увеличением содержания воды в системе (от 0 до 50%) не только увеличивается молекулярная масса образующегося полимера, но и существенно изменяются оптимальные условия синтеза (условия получения полимера с максимальной молекулярной массой): увеличивается оптимальная температура, изменяется оптимальное соотношение мономеров и т.д.
Влияние воды в водно-органических средах на закономерности поликонденсации весьма многообразно. Обычно роль воды сводят к интенсификации побочных реакций гидролиза мономеров. Однако вода может оказывать и положительное влияние на поликонденсацию. Это можно объяснить увеличением степени набухания некоторых полимеров в присутствии воды, а также ускорением реакций, ответственных за возрастание молекулярной массы за счет специ-
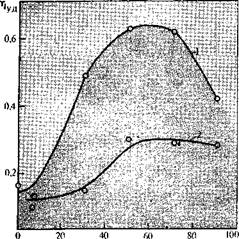
рис. 5.10. Зависимость удельной вязкости полимера при поликонденсации гсксаметнаендиамина и дифтор-ангидрида изофталевой кислоты от содержания воды в реакционной среде (изопропнловый спирт-вода) [20]:
1—при оптимальном соотношении
мономеров (ом. рис. 5.11): Я—при
экмгмольном соотношении.
Содержание воды,% (об)
20 40 60 80
Содержание воды % (об.;
РИС. 5.11. Зависимость оптимальных значений концентрации мономеров (1), температуры
синтеза (£), соотношения мономеров (3) и удельной вязкости (4) полимера от содержания
воды в реакционной среде нзопропиловый спирт—вода при поликонденоацяи гексаметилен-
дианина и дифторангидрида изофталевой кислоты (ФЛИК) [20).
фических свойств воды (высокой диэлектрической проницаемости, способности к сольватации, наличием межмолекулярных водородных связей, обеспечивающих эстафетный механизм переноса протона и т.д.) [20].
5.4. Поликонденсация в активных растворителях
Активными являются растворители, которые в заметной степени взаимодействуют хотя бы с одним мономером, снижая молекулярную массу образующегося полимера. Несмотря на это, такие растворители могут применяться для получения достаточно высокомолекулярных полимеров, если скорость основной реакции (образования макромолекул) значительно выше скорости побочных реакций, приводящих к химической дезактивации реакционных центров.
В общем, использование таких растворителей для целей синтеза невыгодно, так как из-за побочных реакций получить полимер высокой молекулярной массы в них довольно трудно. Однако другие полезные свойства таких растворителей, например доступность, часто повышенная растворяющая способность по отношению к полимеру, делают их применение для синтеза полимеров весьма заманчивым.
Обычные технологические операции, используемые при проведении поликонденсации в растворе — растворение мономеров в растворителе и их смешение, — часто оказывается неприемлемыми при
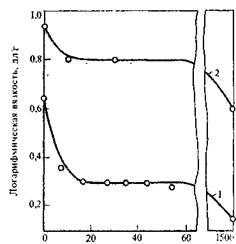
1'ПС. 5.12. Зависимость логарифмической вязкости полн-л1-фениленизофтал-имида от продолжительности выдержки дига.'югснангидридов в растворителе при синтеае в диметилапотамиде [24|;
I — дихлорангидрид изофталеной кислоты; -j — дифторангидрид изофталеной кислоты (точки на оси ординат отвечают загрузке твердого продукта).
Время,.мин
поликонденсации в активных растворителях. Так, на рис. 5.12 показано, что даже 10-минутное пребывание дихлорангидридов кар-боновых кислот в диметилформамиде приводит к резкому (почти в 2 раза) снижению вязкости полимера. Поэтому проведение поликонденсации в активных растворителях требует применения особых приемов (см. ниже).
Оценка активности растворителя. При работе с активными растворителями очень важно оценить «степень активности» растворителя, т. е. выяснить, насколько интенсивно он реагирует с мономером. Интенсивность этого взаимодействия может быть настолько большой, что практически окажется возможным получение достаточно высокомолекулярного продукта.
Такая оценка весьма полезна для ряда растворителей и мономеров, так как она позволяет изменить методику синтеза полимера в зависимости от степени этой активности.
Одним из способов такой оценки является проведение синтезов на модельном (низкомолекулярном) соединении. Так, изучение [23, 25] взаимодействия дихлорангидрида нзофталевой кислоты с амид-ными растворителями в присутствии анилина показало, что в системе протекают следующие конкурирующие реакции:
+ Анилин
------------------> Целевой продукт
Дихлорангидрид —
Побочный продукт
что образование целевого продукта—дианилида изофталевой кислоты в присутствии диметилформамида протекает с меньшим выходом вследствие расхода дихлорангидрида в реакции с растворителем. Это является основной причиной получения низкомолекулярных ароматических полиамидов из дихлорангидридов в среде диметилформамида.
Данные правой колонки табл. 5.4 получены после 24-часовой выдержки дихлорангидрида в растворе. Это сделано для того, чтобы относительная разность, характеризующая активность растворителей, проявилась более заметно. Так, если при загрузке дихлорангидрида в твердом виде второй,третий и четвертый растворители кажутся почти одинаковыми, то по данным правой колонки табл. 5.4 они существенно различаются. Это подтверждается данными о синтезе полимеров.
.Для быстрой полуколичественной оценки относительной активности растворителей амидного типа в реакции с дихлорангидрида-ми очень удобен термохимический метод, по которому определяется теплота взаимодействия мономера с активным растворителем.
Поскольку теплота процесса собственно растворения и реакция взаимодействия с растворителем, как правило, существенно различаются, то по экспериментально найденной теплоте растворения можно оценить активность растворителя.
В табл. 5.5 приведены данные о теплотах взаимодействия дихлорангидрида изофталевой кислоты с некоторыми растворителями, применяемыми в практике поликонденсации. Для инертных к данному соединению растворителей (группа А — растворители 1-—4) характерен только эндотермический эффект, обусловленный
ТАБЛИЦА 5.4
Оценка активности амидпых растворителей
к дихлорангидриду изофталевой кислоты по реакции
в присутствии модельного соединения (анилина) [23, 25]
Количество непрореагнровавшего анилина, %
| Амидный растворитель | при загрузке твердого дихлорангид-рида н раствор анилин а | при загрузке анилина * в раствор ди-хлорангидрида |
| Диметилформамия | — | |
| Диметнлацетамид | 0,4 | |
| Диметилацетамид + LiCl (1,7 моль/л) | 0,6 | 15,9 |
| Диметилацетамид + ZnCl2 (0,4 моль/л) | 1,3 | 49,1 |
Анилин загружали в раствор дихлорангпдрида через 24 ч после его прпготонления.
растворением мономера; синтез полимеров в этих растворителях ведется по обычной методике.
Для очень активных растворителей (группа В — растворители 8—!0) характерен большой эндотермический эффект взаимодействия дихлорангидрида с растворителем, соизмеримый с суммарным эффектом поликонденсации; в растворителях этой группы получение высокомолекулярных полимеров невозможно.
Для активных растворителей (группа Б — растворители 5—7) при измерении теплового эффекта вначале наблюдается эндотермический эффект растворения мономера, а затем сравнительно небольшой, растянутый во времени экзотермический эффект взаимодействия дихлорангидрида с растворителем.
Таким образом удалось получить ряды растворителей по их активности к хлорангидридам, а также оценить их относительную активность к различным мономерам (рис. 5.13). Определяя теплоту взаимодействия различных мономеров в одинаковых растворителях, можно получить данные, характеризующие относительную
ТАБЛИЦА 5.5
Теплота растворения и теплота взаимодействия
дихлорангидрида изофталевой кислоты с различными
растворителями при 25 °С [26]
| Шй пп. | Растворитель | нвя 'теплота Теплота взаи-оаствопе модействия растворе с pacTBOplITe. кДж/моль лем' «Дж/моль | Время взаимодействия, мин | Возможность син теза высокомолекулярных по лиамидов |
| А | . Неактивные растворители | |||
| Нитробензол | -22,6 — | Да | ||
| Метиленхлорид | -21,4 | Да | ||
| Толуол | —21,0 — | Да | ||
| Тетрагидрофуран | -15,6 - | Да | ||
| Б. | Активные растворители | |||
| Тетраметилмочевина • | — 10,5 18 | Да | ||
| М-метил-а-пирролидон | -16,4 40 | Да | ||
| Диметилацетамид | -17,2 57 | Да | ||
| В. | Очень активные растворители | |||
| Пирролидон | -(17) * 176 | 0,5 | Нет | |
| Диметилформамид | —(17) * 222 | 0,5 | Нет | |
| Диметилсульфоксид | -(17) * 226 | 0,5 | Нет |
Приближенные значения.
активность растворителя к ряду мономеров. Ниже приведены такие данные для систем дигалогенангидрид — диметилацетамид [26J:
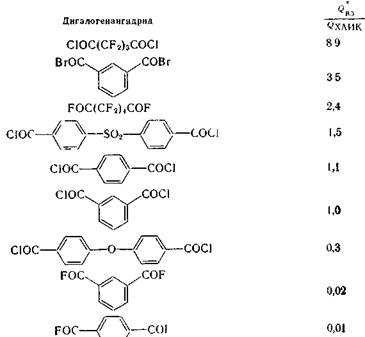
* Q —теплота взаимодействия дигалогенангидрида с диметилацетамидом; <?ХАИК~ теплота взаимодействия дихлорангидрида изофталевой кислоты с ДМАА в тех же условиях.
Из этих данных следует, что если для одних мономеров данный растворитель является очень активным, для других он малоактивен. Поэтому слишком активные растворители (группа В, табл. 5.5),
РИС. 5.13. Взаимосвязь логарифмической вязкости полимера и суинариого теплового эффекта при поликонденсацин дихдорангид-рида изофталевой кислоты и.ч-фсчш.н'л-днанина п днметилацетаниде в присутствии различных третичных аминов [27]:
1—без амина; s —диметиланилин; з — пири-Дин; 4 — а-пиколин; 5 — р-ииколин.
Суммарный тепловой эффект, кДж/моль
ТАБЛИЦА 5.0
Удельны/' вязкости ароматических полиамидов, полученных из /><u.iичпых дигалогенаигидридов в растворе [24]
Удельная вязкость полимера
| Диамин | Удельная | вязкость полимера |
| дихлорангидрид дифторангидрид изофталевой кислоты терефталевои кислоты | ||
| лс-Фенилен диамин о-Толидин м Фенилендиамин | Растворитель — 0,08 0,07 Растворитель — 0,06 | диметилформамид 0,70 1,08 диметилсульфоксид 0,76 |
непригодные для синтеза ароматических полиамидов на основе ди-хлорангидридов карбоновых кислот, оказались пригодными для синтеза тех же полимеров с использованием дифторангидридов тех же кислот (табл. 5.6 и рис. 5.12).
Термохимическая оценка активности растворителя хорошо коррелирует с данными о синтезе полимеров: чем больше теплота взаимодействия днхлорангидрида с растворителем (а значит, тем интенсивнее протекают побочные процессы), тем меньше молекулярная масса (логарифмическая вязкость) образующегося полимера (см. рис. 5.13).
Особенности синтеза полимеров. Использование активных растворителей требует особых приемов при работе с ними. Так, необходимо сократить время контакта мономера с этим растворителем,, по крайней мере, до начала поликонденсации. При синтезе ароматических полиамидов это достигается дозированием в реакционную систему одного из мономеров, например дихлорангидрида дикарбо-новой кислоты, в твердом виде, а не в виде раствора (см. рис. 5.9).. Дозирование дихлорангидрида в виде предварительно приготовленного раствора приводит к получению низкомолекулярного полимера..
Для уменьшения 'времени контакта мономеры, способные к побочным реакциям, следует вводить в реакционную систему в твердом виде с небольшой скоростью; при этом молекулярная масса: полимера должна увеличиваться.
Дальнейший поиск новых приемов поликонденсации в активных растворителях и уменьшение относительной доли побочных реакций является очень важной задачей, успешное решение которой зачастую определяет успех создания промышленного технологического процесса.
В этой связи интересны результаты работы [28], в которой на примере поликонденсации л-фенилендиамина с дихлорангидридом терефталевои кислоты в амидном растворителе было показано, что
такие простые параметры процесса смешения реагентов, как интенсивность перемешивания, нремя дозирования, температура при смешении существенно влияют на интенсивность побочных процессов дихлорангидрида с амидным растворителем; это, в свою очередь, определяет молекулярную масеу образующегося полимера.
На рис. 5.14 приведены данные, иллюстрирующие изменение относительной доли побочной реакции при различной интенсивности смешения мономеров. Эта доля определялась по количеству анилина, прореагировавшего с дихлорангидридом в данных условиях. Высокий процент прореагировавшего анилина свидетельствует о малом количестве побочных реакций. Из рисунка видно также, что интенсивность побочных реакций снижается при повышении интенсивности перемешивания реагентов. В связи с этим повышается молекулярная масса получающегося полимера. Так, кривая 1 соответствует удельной вязкости поли-4,4'-дифениленсульфонтерефтал-амида, равной 0,9, а кривая 2—1,4. Кроме интенсивности перемешивания молекулярная масса полимеров при синтезе в активных растворителях существенно зависит от скорости дозирования реагентов и их агрегатного состояния (рис. 5.15).
Активные растворители вполне могут быть применены для синтеза различных полимеров. Так, авторами работы [20] была исследована поликонденсация диаминов с дифторангидридами в водно-
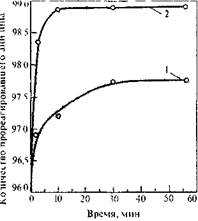
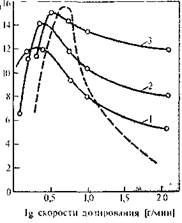
РИС. 5.14. Кинетические кривые взаимодействия дихдорангидрида терефталевои i HC.IGIM в «як-лином в среде димстилацетамид — L1C1 ири различной интенсивности перемешивания 1281:
1—300 об/мин; г—3000 об/мин.
РИС. 5.15. Зависимость удельной вязкости поли-п-Фенилентерефталамида от скорости дознро-
ваняя расплава дихлорангидрида терефталевои кислоты при поликонденсация в системе
диметилацетамид — 1ЛС1 при различной интенсивности перемешивания:
1 — 500 об/мив; Я — 15UO; з — 3000 об/мин. Пунктирная кривая соответствует дозированию дихлорангидрида в твердом виде.
спиртовых средах, т.е. в средах, в которых оба компонента актив-ны в определенной степени по отношению к дифторангидридам. Было показано (см. рис. 5.10), что при содержании воды в спирте до 60% удельная вязкость полимера увеличивается за счет ускорения основной реакции — ацилирования и только при содержании воды в системе выше 70% молекулярная масса полимера начинает уменьшаться за счет увеличения доли гидролиза.
В настоящее время поликонденсация в активных растворителях лежит в основе промышленного метода получения важного класса термостойких полимеров — ароматических полиамидов.
5.5. Поликонденсация, сопровождаемая самопроизвольным выделением полимера из раствора
Этот тип поликонденсации похож на обычную поликонденсацию в растворе; он отличается от нее только тем, что в ходе процесса (иногда практически сразу после смешения мономеров) образующийся полимер самопроизвольно выделяется (выпадает) из реакционной среды из-за ее недостаточной растворяющей способности по отношению к полимеру,
Поликонденсация с выделением полимера из раствора в настоящее время получает все большее распространение в связи с развитием химии и технологии необратимых процессов поликон-
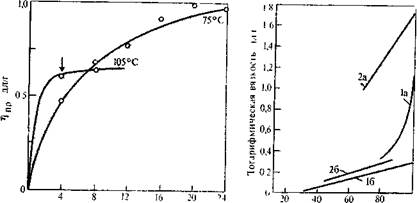
Время, ч
Выход полимера, %
РИС. 5.16. Кинетические кривые нарастания приведенной вязкости полимора при поликонденсации о-толидина и дифтораигидрида изофталевой кислоты [24] при синтезе в днмстнлапета-ниде при различной температуре. Стрелкой отмечено время выпадения полимера из раствора.
РИС. 5.17. Зависимость вязкость — выход полимера для поликонденсации в растворе, сопровождаемой выпадением полимеров при 'синтезе [30]:
1 — этиленгликоль — 4,4'-дифенилмет;шдиизоцианат; s — 2,5-диметшшиперазин — дихлорангид-
рид себациновой кислоты; а — полностью гомогенная система; S — полимер выпадает в осадок.
денсации. Ниже рассмотрены основные особенности таких процессов.
Основные закономерности процесса. Выпадение полимера при синтезе, как правило, вызывает отклонение от закономерностей поликонденсации, характерных для простейших случаев.
Самопроизвольное выделение (выпадение) полимера из раствора обычно приводит к прекращению процесса поликонденсации и получению полимера с меньшей молекулярной массой. На рис. 5.2 показано, например, что при выпадении полимера его молекулярная масса меньше, чем при поликонденсации в полностью гомогенных системах (при одних и тех же параметрах). Это подтверждается также кинетическими кривыми, полученными при синтезе поли-n-фениленизофталамида (рис. 5.16). Кинетическая кривая процесса, сопровождаемого выпадением полимера из раствора, запредели-вается, т.е. в случае выпадения полимера из раствора (кривая 2) нарастание молекулярной массы полимера прекращается раньше, чем при поликонденсации в полностью гомогенном растворе. Действие, аналогичное выпадению полимера из раствора, т. е. прекращение процесса поликонденсации, наблюдается при образовании в' ходе процесса полимерного студня (геля). Это было отмечено, например, при синтезе жесткоцепного поли-п-фенилентерефталами-да в смеси гексаметилфосфортриамида с N-метил-сс-пирролидоном (2: 1 по объему) при концентрации более 0,4 моль/л [29].
Зависимость вязкость — выход полимера, отражающая соотношение между молекулярной массой полимера и глубиной превращения для некоторых процессов, сопровождаемых выпадением полимера, приведена на рис. 5.17. Из рисунка видно, что эта зависимость очень «чувствительна» к выпадению полимера. Так, части кривых, описывающие поликонденсацию в полностью гомогенных системах и в системах с выпадением полимера, не «стыкуются»: вязкость полимеров, выпавших при синтезе, меньше, чем в тех случаях, когда полимер полностью (и до конца процесса) остается в растворе.
При поликонденсации в растворе, сопровождаемой выпадением полимера из реакционной среды, изменяется такая характерная зависимость необратимых процессов поликонденсации, как зависимость молекулярной массы полимера от скорости дозирования мономера, взятого в избытке. Как видно из табл. 5.7, медленное прибавление второго реагента при поликонденсации, сопровождаемой выпадением полимера, приводит к получению полимера с меньшей молекулярной массой, чем при быстром смешении. В случае полностью гомогенной системы наблюдается обратная картина: при медленном дозировании получается полимер с большей молекулярной массой, чем при быстром. Это обусловливается тем, что самопроизвольно выделившийся (выпавший) полимер является нереак-ционноспособным.
Из приведенных примеров видно, что, несмотря на значительное торможение реакции роста цепи за счет выпадения полимера,
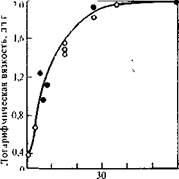
молекулярная масса получающегося при этом полимера достаточно высока. Это значит, что достаточно длинные макромолекулы полимера успевают образоваться за время от начала контакта (смешения) мономеров до момента самопроизвольного выделения полимера из реакционной среды. Это подтверждается данными рис. 5.18, на котором приведена зависимость вязкости поли-л-фе-нилентерефталамида от содержания хлорида лития в системе. Введение LiCl сильно изменяет свойства реакционной среды, сначала увеличивая ее растворяющую способность, а затем, по достижении определенного содержания, высаливая полимер из раствора. Если эту зависимость выразить в виде время пребывания полимера в растворе—логарифмическая вязкость, то видно, что все экспериментальные точки лягут на одну кривую (рис. 5.19). Следовательно, поликонденсация, сопровождаемая самопроизвольным выделением 'полимера из реакционной среды, происходит до этого момента как бы в гомогенном метастабильном растворе.
Метастабильные растворы полимеров. Такие растворы термодинамически неустойчивы и характеризуются иными параметрами, чем равновесные (истинные растворы): степенью пересыщения (отношением концентрации в данный момент к равновесной) и време-Н£м жизни (т.е. временем его существования до момента разделения на фазы: фазу полимера и фазу растворителя). К сожалению, к настоящему времени метастабильные растворы полимеров изучены мало. Так, известна, например, зависимость времени пребы-
ТЛЕ.ШЩА 5.7
Зависимость молекулярной массы (вязкости) полиэфиров щавелевой кислоты от скорости дозирования оксалилхлорида
| •Синтезируемый полимер | Логарифмическая вязкость | |
| постепенное дочнро вание {10 мин) | быстрое позирование ('2 — 3 с) | |
| Полимеры выпадают из | раствора при синтезе |
2,0 2,5
Содержание соли, моль/л
1О 20
40 50 60
Время, мин
РИС. 5.18. Зависимость логарифмической вяакости поли-п-фенилеитерефтадамида при синтезе)
в днметвлацетамиде от концентрации соли i» реакционной среде [31]:
О—L1CI; ф-ЫИг.
РИС. 5.19. Зависимость логарифмической вязкости ноли-гг-феиидентсрефталамида от времени! пребывания полимера в растворе при синтезе в двметилацетамиде с добавками солей [31];
О—LiCl; • — LiBr.
вания полимера в растворе от его концентрации и содержания хлорида лития (рис. 5.20). Можно предполагать, что закономерности их образования будут аналогичны закономерностям пересыщенных растворов низкомолекулярных соединений. Согласно теории пересыщенных растворов низкомолекулярных соединений [32], чем выше скорость реакции образования соединений, тем большая степень пересыщения может быть достигнута. Поэтому при рассмотрении поликонденсации, сопровождаемой самопроизвольным выпадением (выделением) полимера из реакционной среды, следует также иметь в виду, что при таком варианте поликонденсации большое значение играют абсолютные скорости образования макромолекул. Если эта скорость велика, то макромолекула «успеет» вырасти за время, определяемое стабильностью метастабильного раствора (время его жизни); если скорость образования мала, то полимер выделится (выпадет) из реакционной среды низкомолекулярным. На основе данных по пересыщенным растворам низкомолекулярных соединений можно полагать, что че_м больше сродство растворителя к полимеру, тем больше время жизни пересыщенного раствора полимера (его стабильность), тем более высокомолекулярный полимер получится в таком растворе. И, следовательно, наиболее высокомолекулярный полимер образуется в средах, имеющих наибольшее сродство к полимеру.
Если за такое сродство принять степень набухания полимера, то чем она выше, тем более высокомолекулярным образуется полимер. Об этом свидетельствуют данные рис. 5.21.
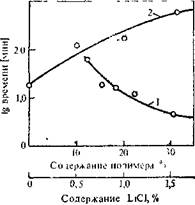
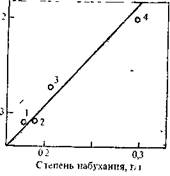
РИС. 5.20. Зависимость логарифма времени жизни реакционных растворов поли(4,4'-дифенилен-сульфон)терефталамида при синтезе в N-метил-а-пирролидоне от концентрации образовавшегося полимора (1) и концентрации добавленного lit] (35J.
РИС. 5.21. Зависимость приведенной вязкости полиарилата на основе терефталевой кислоты и фенолфталеина от степени набухания при синтезе в различных реакционных средах [IS]:
i—ацетон; г — метилэтилкетон; а—ацетон —бензол в соотношении 88: 12 (по объему); 4 — ацетон— бензол в соотношении 69: 31 (по объему).
Следует полагать, что чем больше степень набухания полимера в реакционной среде, тем больше время жизни метастабильного раствора полимера.
В этой связи большое значение приобретают методы оценки степени набухания полимера в реакционных средах.
Определение набухающей способности растворителя. Степень набухания определяют различными способами: весовым, объемным и др., причем для этого можно воспользоваться образцом полимера, полученного другим способом (в системе несмешивающихся жидкостей, в твердой фазе и т.д.).
Однако все эти методы для слабонабухающих полимеров непригодны из-за их малой точности. Более точным является определение температур стеклования полимера: жидкость, взаимодействующая"с полимером, изменяет (понижает) температуру стеклования полимера. На рис. 5.22 приведены данные о температуре стеклования и удельной вязкости полигексаметиленизофталамида в бинарном растворителе тетрагидрофуран — вода. Из рисунка видно, что изменение температуры стеклования полимеров в зависимости от состава растворителя симбатно изменению удельной вязкости полимера при синтезе в том же растворителе.
Интересный способ оценки степени набухания полимера был применен авторами работы [33]. Он основан на изучении скорости упорядочения (кристаллизации) полимера в растворителях различного состава: кристаллизация полимера быстрее протекает в жидкостях, способствующих набуханию полимера. По этому спосо-
бу образны наиболее разупорядоченного полимера помещают на одинаковое время в различные растворители и по окончании опыта вновь оценивают их упорядоченность. В «наилучшем» для данного полимера растворителе упорядоченность образца увеличивается в большей степени.
Упорядоченность полимера после выдержки в изучаемых растворителях можно измерить прямыми способами (например, рентгенографически). Однако более простым является способ, основанный на оценке снижения растворимости упорядоченного полимера. Поскольку упорядоченный полимер „хуже растворим, чем исходный, то, определяя растворимость образца после выдержки в растворителях (например, по мутности получаемых растворов), можно оценить набухающую способность растворителя. Чем хуже р'астворим полимер, тем выше была набухающая способность растворителя, в котором выдерживался образец. Так, из данных рис. 5.23 следует, что для ароматического полиамида наилучшую набухающую способность имеет смесь тетрагидрофурана и воды в соотношении 90: 10 (по объему).
Все эти методы оценки набухающей способности растворителя предполагают, что полимер синтезирован заранее (например, другими методами), что не всегда возможно.
С этой точки зрения интересны способы, основанные на определении растворимости модельных низкомолекулярных соединений, растворимость которых в ряду растворителей будет симбатна растворимости аналогичных полимеров. Модельное низкомолекулярное соединение подбирают так, чтобы по строению оно было похоже на фрагмент полимерной цепи. Например, полигексаметилен-
избфталамиду
г_СОМН(СН2)в\'НСОч

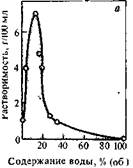
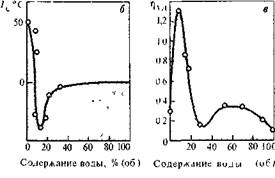
РИС. 5.22. Зависвмость растворимости модельного соединенна (а), температуры стекловании полимора (6) и удельной вязкости полимера (в) от состава растворителя при поликонденсации гексаметилендиамина и дифторангидрида терефталевой кислоты в смеси тетрагидрофуран —
вода [20].
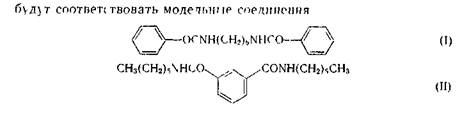
По растворимости модельных соединений в ряду растворителей можно получить информацию об относительной силе того же ряда растворителей по отношению к полимерам аналогичного строения. Плодотворность такого подхода иллюстрируется рис. 5.22, из которого видно, что растворимость модели хорошо коррелирует как с изменением температур стеклования, так и с изменением удельной вязкости полимера, получаемого в этих же средах.
Роль упорядоченности полимера при синтезе. Особенно резкое замедление наращивания полимерной цепи происходит при выпадении полимера из реакционной смеси в кристаллическом виде. Большая плотность кристаллического продукта обусловливает практически полное отсутствие реакционной способности полимерных осадков. При не очень плотном осадке, особенно аморфном, е некоторых случаях процесс поликонденсации может продолжиться (рис. 5.24).
s 5
-е
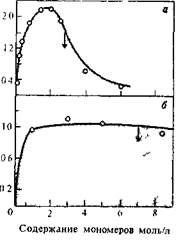
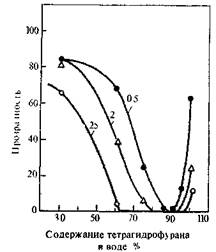
РИС. 5.23. Зависимость прозрачности 5%-ных растворов поли-лс-фсниленизофталамида в ди-
нетадформаицде от состава смеси, в которой происходит упорядочение полимера [38]. Цифры
на кривых —продолжительность выдержки полиптера в смеси в часах.
РИС. 5.24. Зависимость логарифмической вязкости поли(дифсниленсульфон)амидов от концентрации мономеров при синтезе в растворе диметилацетамнда [24]:
а—кристаллизующийся поли(4,4'-дифениленсульфон)амид; в—некристаллизующийся ноли-(3,3'-дифениленсульфон)амид. Стрелками отмечено выпадение полимера при синтезе.
РИС. 5.25. Зависимость удельной вяакости полимеров различного строения (жесткости) от концентрации мономеров при синтезе в растворе [35]:
i — поли-4,4'-дифенилтерефталамид;
2 — поли-п-фенилентерефталамид; з—по-
ли-.«-фенилентерефталамид; 4 — поли-
м -фениле) (изофталамид.
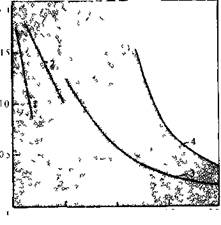
О 0,5 1,0 1,5- 2,0
Содержание мономеров, моль/л
Одной из главных причин нестабильности растворов полимеров является процесс упорядочения макромолекул в растворе. Чем бо-дее упорядочены макромолекулы в растворе, тем быстрее происходит их выделение (выпадение). Степень упорядоченности макромолекул в растворе можно выразить через общее число конформаций Q независимых друг от друга цепей: чем меньше Q, тем более упорядочены макромолекулы в растворе. Общее число конформаций макромолекул в растворе связано с молекулярной массой полимера, его жесткостью и концентрацией раствора соотношением [34]:
Q = (<oe-v)V"
где и — число возможных конформаций одного звена (гибкость цепи); V—ооъ-емная доля полимера ь растворе (его концентрация); п — число звеньев цепи (молекулярная масса); N — число независимых друг от друга цепей.
Из этого уравнения следует, что степень упорядоченности возрастает (Q уменьшается) при увеличении концентрации полимера (V —>1) и при уменьшении гибкостимакромолекулы (ш-^е).
Таким образом, чем более.жесткой является полимерная цепь, тем при более низких" концентрациях полимера он будет получаться высокомолекулярным. Эта зависимость четко прослеживается на практике. Например, из рис. 5.25 видно, что чем больше в полимерах пара-ароматических структур, придающих ему повышенную жесткость, тем при более низких концентрациях они получаются высокомолекулярными.
На основании этих положений можно объяснить, а иногда и предсказать влияние условий синтеза на структуру получающегося полимера.
Рис. 5.26 иллюстрирует влияние некоторых условий синтеза на структуру получающегося ароматического полиамида: в зависимости от температуры и концентрации исходных мономеров можно
получить ароматический полиамид любой заданной степени упорядоченности.
Изложенные выше соображения о закономерностях поликонденсации, сопровождаемой самопроизвольным выделением полимера из реакционной среды, позволяют выбрать (и в некоторых случаях прогнозировать) оптимальные условия синтеза различных полимеров.
Некоторые авторы, однако, по-иному трактуют закономерности поликонденсации, сопровождаемой выпадением полимера из раствора.
Согласно работам [18, 36], самопроизвольное выделение полимера из реакционной среды, например при добавлении высадителя, может привести к повышению молекулярной массы полимера (рис. 5.27).
При этом, как отмечают авторы, не наблюдается увеличения растворимости полимера (что может иногда быть), а увеличение молекулярной массы происходит вследствие выделения полимерной фазы.
Согласно [18], в ряде случаев выпадение полимера в процессе синтеза может способствовать получению высокомолекулярного продукта за счет сворачивания макромолекул при выпадении и увеличения таким образом локальной концентрации концевых групп. Думается, что нужны дополнительные эксперименты, подтверждающие эту точку зрения.
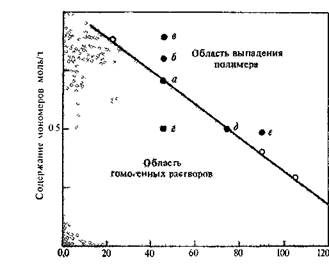
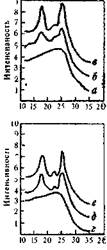
РИС. 5.26. Взаимосвязь кристалличности ароматического полиамида на основе о-толидива н днфторапгидрида изофталевой кислоты с концентрацией мономеров и температурой [S(|.
"Г
РИС. 5.27. Зависимость приведенной вязкости по.чиа|1нлата на основе терефта-левой кислоты фенолфталеина от содержания ацетона в смеси с дихлорэтаном • трнэтиламином [18]. Пунктиром показана граница выпадения полимера при синтезе.
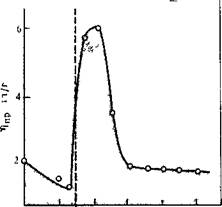
20 I 40 60 80 100 Содержание ацетона, % (об.)
В работе [36] отмечалось, что при введении осадителя в ходе поликонденсации ароматических полиэфиров также происходило увеличение молекулярной массы образующегося полимера. Автор объясняет это сдвигом поликонденсационного равновесия за счет вывода одного из продуктов реакции. Однако эта точка зрения не кажется убедительной, так как имеющийся экспериментальный материал относится к необратимым процессам поликонденсации.
При обсуждении данных этих экспериментов необходимо иметь в виду, что при выпадении полимера из реакционной среды может происходить также самопроизвольное фракционирование, т. е. из раствора будут выпадать высокомолекулярные фракции, а низкомолекулярные будут оставаться в растворе. Поэтому при анализе полученных результатов следует определять среднюю молекулярную массу всего продукта, а не только выделившегося из осаждения.
Таким образом, поликонденсация, сопровождаемая самопроизвольным выделением (выпадением) полимера из реакционной среды, является достаточно сложным вариантом поликонденсации в растворе. Этот процесс имеет и большое промышленное значение, поскольку позволяет получать ряд важных в практическом отношении полимеров с__пониженной растворимостью, в том числе термостойких.
5.6. Технологические особенности поликонденсации в растворе
Поликонденсация в растворе* в настоящее время широко используется в промышленности для получения большого числа полимеров. Кроме создания благоприятных условий для получения
* Этот способ называется также лаковым.
высокомолекулярных полнмероп этот метод имеет ряд технологических преимуществ.
В первую очередь необходимо отметить хорошие условия отвода тепла реакции вследствие разбавления мономеров, что, в свою очередь, позволяет избежать протекания некоторых побочных процессов, развиваемых при повышенных температурах (см. гл. 4). Поликонденсация в растворе протекает значительно быстрее, чем поликонденсация в расплаве и тем более в твердой фазе. Поэтому, несмотря на то что при поликонденсации в растворе мономеры применяются не в очень больших концентрациях, этот способ поликонденсации является довольно высокопроизводительным.
В некоторых случаях получаемый по этому методу раствор полимера можно использовать для непосредственной переработки. Так, реакционные растворы полиамидокислот, получающиеся при поликонденсации диаминов с диангидридами используются без какой-либо дополнительной обработки для получения пленок, покрытий, лаков. Иногда реакционные растворы перед использованием подвергаются нейтрализации (
 2015-05-26
2015-05-26 2009
2009






