Отчёт по лабораторной работе № 6.
По дисциплине: Физическая химия
(наименование учебной дисциплины согласно учебному плану)
Тема: Приготовление буферного раствора
Выполнил: студент гр. АПМ-03 ______________ / Бекурин К.В. /
(подпись) (Ф.И.О.)
ПРОВЕРИЛ:
Доцент: ____________ /Иванов И.И./
(подпись) (Ф.И.О.)
Санкт-Петербург
2004 год
Цель работы: научиться выбирать состав буферного раствора с заданным значением pH, рассчитывать количества компонентов, необходимые для приготовления буферного раствора. Познакомиться с понятием ёмкости буферного раствора и научиться её определять. Освоить современные методы измерения водородного показателя растворов с помощью pH-метров.
Оборудование и реактивы:
-pH-метр;
- гидроксид Na для титрования, 0,05 М раствор;
- фенолфталеин;
- уксусная кислота, 0,2 М раствор;
- ацетат Na, 0,2 М раствор;
- коническая колба для титрования объёмом 100 мл;
- мерные цилиндры объёмом 100 мл и объёмом 50 мл;
- пипетка Мора объёмом 5 мл;
- бюретка объёмом 25 мл.
Задание
Приготовить буферный раствор с pH=4,5. Рассчитать его буферную емкость.
Ход работы
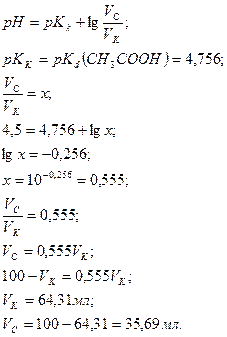
Получили буферный раствор, состоящий из 64,31мл CH3COOH 0,2 M и 35,69мл CH3COONa 0,2 M. С помощью pH-метра измеряем pH раствора: pH=4,9. Для уточнения результата воспользуемся индикаторной бумагой: pH=4,6. Следовательно, полученный раствор соответствует условию задачи.
Для полученного ацетатного буфера рассчитаем емкость по щелочи методом титрования. Для титрования используем раствор NaOH 0,05 M. Отбираем на 5мл аликвоту буферного раствора и помещаем в коническую колбу для титрования. Добавляем 4 капли фенолфталеина. Затем с помощью пипетки Мора начинаем добавлять в колбу раствор NaOH 0,5 M до тех пор, пока окраска индикатора не станет розовой. Данную процедуру повторяем 3 раза:
1. 14,1мл NaOH 0,5 M;
2. 13,5мл NaOH 0,5 M;
3. 14,0мл NaOH 0,5 M.
Получили, что для титрования 5мл приготовленного ацетатного буфера в среднем требуется 13,8мл NaOH 0,5 M.
Рассчитаем буферную емкость по щелочи:
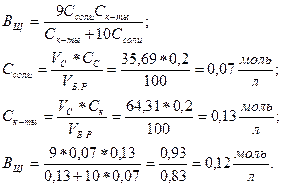
Теперь определим экспериментальное значение буферной ёмкости, которое рассчитаем по уравнению:
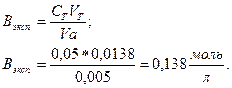
Вывод: в ходе работы мною был приготовлен буферный раствор, состоящий из 64,31мл CH3COOH 0,2 M и 35,69мл CH3COONa 0,2 M, pH которого 4,6, что незначительно отличается от заданного преподавателем 4,5. Следовательно, расчеты объемов составляющих этот буферный раствор компонентов были выполнены правильно. Это подтверждает и вычисленное значение буферной емкости по щелочи 0,12моль/л.
 2015-06-14
2015-06-14 295
295






