В природе в коллоидном состоянии широко распространены сульфидные руды многих элементов (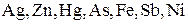 ).
).
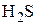 – важнейший стабилизатор коллоидных частиц сернистых минералов, может диссоциировать по двум стадиям:
– важнейший стабилизатор коллоидных частиц сернистых минералов, может диссоциировать по двум стадиям:
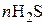

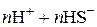

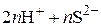 .
.
Показано, что устойчивость коллоидных растворов, стабилизированных 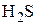 зависит от присутствия кислорода воздуха. Так, при хранении золя сульфида ртути без воздуха ее устойчивость возрастает, что, по-видимому, объясняется изменением состава мицеллы:
зависит от присутствия кислорода воздуха. Так, при хранении золя сульфида ртути без воздуха ее устойчивость возрастает, что, по-видимому, объясняется изменением состава мицеллы:
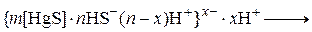
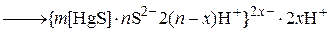 .
.
При этом потенциалопределяющими ионами являются в первом случае 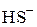 , во втором –
, во втором – 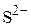 .
.
Коллоидный карбонат кальция в природе не устойчив и сравнительно быстро переходит в метаколлоидные формы. Предположив, что 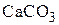 образуется при обменной реакции:
образуется при обменной реакции:
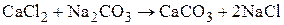 .
.
Вероятное строение мицеллы можно представить следующим образом:
· при избытке 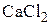 :
:
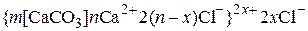 ,
,
· при избытке 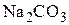 :
:
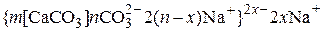 .
.
Золь сульфата бария образуется в природе при взаимодействии растворимых соединений бария с растворимыми сульфатами. Заряд коллоидной частицы обычно отрицателен:
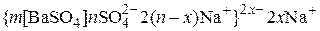 ,
,
стабилизатор: 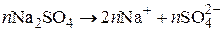 .
.
Щелочные метасиликаты при гидролизе
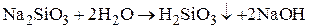
образуют устойчивые золи кремниевой кислоты, которые в щелочных растворах имеют отрицательный заряд:
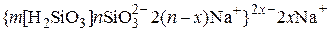 ,
,
стабилизатор: 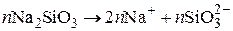 .
.
Возникновение двойного электрического слоя на поверхности ионностабилизированных частиц сообщает им электрический заряд. Последний может возникать также за счет диссоциации собственных частиц ионогенных групп.
Например, гидроксид алюминия, образующийся при обменных и гидролитических реакциях, легко пептизируется, т.к. на поверхности частиц возможна диссоциация по кислотному или основному типу в зависимости от рН грунтовых вод:
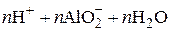

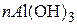

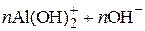 ,
,
поэтому строение мицеллы определяет рН среды:
· при рН < 7
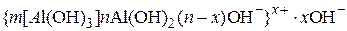 ;
;
· при рН > 8,1
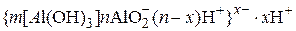 ;
;
· при 7 ≤ рН ≤ 8,1
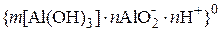 ,
,
значение электрокинетического потенциала равно нулю.
Другим примером является золь кремнезема на поверхности частиц 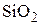 , построенных из
, построенных из 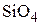 -тетраэдров при взаимодействии с водой, когда образуются силанольные группы:
-тетраэдров при взаимодействии с водой, когда образуются силанольные группы:
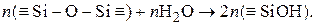
Возникшее поверхностное соединение – поликремнекислота – способно к частичной диссоциации по кислотному типу:
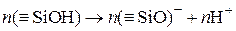 .
.
Мицелла может быть представлена:
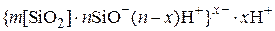 .
.
Вопросы и задания для самоконтроля
1. Что является причиной электрокинетических явлений?
2. Каким образом образуется двойной электрический слой?
3. Перечислите и охарактеризуйте основные теории строения ДЭС.
4. Что такое электрокинетический потенциал и где он возникает?
5. Каким образом можно количественно рассчитать величину электрокинетического потенциала?
6. Каково строение коллоидных мицелл?
7. Приведите примеры мицелл гидрофобных золей в природе.
Глава 5
УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ
ЛИОФОБНЫХ ДИСПЕРСНЫХ СИСТЕМ
 2015-06-05
2015-06-05 4556
4556
