Обладает основными свойствами. Выражены в разной степени. Электронная плотность азота в 1-ом положении оттянута на фенильный радикал и рядом стоящую карбонильную группу, поэтому основных свойств азот в 1-ом положении не проявляет (не протонируется даже уксусным ангидридом). Во 2-ом положении - слабовыраженные основные свойства.
Анальгин - соль сильной кислоты и сильного основания - рН = 6-7,5. Значения рН - обязательный показатель качества для эти соединений.
Анальгин - соль Þ основные свойства выражены слабо.
На атом азота – реакция с общеалколоидными осадительными реактивами.
Реакции окисления-восстановления
с FeCl3 анальгин даёт синий, переходящий в зеленый, желтый и, наконец, обесцвечивается со временем.
с AgNO3 - окисляется практически мгновенно - осадок свободного серебра (сероватый).
с NaNO2 в кислой среде анальгин окисляется. Продукты реакции нестабильны, меняется окраска во времени как с хлоридом железа.
Для анальгина - используются окислители - гексацианоферрат калия
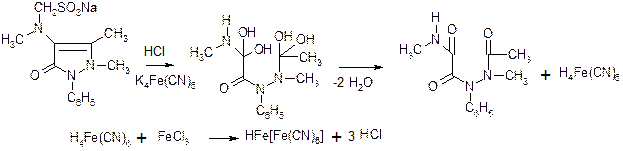 берлинская лазурь.
берлинская лазурь.
Фармакопейная реакция на анальгин - с KJO3 - образуется комплексная соль:
KJO3 ® KJ/J2 (реактив Люголя) - образуется бурый осадок + продукты окисления анальгина.
 2015-06-28
2015-06-28 3814
3814








