Соли диазония в определенных условиях реагируют с некоторыми ароматическими соединениями с образованием азосоединений Ar–N=N–Ar, в которых группа – N2 – соединена с двумя углеводородными радикалами. Эти реакции называются реакциями азосочетания.
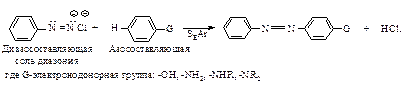
Замещение обычно протекает в п -положение, если оно занято, сочетание происходит в о -положение.
Механизм реакции – электрофильное замещение SEAr. Электрофильным агентом является ион диазония, очень слабый электрофил.
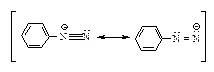
Такой слабый электрофил атакует только очень реакционноспособные кольца, содержащие сильные электронодонорные группы G.
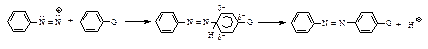
Сочетание с фенолами ведется в слабощелочной среде, при пониженной температуре. Фенол обладает заметно кислыми свойствами, в водном растворе он существует в равновесии с феноксид-ионом.
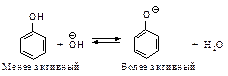
Наличие полного отрицательного заряда делает заместитель бóльшим донором электронов. Чем больше щелочность среды, тем выше содержание феноксид-иона, тем выше скорость азосочетания. С другой стороны, в присутствии ОНy ион диазония существует в равновесии с неионизированным соединением. Это значит, что реакции азосочетания будет благоприятствовать низкая концентрация гидроксид-иона, т.е. кислая среда.
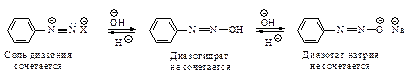
Условия, при которых протекает реакция сочетания с фенолами, являются компромиссными: раствор должен быть настолько слабо щелочным, чтобы концентрация диазотат-иона не стала слишком высокой, и настолько сильно щелочным, чтобы концентрация феноксид-иона была достаточной для успешного протекания реакции, т.е. поддерживается слабощелочная среда.
Сочетание с аминами. Высокая кислотность среды способствует тому, что диазосоединение полностью находится в виде диазокатиона. Но чем выше кислотность, тем выше доля амина в виде иона аммония, который не активен в реакциях электрофильного замещения. Поэтому среда должна быть слабокислой, чтобы достаточное количество амина было в свободном состоянии.
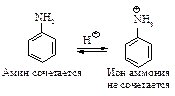
Примеры:
 2015-06-24
2015-06-24 1998
1998
