| Название, формула | Тпл., оС | Ткип., оС | Ка∙105 |
| Пировиноградная СН3СОСООН | 165 (разл.) | ||
| Ацетоуксусная СН3СОСН2СООН | - | 100 (разл) | |
| Левулиновая СН3СОСН2СН2СООН | 2,3 |
Кетокислота ведет себя как кетон и как кислота. По карбонильной группе кетокислоты вступают в реакции нуклеофильного присоединения, гидрирования, по карбоксильной группе дают производные карбоновых кислот. Но кроме свойств индивидуальных функциональных групп, кетокислоты обладают особыми свойствами, которые обусловлены определенным взаимным расположением функциональных групп. К таким свойствам относится, например, повышенная кислотность a-водородов в b-кетокислотах; на этом свойстве основаны синтезы с помощью ацетоуксусного эфира.
Синтез кетонов и кислот с помощью ацетоуксусного эфира. В b-кетокислотах a-углеродный атом связан с двумя электроноакцепторными группами, вследствие этого a-водород обладает значительно большей кислотностью по сравнению с кислотностью a-водородного атома обычных эфиров.
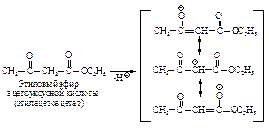
Образующийся анион обладает высокой устойчивостью (Ка a-водорода в водном растворе составляет 10-11) вследствие того, что кислороды двух карбонильных групп участвуют в распределении отрицательного заряда.
Анионы сложных эфиров, подобных этилацетоацетату, могут быть проалкилированы. Эти реакции имеют важное значение для синтеза кетонов и карбоновых кислот.
Ацетоуксусный эфир (I) действием этоксида натрия превращается в натрацетоуксусный эфир (II), который вводится в реакцию с алкилгалогенидом. Удовлетворительные результаты достигаются при использовании первичных галогеналканов. Продукт моноалкилирования – моноалкилацетоуксусный эфир (III), содержит еще один кислый водород, который также может отщепляться под действием основания, а полученный анион может снова алкилироваться. При этом образуется диалкилацетоуксусный эфир (IV). Все реакции проводятся в абсолютном этиловом спирте.
При гидролизе разбавленным водным раствором кислоты моно- или диалкилацетоуксусные эфиры превращаются в кислоты, которые при нагревании легко декарбоксилируются, в результате образуются метилалкилкетоны (V, VI).
Под действием концентрированной щелочи происходит реакция, обратная конденсации Кляйзена (см. п. 7.1.3), и моно- или диалкилацетоуксусные эфиры расщепляются с образованием уксусной кислоты и моно- или диалкилзамещенных уксусных кислот (VII, VIII).
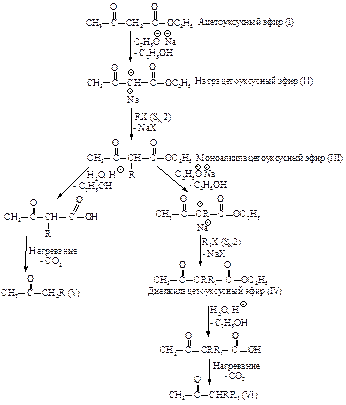
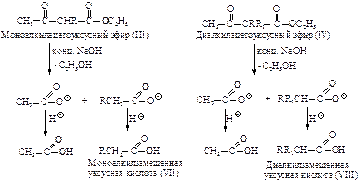
Получение ацетоуксусного эфира описано в п. 7.1.3.
 2015-06-24
2015-06-24 1081
1081








