Экспериментальное изучение скорости прямой реакции показывает
Механизм реакции известен:
Скорость прямой реакции по этому механизму соответствует опытной скорости. Создаётся впечатление, что два опытных факта -
постоянство отношения
другу. Понять, что противоречия здесь нет, позволяет принцип детального равновесия.
В условиях равновесия каждому прямому процессу должен соответствовать обратный, идущий с той же скоростью. Поэтому в равновесии каждую из приведённых реакций нужно записать как обратимую:
1)
2)
3)
Видно, что сумма реакций 2) и 3) даёт исходную реакцию и, следовательно,
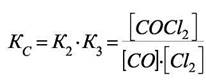
Это выражение полностью соответствует формуле (7.30). Механизм образования 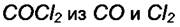 мог бы быть и другим, но выражение
мог бы быть и другим, но выражение
для КС останется тем же. Вид его не зависит от кинетики, так как в равновесной системе выполняется принцип детального равновесия, т.е. каждому прямому процессу соответствует обратный, идущий с той же скоростью.
Допустим, например, что фосген образуется так
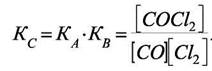
Таким образом, можно сделать вывод, что выражение для константы равновесия не зависит от кинетического механизма химического превращения.
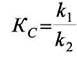
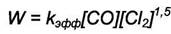
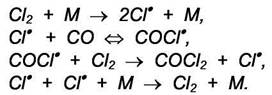
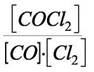
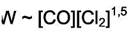
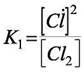
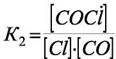
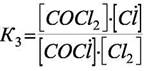
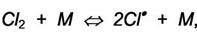
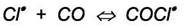
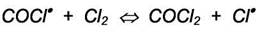
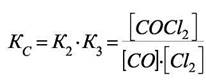
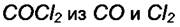 мог бы быть и другим, но выражение
мог бы быть и другим, но выражение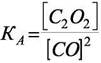
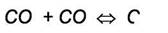
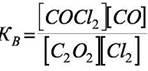
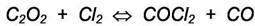
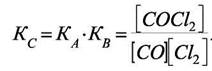
 2015-07-04
2015-07-04 356
356








