В пробирку поместите 5 мл раствора хлорида железа (III) – FeCl3 и столько же гидроксида натрия – NaOH. Образуется осадок.
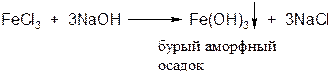 |
Разделите полученный осадок на две пробирки. В первую пробирку прибавьте 2 мл серной кислоты (H2SO4) а во вторую пробирку добавить 2 мл раствора гидроксида натрия (NaOH).
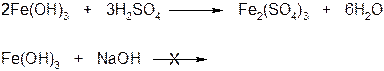
Вывод: гидроксид железа проявляет основные свойства – реагирует только с кислотами.
Опыт №3.
Амфотерные оксиды и гидроксиды. Отношение гидроксидов к кислотам и щелочам.
К 5 мл раствора соли алюминия прибавьте 5 мл раствора гидроксида натрия. Образуется белый студенистый осадок.

Разделите полученный осадок на две пробирки. В первую пробирку прибавьте 2 мл соляной кислоты (HСL) а во вторую пробирку прибавить 2 мл раствора гидроксида натрия (NaOH).
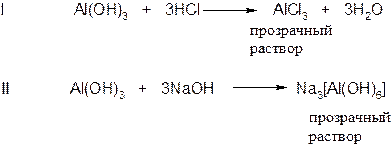
Вывод: гидроксид алюминия проявляет амфотерные свойства и взаимодействует как с кислотами, так и с основаниями.
 2015-07-14
2015-07-14 1200
1200








