Помимо чужеродных соединений, загрязняющих пищевые продукты, так называемых контаминантов-загрязнителей, и природных токсикантов, необходимо учитывать действие веществ, не обладающих общей
| токсичностью, но способных избирательно ухудшать или блокировать усвоение нутриентов. Эти соединения принято называть антиалиментарными факторами питания. Этоттерминраспространяется только на вещества природного происхождения, которые являются составными частями натуральных продуктов питания. Перечень антиалиментарных факторов питания достаточно обширен. Остановимся на рассмотрении некоторых из них. Ингибиторы пищеварительных ферментов.К этой группе относятся вещества белковой природы, блокирующие активность пищеварительных ферментов (пепсин, трипсин, химотрипсин, α-амилаза). Белковые ингибиторы обнаружены в семенах бобовых культур (соя, фасоль и др.), злаковых (пшеница, ячмень и др.), в картофеле, яичном белке и других продуктах растительного и животного происхождения. Механизм действия этих соединений заключается в образовании стойких комплексов «фермент-ингибитор», подавлении активности главных пищеварительных ферментов и, тем самым, снижении усвоения белковых веществ и других макронутриентов. К настоящему времени белковые ингибиторы достаточно хорошо изучены и подробно охарактеризованы: расшифрована первичная структура, изучено строение активных центров ингибиторов, исследован механизм действия ингибиторов и т. п. На основании структурного сходства все белки-ингибиторы растительного происхождения можно разделить на несколько групп, основными из которых являются следующие. 1. Семейство соевого ингибитора трипсина (ингибитора Кунитца). 2. Семейство соевого ингибитора Баумана—Бирка. 3. Семейство картофельного ингибитора I. 4. Семейство картофельного ингибитора II. 5. Семейство ингибиторов трипсина/α-амилазы. Ингибитор Кунитца был впервые выделен из семян сои еще в 1946 г. Его молекулярная масса 20 100 Да. Молекула ингибитора состоит из 181 аминокислотного остатка и содержит две дисульфидные связи в положении цис(39) — цис(86) и цис(136) — цис(145). Трипсиносвязывающий реактивный центр включает остаток аргинина, связанный пептидной связью с остатком изолейцина: арг(63) — иле(64), поэтому ингибиторы этого семейства также называют трипсиновыми ингибиторами аргини-нового типа. Ингибитор Баумана—Бирка был впервые выделен также в 1946 г. из семян сои. Ингибитор эффективно подавляет активность трипсина и хи-мотрипсина, причем с одной молекулой ингибитора могут связываться молекулы обоих ферментов. Ингибитор Баумана—Бирка — первый описанный «двухглавый» (или двухцентровой) ингибитор сериновых проте- |
 |
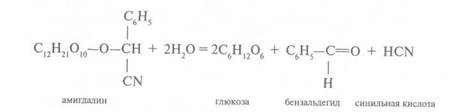 |
 |
Его молекулярная масса примерно 8000 дальтон. Молекула ингибитора состоит из 71 аминокислотного остатка. Особенностью аминокислотного состава является высокое содержание остатков цистеина (7 на одну молекулу) и отсутствие остатков глицина и триптофана. Обращает на себя внимание, что молекула ингибитора Баумана—Бирка состоит из двух частей, сходных по структуре (доменов), которые соединены между собой короткими полипептидными цепочками. Реактивный центр, ответственный за связывание трипсина, локализован в первом домене и содержит пептидную связь: лиз(16) — сер(17); а реактивный центр, ответственный за связывание химотрипсина, находится во втором домене и содержит пептидную связь: лей(43) — сер(44), поэтому ингибиторы этого семейства иногда называют ингибиторами лизинового типа.
В клубнях картофеля содержится целый набор ингибиторов химотрипсина и трипсина, которые отличаются по своим физико-химическим свойствам: молекулярной массе, особенностям аминокислотного состава, изоэлектрическим точкам, термо- и рН-стабильности и т. п. Кроме картофеля, белковые ингибиторы обнаружены в других пасленовых, а именно — в томатах, баклажанах, табаке. Наряду с ингибиторами сери-новых протеиназ в них обнаружены и белковые ингибиторы цистеино-вых, аспартильных протеиназ, а также металлоэкзопептидаз.
Заслуживает внимания и тот факт, что в семенах растений и в клубнях картофеля находятся «двухглавые» ингибиторы, способные одновременно связываться и ингибировать протеазу и α-амилазу. Такие белковые ингибиторы были выделены из риса, ячменя, пшеницы, тритикале, ржи.
Рассматриваемые белковые ингибиторы растительного происхождения характеризуются высокой термостабильностью, что в целом не характерно для веществ белковой природы. Например, полное разрушение соевого ингибитора трипсина достигается лишь 20 минутным автоклавированием при 115°С, или кипячением соевых бобов в течение 2—3 ч. Из этого следует, что употребление семян бобовых культур, особенно богатых белковыми ингибиторами пищеварительных ферментов, как для корма сельскохозяйственных животных, так и в пищевом рационе человека, возможно лишь после соответствующей тепловой обработки.
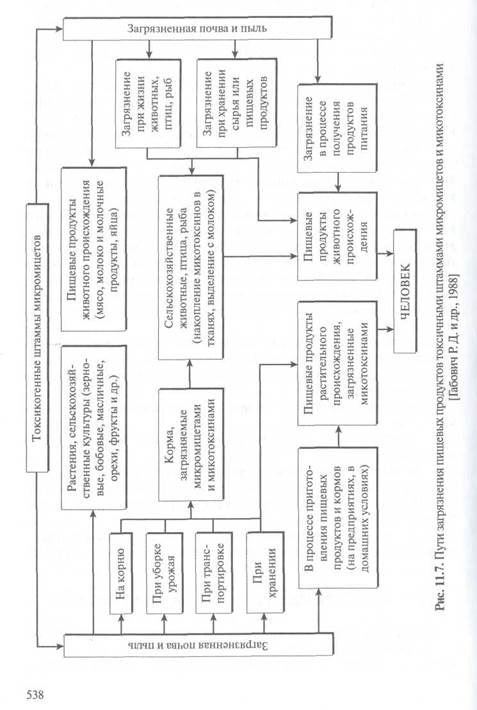
Цианогенные гликозиды. Цианогенные гликозиды — это гликозиды некоторых цианогенных альдегидов и кетонов, которые при ферментативном или кислотном гидролизе выделяют синильную кислоту — HCN, вызывающую поражение нервной системы.
Из представителей цианогенных гликозидов целесообразно отметить лимарин, содержащийся в белой фасоли, и амигдалин, который обнаруживается в косточках миндаля (до 8%), персиков, слив, абрикос (от 4 до 6%).
| Биогенные амины.К соединениям этой группы относятся серотонин, тирамин, гистамин. |
Амигдалин представляет собой сочетание дисахарида гентиобио-зы и агликона, включающего остаток синильной кислоты и бензаль-дегида.
Серотонин, главным образом, содержится во фруктах и овощах. Например, содержание серотонина в томатах — 12 мг/кг; в сливе — до 10 мг/кг. Тирамин чаще всего обнаруживается в ферментированных продуктах, например в сыре до 1100 мг/кг. Содержание гистамина коррелирует с содержанием тирамина в сыре от 10 до 2500 мг/кг. В количествах более 100 мг/кг гистамин может представлять угрозу для здоровья человека.
Алкалоиды. Алкалоиды — весьма обширный класс органических соединений, оказывающих самое различное действие на организм человека. Это и сильнейшие яды, и полезные лекарственные средства. Печально известный наркотик, сильнейший галлюциноген — ЛСД — диэтил-амид лизергиловой кислоты, был выделен из спорыньи, грибка, растущего на ржи, в 1943 г. швейцарским химиком А. Гофманом.
С 1806 г. известен морфин, он выделен из сока головок мака и является очень хорошим обезболивающим средством, благодаря чему нашел применение в медицине, однако при длительном употреблении приводит к развитию наркомании.
Хорошо изучены в настоящее время так называемые пуриновые алкалоиды, к которым относятся кофеин и часто сопровождающие его теобромин и теофиллин. Структурные формулы кофеина, теобромина и тео-филлина представлены ниже.
 |
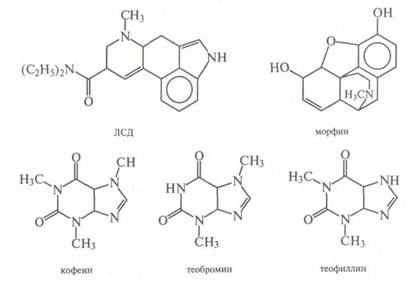
Содержание кофеина в сырье и различных продуктах колеблется в достаточно широких пределах. В зернах кофе и листьях чая, в зависимости от вида сырья, от 1 до 4%; в напитках кофе и чая, в зависимости от способа приготовления, до 1500 мг/л (кофе) и до 350 мг/л (чай). В напитках пепси-кола и кока-кола до 1000 мг/л и выше. Здесь уместно подчеркнуть, что пуриновые алкалоиды при систематическом употреблении их на уровне 1000 мг в день вызывают у человека постоянную потребность в них, напоминающую алкогольную зависимость.
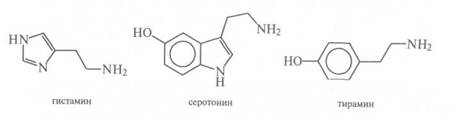
К группе стероидных алкалоидов будут относится соланины и чакони-ны, содержащиеся в картофеле. Иначе их называют гликоалкалоидами, они содержат один и тот же агликон (соланидин), но различные остатки сахаров. В картофеле обнаружены шесть гликоалкалоидов, одним из которых является α-соланин.
Особенности состава других гликоалкалоидов картофеля видны из сопоставления их структурных компонентов:
α-соланин.... соланидин + галактоза + глюкоза + рамноза; β-соланин.... соланидин + галактоза + глюкоза;
γ-соланин........ соланидин + галактоза;
α-чаконин.... соланидин + глюкоза + рамноза + рамноза;
β-чаконин ……соланидин + глюкоза + рамноза;
γ-чаконин........ соланидин + глюкоза;
Таким образом, гликоалкалоиды картофеля весьма близки по составу и являются промежуточными продуктами при биосинтезе α -соланина. Это вещества средней токсичности, их накопление в клубнях картофеля (в позеленевших частях клубня их количество может увеличиваться более чем в 10 раз и достигать 500 мг/кг), придает горький вкус и вызывает типичные признаки отравления. Эти соединения обладают антихолин-эстеразной активностью.
Соланины и чаконины могут содержаться в баклажанах, томатах, табаке.
Антивитамины. Согласно современным представлениям, к антивитаминам относят две группы соединений.
1-я группа — соединения, являющиеся химическими аналогами витаминов, с замещением какой-либо функционально важной группы на неактивный радикал, т. е. это частный случай классических антиметаболитов.
2-я группа — соединения, тем или иным образом специфически инак-тивирующие витамины, например с помощью их модификации, или ограничивающие их биологическую активность.
Если классифицировать антивитамины по характеру действия, как это принято в биохимии, то первая (антиметаболитная) группа может рассматриваться в качестве конкурентных ингибиторов, а вторая — неконкурентных, причем во вторую группу попадают весьма разнообразные по своей химической природе соединения и даже сами витамины, способные в ряде случаев ограничивать действие друг друга.
Рассмотрим некоторые конкретные примеры соединений, имеющих ярко выраженную антивитаминную активность.
Лейцин — нарушает обмен триптофана, в результате чего блокируется образование из триптофана ниацина — одного из важнейших водорастворимых витаминов — витамина PP.
Индолилуксусная кислота и ацетилпиридин — также являются антивитаминами по отношению к витамину РР; содержатся в кукурузе. Чрезмерное употребление продуктов, содержащих вышеуказанные соединения, может усиливать развитие пеллагры, обусловленной дефицитом витамина PP.
Аскорбатоксидаза и некоторые другие окислительные ферменты проявляют антивитаминную активность по отношению к витамину С. Аско-батоксидаза (Н. Ф. 1.10.3.3) катализирует реакцию окисления аскорбиновой кислоты в дегидроаскорбиновую кислоту:
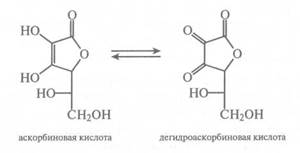
Содержание аскорбатоксидазы и ее активность в различных продуктах неодинакова: наиболее активна аскорбатоксидаза в огурцах, кабачках, наименее — в моркови, свекле, помидорах. При измельчении овощей за 6 часов хранения теряется более половины витамина С, т. к. измельчение способствует взаимодействию фермента и субстрата.
Тиаминаза (Н. Ф. 3.5.99.2) — антивитаминный фактор для витамина В1 — тиамина. Она содержится в продуктах растительного и животного происхождения, наибольшее содержание этого фермента отмечено у пресноводных и морских рыб, кроме того, тиаминаза продуцируется бактериями кишечного тракта — Вас. thiaminolytic и Вас. anekrinolytieny, что может являться причиной дефицита тиамина. Оршодифенояы и биофла-воноиды (вещества с Р-витаминной активностью), содержащиеся в кофе и чае, а также окситиамин, который образуется при длительном кипячении кислых ягод и фруктов, проявляют антивитаминную активность по отношению к тиамину.
Все это необходимо учитывать при употреблении, приготовлении и хранении пищевых продуктов.
Линатин — антагонист витамина В6, содержится в семенах льна. Кроме этого, ингибиторы пиродоксалевых ферментов обнаружены в съедобных грибах и некоторых видах семян бобовых.
Авидин — белковая фракция, содержащаяся в яичном белке, приводящая к дефициту биотина (витамина Н), за счет связывания и перевода его в неактивное состояние.
Гидрогенизированные жиры — являются факторами, снижающими сохранность витамина А (ретинола).
Говоря об антиалиментарных факторах питания, нельзя не сказать о гипервитаминозах. Известны два типа: гипервитаминоз А и гипервита-
миноз D. Например, печень северных морских животных несъедобна из-за большого содержания витамина А.
Приведенные выше данные свидетельствуют о необходимости дальнейшего тщательного изучения вопросов, связанных с взаимодействием различных природных компонентов пищевого сырья и продуктов питания, влияния на них различных способов технологической и кулинарной обработки, а также режимов и сроков хранения с целью снижения потерь ценных макро- и микронутриентов, и обеспечения рациональности и адекватности питания.
Факторы, снижающие усвоение минеральных веществ. К факторам, снижающим усвоение минеральных веществ, в первую очередь следует отнести щавелевую кислоту и ее соли (оксалаты), фитин (инозитолгекса-фосфорная кислота) и танины.
Наиболее изучена в этом плане щавелевая кислота:
ноос-соон
Продукты с высоким содержанием щавелевой кислоты способны приводить к серьезным нарушениям солевого обмена, необратимо связывать ионы кальция. Установлено, что интоксикация щавелевой кислотой проявляется в большей степени на фоне дефицита витамина D.
Известны случаи отравлений с летальным исходом, как от самой щавелевой кислоты (при фальсификации продуктов, в частности вин, когда подкисление проводили дешевой щавелевой кислотой), так и от избыточного потребления продуктов, содержащих ее в больших количествах. Смертельная доза для взрослых людей колеблется от 5 до 150 г и зависит от целого ряда факторов. Содержание щавелевой кислоты в среднем в некоторых растениях таково (в мг/100 г): шпинат—1000, ревень — 800, щавель — 500, красная свекла — 250.
 |
Фитин, благодаря своему химическому строению, легко образует труднорастворимые комплексы с ионами Са, Mg, Fe, Zn, и Сu. Этим объясняется его деминерализующий эффект.
Достаточно большое количество фитина содержится в злаковых и бобовых культурах: в пшенице, горохе, кукурузе его содержание примерно 400 мг/100 г продукта, причем основ-
ная часть сосредоточена в наружном слое зерна. Хлеб, выпеченный из муки высшего сорта, практически не содержит фитина. В хлебе из ржаной муки его мало, благодаря высокой активности фитазы, способной расщеплять фитин.
Дубильные вещества, кофеин, балластные соединения могут рассматриваться как факторы, снижающие усвоение минеральных веществ.
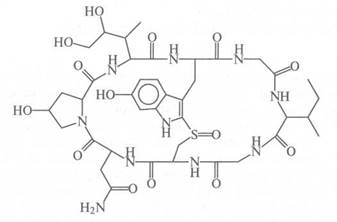
Яды пептидной природы. Интересным и важным является тот факт, что многие биологически активные вещества являются циклопептида-ми, т. е. имеют циклическое строение. К таким циклопептидам относятся антибиотики, гормоны и токсины. Было показано, что ядовитый гриб бледная поганка (Amanita phalloides) содержит не менее десяти токсичных циклопептидов. Их молекулярная масса около 1000; они содержат атом серы, принадлежащий к остатку цистеина, связанному с индоль-ным кольцом триптофана. Ниже представлена структура особенно ядовитого циклопептида бледной поганки α-аманитина:
Алкоголь. Алкоголь можно рассматривать как рафинированный продукт питания, который имеет только энергетическую ценность. При окислении 1 г этанола выделяется 7 ккал энергии; данная величина лежит между калорийностью углеводов и жиров. Алкоголь не является источником каких-либо пищевых веществ, поэтому его часто называют источником «холостых» калорий.
Попадая в организм человека, этанол под воздействием фермента — алкогольдегидрогеназы окисляется до ацетальдегида, согласно уравнению:
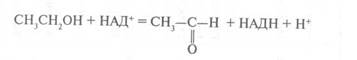
Далее ацетоальдегид под воздействием другого фермента — альдегид-дегидрогеназы окисляется до ацетата:
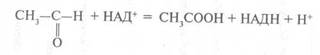
В результате этих двух реакций образуются две молекулы НАДН, которые служат донорами водорода в дыхательной цепи митохондрий. В ходе последующего переноса электронов к кислороду из АДФ и остатка фосфорной кислоты образуется 6 молекул АТФ. Образовавшийся из этанола ацетат в дальнейшем активируется и переходит в ацетил-кофермент А:
Из приведенной структуры видно, что сера цистеина, связываясь с остатком триптофана, разделяет циклопептид на два кольца. Подобная бициклическая структура свойственна всем циклопептидам бледной поганки.
Лектины. Лектины — группа веществ гликопротеидной природы с молекулярной массой от 60 до 120 тысяч дальтон. Они широко распространены в семенах и других частях растений. Лектины обнаружены в бобовых, арахисе, проростках растений, а также в икре рыб.
Лектины обладают способностью повышать проницаемость стенок кишечника для чужеродных веществ; нарушать всасывание нут-риентов; вызывать агглютинацию (склеивание) эритроцитов крови. С этим связано их негативное действие при высоких концентрациях (см. также раздел Белки). Некоторые лектины токсичны, например, лектин из семян клещевины (Ricinus communis) — рицин, а также лектины некоторых животных и микроорганизмов, в частности холерный токсин.
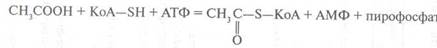
Образовавшийся ацетил-КоА, в свою очередь, может окисляться в цикле лимонной кислоты.
Алкоголь синтезируется ферментными системами организма для собственных нужд и в течение дня организм человека способен синтезировать от 1 до 9 г этилового спирта. Эндогенный алкоголь является естественным метаболитом, и ферментных мощностей организма вполне хватает для его окисления в энергетических целях. При потреблении алкоголя в больших количествах ферменты не справляются, происходит накопление этилового спирта и уксусного альдегида, что вызывает симптомы обширной интоксикации (головная боль, тошнота, аритмия сердечных сокращений). Таким образом, алкоголь можно рассматривать как антиалиментарный фактор питания, приводящий к специфическим нарушениям обмена веществ.
 |
 |
 |
 |
У людей, потребляющих большие количества алкоголя, обнаруживается дефицит незаменимых веществ. Примером могут служить тяжелые формы недостаточности витаминов у алкоголиков: алкогольные формы полиневрита, пеллагры, бери-бери и т. п., а также гипогликемия, т. к. этанол блокирует синтез глюкозы из лактата и аминокислот.
Хроническое потребление алкогольных напитков приводит не только к авитаминозам, но и к нарушению углеводного, жирового и белкового обмена и заканчивается, как правило, биохимической катастрофой с тяжелыми патологиями. Кроме того, совершенно очевидно, что алкоголь обладает наркотическим действием, вызывая устойчивую зависимость, которая приводит к негативным изменениям психики и, в конечном счете, к деградации личности.
В этом разделе приведены сведения о компонентах пищи, способных оказывать неблагоприятное воздействие на организм человека. Эти данные свидетельствуют о необходимости их учета при составлении рационов питания, при решении ряда технологических вопросов в производстве продуктов питания, а также при их кулинарной обработке.
В табл. 11.1 приведены антиалиментарные факторы питания и их основные источники, а также возможные пути устранения их негативного влияния.
 2015-09-06
2015-09-06 1207
1207








