Различают четыре способа дезаминирования аминокислот: 1. Восстановительное дезаминирование:
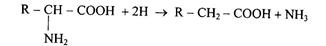
В результате образуется органическая кислота и аммиак.
2. Гидролитическое дезаминирование:
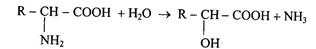
В результате реакции образуется оксикислота и аммиак.
Эти виды дезаминирования характерны для бактерий (преджелудка жвачных, толстого отдела кишечника других животных).
3. Внутримолекулярное дезаминирование:
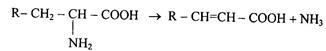
В результате образуется ненасыщенная органическая кислота и аммиак.
Такой вид дезаминирования характерен для бактерий, растений, а в животном организме дезаминируется гистидин. Под действием фермента гистидиндезаминазы происходит образование аммиака и урокиноновой кислоты.
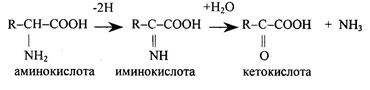
4. Окислительное дезаминирование:
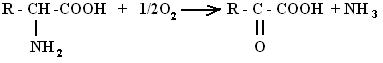
Это наиболее распространенная форма дезаминирования. Реакция происходит с участием ферментов, где акцептором водорода, как правило, является НАД, реже – ФМН. Она проходит в
две стадии. На первой стадии образуется неустойчивая иминокислота, во второй стадии с участием молекулы воды образуется аммиак и кетокислота:
В тканях организма важно дезаминирование Д-аминокислот, так как в белках содержатся только L-аминокислоты. Поэтому в организме весьма активна дегидрогеназа а-глутаминовой кислоты, которая превращает ее в а-кетоглутаревую кислоту.
Реакция весьма распространена. Глутаматдегидрогеназа играет решающую роль в процессах окислительного дезаминирования большинства аминокислот путем непрямого Дезаминирования.
Коферментом глутамат дегидрогеназы является НАД (НАДФ):
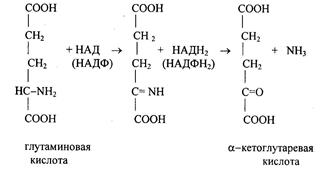
НАДН2 в дыхательной цепи митохондрий обеспечивает синтез трех молекул АТФ (печень, мышца, почки, мозг и т.д.).
 2015-10-16
2015-10-16 861
861








