ЛАБОРАТОРНАЯ РАБОТА
Исходные материалы (выдаются на стол): а) яичный белок,
б) белок мяса,
в) белок молока.
ОПЫТ №1. Отношение белков к кислотам и щелочам
Введение. Белки явл-ся коллоидными амфотерными электролитами, их основные св-ва обусловлены наличием аминного азота, а кислотные св-ва главным образом присутствием карбоксильных групп:
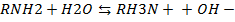
В большинстве случаев константа диссациации белка как кислоты слегка превышает конст. диссациации того же белка как основания, поэтому частица чистого белка в водном р-ре обычно заряжена отрицательно. При пост. подкислении такого р-ра степень кислотной диссациации белка снижается, а степень основной диссациации повышается. При достижении равенства конц. полож. и отриц. частиц белка коллоидный р-р белка оказывается наименее устойчивым и особенно легко коагулирует, т.е. свертывается. Отвечающая этой «изоионной» точке концентрация ионов водорода в р-ре является величиной, характерной для данного белка. Изоионные точки белков, применяемых в описанном опыте, лежат в пределах рН 4,5—6,5.
Добавление избытка к-ты, т.е. уменьшение рН ниже изоионной точки, резко усиливает диссациацию белков как основания, частицы белка заряжаются положительно, и коллоидный р-р белка снова делается более устойчивым. Наоборот, избыток щелочи повышает устойчивость отрицательно заряженных частиц белка.
Материалы:
· р-ры белков,
· уксусная кислота (конц.)
· сернокислый аммоний (16%-ный раствор)
· едкий натр (5-% р-р).
К 2-3 мл р-ра белка добавляют уксусную к-ту по каплям при встряхивании. Во всех р-рах наблюдается выпадение белка в осадок в виде мути или хлопьев. При дальнейшем добавлении к-ты осадок белка снова растворяется.
Полученный кислый р-р делят на две части. Одну из них нагревают до кипения, в отличие от исходного р-ра свертывание не наблюдается.
Добавление к горячей кислой жидкости 1-2 капель р-ра сульфата аммония вызывает свёртывание.
К другой части кислого р-ра белка осторожно добавляют р-р щелочи по каплям при встряхивании. При постепенной нейтрализации избытка к-ты образуется осадок белка, снова растворяющийся в избытке щелочи.
Добавив 1-2 мл р-ра щелочи, нагревают полученную щелочную жидкость до кипения, при этом свертывания белка не наблюдается.
Если р-р белка не слишком разбавлен, то при кипячении с избытком щелочи обнаруживается отщепление аммиака и сероводорода.
ОПЫТ №2. Высаливание белков из растворов.
Введение. Соли щелочных металлов и магния при достаточно высокой темп. их конц. осаждают – «высаливают» - многие белки из р-ров. Причинами высаливания белков являются как снятие электрического заряда коллоид. частиц белка адсорбирующимися на них противоположно заряженными ионами соли, так и снятие водных оболочек с гидрофильных частиц белка сильно гидратирующимися ионами добавленной в большом кол-ве соли.
Оба указанных фактора уменьшают устойчивость коллоидного р-ра, так как облегчают слипание и укрупнение (коагуляцию) частиц белка, и последний выпадает в осадок.
Сернокислый аммоний обладает особенно резко выраженной высаливающей способностью и осаждает белки как в слабо кислой, так и в нейтр. среде.
В случае др. солей, например, хлоридов и сульфатов натрия и магния, для полноты высаливания требуется подкисление р-ра при применении сернокислого аммония легкое окисление также резко усиливает высаливание.
Различные белки высаливаются с неодинаковой легкостью. При добавлении к р-ру белка равного объема насыщенного р-ра сульфата аммония в жидкости получается вдвое меньшая концентрация его. В такой «полунасыщенном» р-ре этой соли глобулины выпадают в осадок и могут быть отделены от остающихся в р-ре альбуминов. В насыщенном р-ре сульфат аммония высаливает и альбумины.
Осаждение белков солями щелочных металлов и магния не сопровождается денатурацией, т.е. изменением структуры молекулы белка, поэтому такое осаждение-высаливание – обратимо, и полученные осадки при добавлении воды снова переходят в р-р.
Материалы:
· р-ры белков,
· сернокислый аммоний (насыщенный примерно 43%-ный р-р)
· сернокислый аммоний (тв.)
К 3-4 мл р-ра белка добавляют равный объем насыщ. р-ра сернокислого аммония и слегка встряхивают смесь. Появляется муть или хлопья выпадающих в осадок глобулинов. Отлив около 1 мл мутной жидкости в отдельную пробирку, добавляют в неё 2-3 мл воды, при встряхивании осадок белка снова растворяется.
Главную часть полученной мутной жидкости фильтруют через сухой складчатый фильтр. Прозрачный фильтрат делят на две части. Одну часть фильтрата нагревают до кипения и наблюдают свертывание находящегося в р-ре белка, который выделяется в виде хлопьев или мути. К другой части фильтрата добавляют при легком встряхивании 1-2 г сернокислого аммония в порошке до прекращения его растворения. При этом в жидкости над небольшим осадком избытка кристаллов соли появляется муть или хлопья высоленного белка. При последующем добавлении двойного объёма воды выделившийся осадок снова растворяется.
Р-р миозина почти не содержит альбумидов, поэтому опыт с ним заканчивают на стадии образования сгустка белка при добавлении р-ра сульфата аммония (насыщ.), при последующем добавлении воды высоленный миозин растворяется плохо.
ОПЫТ №3. Свертывание белков при нагревании.
Введение. Осаждение белка в результате свертывания необратимо, и полученные осадки уже нерастворимы ни в воде, ни в растворах солей. Свертывания белка при кипячении обусловенно способностью крупных белковых молекул изменять структуру – «денатурироваться» - при 80-100 ↄС. При последовательном расщеплении молекулы белка, например, при его гидролизе, способность белка свертываться постепенно ослабевает вплоть до полного исчезновения. Пептоны и альбумозы так же, как и некоторые наиболее распространенные белки, например, желатина не свертываются при кипячении их р-ров.
Материалы:
· р-ры белков,
· сернокислый аммоний (16%-ный р-р)
· уксусная к-та (конц.)
· едкий натр (10%-ный р-р)
В пробирку наливают 2-3 мл р-ра исследуемого белка и нагревают до кипения. Большинство белков при этом выпадает в осадок в виде мути или хлопьев. Затем слегка охлаждают жидкость, делят её на две части и добавляют к одной из них 1-2 капли уксусной кислоты, а к другой - 1-2 капли сернокислого аммония. Снова нагревают обе смеси до кипения, при этом в обеих пробирках кол-во свернувшегося белка значительно увеличивается.
ОПЫТ №4. Осаждение белков солями тяжелых металлов.
Введение. Соли тяжелых металлов уже в очень малых конц. осаждают белки, образуя с ними нерастворимые в воде солеобразные соединения. Поэтому белки являются противоядием при отравлениях солями многих тяжелых металлов.
Осаждение белков солями тяжелых металлов необратимо. Однако некоторые из таких осадков, в частности, полученные в условиях описанного опыта, растворяются в избытке осадителя – р-ра соли меди или свинца – в результате пептизации осадка адсорбирующимися на его частицах ионами.
Материалы:
· р-ры белков
· сернокислая медь (насыщ. водный р-р)
· уксуснокислый свинец (20%-ный водный р-р)
Поместив в две пробирки по 1-1,5 мл исследуемого р-ра белка, добавляют в одну из них р-р сульфата меди, а в др. р-р уксуснокислого свинца. Добавляют реактив медленно по каплям, встряхивая.
Первоначально образуется хлопьевидный осадок или муть вследствие выделения малорастворимого соединения белка с солью меди (голубого цвета) или с солью свинца (белого цвета). При дальнейшем добавлении реактива осадок растворяется.
ОПЫТ №5. Биуретовая реакция белков.
Введение. Биуретовая реакция обнаруживает в молекуле белка пептидных группировок, ее дают все белки. Продукты распада белка – полипептиды – также дают биуретовую р-цию, причем цвет образующихся медных комплексов определяется числом аминокислот, связанных пептидной связью. Дипептиды дают синюю окраску, трипептиды – фиолетовую, а тетропептиды и более сложные пептиды – красную. Фиолетовый цвет медного комплекса с белком в условиях проведения биуретовой реакции и др. данные указывают на преобладание в сложной белковой частице трипептидных группировок.
Некоторые другие атомные группы, например, ….., при накоплении их в молекуле также могут обусловить положительную биуретовую р-цию. При ее проведении следует избегать избытка медной соли, так как образующийся в этом случае синий гидрат окиси меди маскирует появление синей окраски фиолетовой.
Материалы:
· едкий натр (20-30%-ный р-р)
· сернокислая медь (насыщ. водный р-р)
А. К 1-2 мл р-ра белка добавляют равный объем щелочи и затем 3-5 капель (не больше!) р-ра медного купороса. Жидкость окрашивается в ярко-фиолетовый цвет, который заметен даже в окрашенной водной вытяжке из мяса.
Б, При малом содержании белка (р-ры лейкозина или молочного альбумина) и недостаточной яркости получаемой окраски снова смешивают в чистой пробирке р-ры белка и щелочи, наклоняют пробирку и осторожно приливают по ее стенке из пипетки 0,5-1 мл р-ра серной к-ты – так чтобы он образовал в пробирке р-ры белка и щелочи, не смешиваясь с остальной жидкостью. В том случае на границе слоев появляется очень отчетливо фиолетовое прозрачное кольцо.
ОПЫТ №5. Ксантопротеиновая реакция белков.
Введение. Ксантопротеиновая реакция обнаруживает наличие в белке свободных или конденсированных ароматических ядер, т.е. остатков таких к-т, как фенилаланин, тирозин, триптофан. Желтое окрашивание появляется в результате нитрования этих ядер азотной к-той и образования полинитросоединений. Переход в щелочной среде желтой окраски подобных в-в в оранжевую обусловлен образованием более интенсивно окрашенных анионов. Взамен едкой щелочи можно применять аммиак.
Кислотные альбуминаты, образующиеся при энергичном действии кислот на белки, нерастворимые в воде и в разбавленных р-рах солей, но хорошо растворяются в щелочах и разбавленных кислотах. Кислотные альбуминаты связывают значительно большее кол-во к-ты, исходный белок.
Материалы:
· р-ры белков,
· азотная к-та (конц., уд. в. 1,4)
· едкий натр или едкое кали (20-30%-ный р-р)
К 1 мл белка добавляют 0,2-0,3 мл азотной к-ты, появлется белый осадок или муть. Затем нагревают смесь до кипения и поддерживают его в течение 1-2 мин., при этом р-р и осадок окрашиваются в ярко-желтый цвет. При кипячении выделившийся осадок может частично или полностью раствориться в результате гидролиза, но характерная желтая окраска р-ра сохраняется.
Охладив смесь, осторожно добавляют к кислой жидкости по каплям избыток (1-2 мл) р-ра щелочи. Выпадает осадок кислотного альбумината, образуя с избытком щелочи ярко-оранжевый р-р.
 2015-10-16
2015-10-16 4535
4535