Не все жидкости являются проводниками. Рассмотрим ток в растворах и расплавах электролитов.
Электролиты – вещества, растворы и расплавы которых проводят электрический ток. Это кислоты, соли, щёлочи, то есть вещества, которые имеют ионное строение. Жидкости обладают ионной проводимостью.
Протекание тока в электролитах сопровождается химическими реакциями.
Электролиз – процесс выделения на электродах вещества, связанный с окислительно-восстановительными реакциями при протекании тока через раствор или расплав электролита. Законы электролиза были открыты экспериментально М. Фарадеем в первой половине XIX века.
Первый закон электролиза: масса выделившегося при электролизе вещества прямо пропорциональна заряду (силе тока и времени его протекания), прошедшему через электролит.
m = kq или m = kIt,
где k – электрохимический эквивалент – постоянная величина, показывающая массу выделившегося вещества при прохождении заряда 1 Кл.
Второй закон электролиза: электрохимический эквивалент – постоянная для данного вещества величина, определяемая выражением:
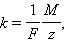
где F – постоянная Фарадея, равная произведению постоянной Авогадро на величину элементарного заряда 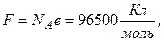 M – молярная масса вещества, z – валентность иона.
M – молярная масса вещества, z – валентность иона.
Обобщённый закон электролиза:
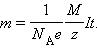
Для тока в растворах и расплавах электролитов справедлив закон Ома. Электрическое сопротивление электролитов описывается формулами однородного проводника.
 2015-10-13
2015-10-13 478
478








