А. Цианид калия КСN – соль слабой одноосновной кислоты НСN и сильного основания КОН. При растворении в воде молекулы КСN полностью диссоциируют на катионы К+ и анионы СN-
КСN ↔ К+ + СN-.
Катионы К+ не могут связывать ионы ОН- воды, так как КОН – сильный электролит. Анионы же СN- связывают ионы Н+ воды, образуя молекулы слабого электролита НСN. Соль гидролизуется, как говорят, по аниону. Ионно-молекулярное уравнение гидролиза
СN-+НОН 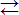 НСN+ОН-,
НСN+ОН-,
или в молекулярной форме
КСN+Н2О 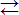 НСN+КОН.
НСN+КОН.
В результате гидролиза в растворе появляется некоторый избыток ионов ОН-, поэтому раствор КСN имеет щелочную реакцию (рН>7).
Б. Карбонат натрия Na2CO3 – соль слабой двуосновной кислоты Н2СО3 и сильного основания NaOH. При растворении в воде молекулы Na2CO3 полностью диссоциируют на катионы Na+ и анионы CO 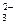 :
:
Na2CO3 ↔ 2Na+ + CO 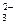 .
.
В этом случае анионы соли CO 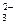 , связывая водородные ионы воды, образуют анионы кислой соли HCO
, связывая водородные ионы воды, образуют анионы кислой соли HCO 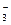 , а не молекулы Н2СО3, так как ионы HCO
, а не молекулы Н2СО3, так как ионы HCO 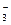 диссоциируют гораздо труднее, чем молекулы Н2СО3. В стандартных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону.
диссоциируют гораздо труднее, чем молекулы Н2СО3. В стандартных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону.
Ионно-молекулярное уравнение гидролиза
CO 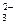 + НОН
+ НОН 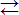 HCO
HCO 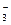 + ОН-,
+ ОН-,
или в молекулярной форме
Na2СО3+Н2О 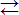 NaHCO3+NaOH.
NaHCO3+NaOH.
В растворе появляется избыток ионов ОН-, поэтому раствор Na2CO3 имеет щелочную реакцию (рН > 7).
В. Сульфат цинка ZnSO4 – соль слабого двукислотного основания Zn(OH)2 и сильной кислоты Н2SO4.
ZnSO4 ↔ Zn2+ + SO 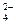 .
.
В этом случае катионы Zn2+ связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH+. Образование молекул Zn(OH)2 не происходит, так как ионы ZnOH+ диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону.
Ионно-молекулярное уравнение гидролиза
Zn2++НОН 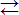 ZnOH++H+
ZnOH++H+
или в молекулярной форме
2ZnSO4+2Н2О 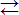 (ZnOH)2SO4+Н2SO4.
(ZnOH)2SO4+Н2SO4.
В растворе появляется избыток ионов водорода, поэтому раствор ZnSO4 имеет кислую реакцию (рН < 7).
Пример 2. Какие продукты образуются при смешивании растворов Al(NO3)3 и К2СО3? Составьте ионно-молекулярное и молекулярное уравнение реакции.
 2015-10-14
2015-10-14 243
243







