Расчёт процессов базируется на первом и втором началах термодинамики, которые мы запишем в дифференциальной форме для одного килограмма термодинамической системы. Пересчёт на всю массу системы будет осуществляться простым умножением удельных характеристик системы на ее массу М.
Итак, имеем
 - I начало термодинамики, (3.1)
- I начало термодинамики, (3.1)
 - II начало термодинамики. (3.2)
- II начало термодинамики. (3.2)
Входящие в эти выражения дифференциалы вычисляются следующим образом:
 (3.3)
(3.3)
Кроме того, для идеального газа имеем
 (3.4)
(3.4)
Считается также заданной химическая формула газа или, в случае смеси, её состав, т.е. считаются заданными величины  .
.
С математической точки зрения система уравнений (3.1) – (3.4) является незамкнутой, т.к. девять уравнений содержат десять неизвестных. В качестве последнего, десятого, должно задаваться уравнение процесса, т.е. функциональная зависимость между параметрами системы, определяемая наложением внешних условий, связанных со свойствами оболочки, ограничивающей рассматриваемую термодинамическую систему. В общем случае записать уравнение процесса в математической форме не представляется возможным, т.к. свойства оболочки зависят от произвола экспериментатора.
На практике чаще всего имеют дело с термодинамическими процессами, в течение которых на каждых малых участках процесса можно с достаточной точностью считать постоянным соотношение между количествами работы и теплоты. Такие процессы называют политропными. Итак, по определению, для политропных процессов имеем

Поскольку для идеального газа  , отсюда следует, что уравнение политропного процесса может быть записано в виде
, отсюда следует, что уравнение политропного процесса может быть записано в виде
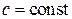 , (3.5)
, (3.5)
т.е. политропный процесс можно определить как процесс с постоянной теплоёмкостью. Так как соотношение между теплотой и работой процесса может быть произвольным и наперёд заданным, то и теплоёмкость его может принимать самые различные значения, в частности нулевое, отрицательные и положительные, т.е. в общем случае  .
.
Соотношения между параметрами в политропном процессе можно получить на основании уравнений политропного процесса в переменных  . Используем для этого две записи I начала термодинамики в формах (3.1), подставив в них дифференциалы из (3.3) и (3.4):
. Используем для этого две записи I начала термодинамики в формах (3.1), подставив в них дифференциалы из (3.3) и (3.4):
 (3.6)
(3.6)
Перенеся слагаемые с 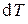 в левые части этих выражений и разделив второе уравнение на первое, получим
в левые части этих выражений и разделив второе уравнение на первое, получим
 .
.
Комплекс (постоянный в случае политропного процесса)
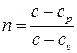 (3.7)
(3.7)
носит название показателя политропы. Имеем, таким образом
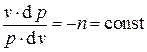 .
.
Разделяя переменные в этом уравнении и интегрируя, получаем связь между давлением и объёмом в политропном процессе в виде
 . (3.8)
. (3.8)
Значение постоянной интегрирования может быть найдено, если заданы давление и удельный объём в каком-либо состоянии, например в начальном, т.е. при 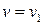 задано давление
задано давление  . Имеем тогда
. Имеем тогда
 . (3.9)
. (3.9)
Далее, получим уравнение политропного процесса в переменных  . Из (3.2) и (3.3) имеем
. Из (3.2) и (3.3) имеем
 .
.
Отсюда с учётом постоянства теплоёмкости легко получаем
 .
.
Используя начальные данные  , находим уравнение политропного процесса в координатах
, находим уравнение политропного процесса в координатах  :
:
 . (3.10)
. (3.10)
Обычно на практике политропный процесс задаётся не значением теплоёмкости c, а значением показателя политропы n, тогда теплоёмкость процесса вычисляется как

или
 , (3.11)
, (3.11)
где величина k носит название показателя адиабаты и определена ранее (см. (2.13)) (происхождение этого названия будет ясно из дальнейшего).
Из уравнения политропного процесса в переменных  (3.9) и записи уравнения состояния для начального и конечного состояний в процессе можно получить так называемые соотношения между параметрами в политропном процессе:
(3.9) и записи уравнения состояния для начального и конечного состояний в процессе можно получить так называемые соотношения между параметрами в политропном процессе:
 . (3.12)
. (3.12)
Вычисление количества теплоты в политропном процессе производится в соответствии с определением (1.32) или (1.33), т.е.
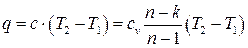 . (3.13)
. (3.13)
Работа изменения объёма в политропном процессе может быть найдена интегрированием (1.25) с учётом зависимости давления от объёма (3.9):
 . (3.14)
. (3.14)
Подстановка пределов и использование соотношений между параметрами в политропном процессе (3.12) позволяет записать выражение для удельной работы изменения объёма в трёх эквивалентных формах:
 (3.15)
(3.15)
Полезная внешняя работа также может быть вычислена непосредственно интегрированием (2.14), однако можно поступить проще, приняв во внимание тот факт, что
 . (3.16)
. (3.16)
 2017-10-25
2017-10-25 2912
2912








