Матеріали, реактиви, обладнання:
розчин гемоглобіну людини, дистильована вода, мірні колби на 50, 100, 200 мл, фотометр КФК-3.
Аналіз спектрів поглинання широко застосовується при дослідженні гемоглобіну – основного компоненту еритроцитів. Функція гемоглобіну полягає у зворотному зв’язуванні молекулярного кисню і транспортуванні його до всіх клітин організму. Гемоглобін відноситься до складних білків – гемопротеїдів. Його молекула складається з чотирьох поліпептидних ланцюгів (2 α- і 2 β-ланцюги). Кожен ланцюг зв’язаний з гемом, в якому розміщений іон двовалентного заліза.
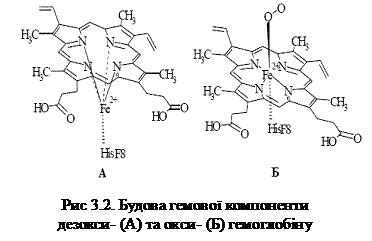 При поглинанні кисню β-ланцюги гемоглобіну зближуються, при віддачі – розходяться. Розміщення α-ланцюгів при цьому мало міняється. Приєднання і віддача кисню молекулою гемоглобіну супроводжується структурними змінами, що приводить до зміни спектрів поглинання гемоглобіну. Відомі також інші похідні гемоглобіну – метгемоглобін і карбоксигемоглобін. В метгемоглобіні залізо знаходиться в трьохвалентному стані, в той час як в дезоксигемоглобіні і оксигемоглобіні – в двохвалентному. Кількість метгемоглобіну в крові людини збільшується при радіоактивному опроміненні, при попаданні в організм великої кількості нітратів з їжею. При взаємодії з СО гемоглобін зв’язує його і переходить в карбоксигемоглобін. Концентрація карбоксигемоглобіну в крові підвищується при отруєні чадним газом, при курінні.
При поглинанні кисню β-ланцюги гемоглобіну зближуються, при віддачі – розходяться. Розміщення α-ланцюгів при цьому мало міняється. Приєднання і віддача кисню молекулою гемоглобіну супроводжується структурними змінами, що приводить до зміни спектрів поглинання гемоглобіну. Відомі також інші похідні гемоглобіну – метгемоглобін і карбоксигемоглобін. В метгемоглобіні залізо знаходиться в трьохвалентному стані, в той час як в дезоксигемоглобіні і оксигемоглобіні – в двохвалентному. Кількість метгемоглобіну в крові людини збільшується при радіоактивному опроміненні, при попаданні в організм великої кількості нітратів з їжею. При взаємодії з СО гемоглобін зв’язує його і переходить в карбоксигемоглобін. Концентрація карбоксигемоглобіну в крові підвищується при отруєні чадним газом, при курінні.
Кожна форма гемоглобіну характеризується певним спектром поглинання, який є залежністю оптичної густини від довжини хвилі λ.
Характерний спектр поглинання оксигемоглобіну складається із таких смуг: 414 нм (пік Соре), 576-578 (α-смуга) і 542-544 нм (β-смуга). Інтенсивність двох останніх значно менша інтенсивності піку Соре. Між α- і β-смугами знаходиться мінімум при 560 нм. Відношення поглинання при 542 нм до поглинання при 560 нм становить 1,60-1,68. Ця величина має назву коефіцієнт Гюфнера.
Максимум поглинання при 920 нм дає можливість відрізнити оксигемоглобін від карбоксигемоглобіну. Крім того, пік Соре для карбоксигемоглобіну зсунутий до 422 нм, а максимуми α і β знаходяться при 570 і 540 нм.
В спектрі поглинання дезоксигемоглобіну виділяють максимум при 429 нм (пік Соре), а наступний єдиний максимум виявляється при 556 нм.
Для лужних розчинів метгемоглобіну положення максимумів при 417, 540 і 578 нм мало відрізняється від оксигемоглобінових, але їх інтенсивність значно нижча.
Кислі розчини метгемоглобіну мають вузьку смугу поглинання при 500 нм, широку – в області 630 нм, а смуга Соре зсунута в більш короткохвильову область – 405 нм.
Таким чином, при вивченні спектрів поглинання гемоглобіну можна не тільки визначити його концентрацію в розчині, але й проаналізувати, в якій формі він знаходиться, визначити кінетику переходу від одної форми до іншої.
В даній роботі для дослідження спектрів поглинання гемоглобіну використовується фотометр КФК-3. Фотометр КФК-3 застосовується для вимірювання коефіцієнтів пропускання і оптичної густини прозорих розчинів і прозорих твердих зразків, а також для вимірювання швидкості зміни оптичної густини речовини і визначення концентрації речовини в розчинах. Спектральний діапазон фотометра від 315 до 990 нм. В якості диспергуючого елемента у фотометрі застосовується дифракційна решітка. Спектральний інтервал, який виділяється монохроматором, не перевищує 7 нм.
Мікропроцесорна система забезпечує виконання наступних задач:
| «НУЛЬ» | - вимірювання і врахування сигналу при неосвітленому фотоприймачеві; |
| «Г» | - градуювання фотометра (визначення вихідного сигналу фотоприймача); |
| «Е» | - вимірювання оптичної густини; |
| «П» | - вимірювання коефіцієнта пропускання; |
| «С» | - вимірювання концентрації; |
| «А» | - вимірювання швидкості зміни оптичної густини; |
| «Г» | - введення коефіцієнта факторизації. |
Принцип дії фотометра КФК-3 оснований на порівнянні світлового потоку І0, що проходить через розчинник, і світлового потоку І, що проходить через розчин досліджуваної речовини.
Світлові потоки І0 та І перетворюються фотоприймачем в електричні сигнали U0, U і UT (UT – сигнал при неосвітленому фотоприймачеві), які обробляються мікро-ЕОМ фотометра і висвічуються на цифровому табло у вигляді значень коефіцієнта пропускання, оптичної густини, швидкості зміни оптичної густини, концентрації.
Коефіцієнт пропускання (τ) досліджуваного розчину визначається як відношення світлових потоків або сигналів:
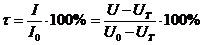 .
.
Оптична густина (D):
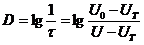 .
.
Швидкість зміни оптичної густини:
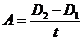 ,
,
де D2-D1 – різниця значень оптичної густини за час t в хвилинах. Час t може приймати значення 1, 2, 3, 4, 5, 6, 7, 8, 9 хвилин.
Концентрація:
С= D·F,
де F – коефіцієнт факторизації, що визначається дослідником і вводиться з цифрової клавіатури в межах від 0,001 до 9999.
Оптична схема фотометра КФК-3 показана на рис. 3.3.
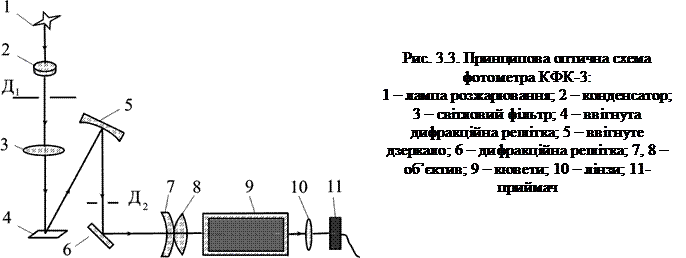
Дифракційна решітка і дзеркало створюють в площині діафрагми Д2 розтягнуту картину спектру. Повертаючи дифракційну решітку навколо осі, паралельної штрихам решітки, щілиною діафрагми Д2 виділяють промені будь-якої довжини від 315 до 990 нм. Об’єктив створює в кюветному відділенні слабозбіжний пучок світла. Лінза зводить пучок, що пройшов кюветне відділення, на фотоприймачі у вигляді рівномірно освітленого світлового круга. В кюветному відділенні при роботі встановлюються прямокутні кювети з досліджуваним розчином.
Хід роботи
Готують розчин невідомої форми гемоглобіну, який відповідає закону Бугера-Ламбетра-Бера, в дистильовані воді. Розчин наливають в односантиметрову кювету. В другу кювету наливають дистильовану воду. Потім роботу проводять на фотометрі в режимі вимірювання оптичної густини. Для цього кювети розміщують у кюветному відділенні. Переводом ручки кюветного відділення у світловий пучок поміщають кювету з водою. Поворотом ручки, зв’язаної з дифракційною решіткою, встановлюють необхідну довжину хвилі, значення (в нм) при цьому висвітлюється на верхньому цифровому табло. Далі при закритій кришці кюветного відділення натискають послідовно клавішу «Г» і клавішу «Е». При цьому на табло з’являється значення «0,000±0,002». Це означає, що початковий відлік оптичної густини встановився на фотометрі правильно. Після цього при відкритій кришці натискають клавішу «НУЛЬ», закривають кришку і натискають клавішу «Е». На табло з’являється значення «0,000». Таким чином враховано густину поглинання розчинника (в даному випадку води) і нульовий відрахунок. Далі поворотом ручки кюветного відділення в світловий пучок переводять кювету з розчином гемоглобіну. При цьому на табло з’являється значення оптичної густини при заданій довжині хвилі.
Для побудови спектральної кривої необхідно визначити оптичну густину розчину в інтервалі від 350 до 700 нм, змінюючи кожен раз довжину хвилі на 5 нм результати оформлюють на міліметровому папері у вигляді графіку залежності D від λ.
Після побудови спектральної кривої необхідно проаналізувати на ній максимуми і мінімуми поглинання і визначити, в якій формі знаходиться гемоглобін, його фізико-хімічний стан.
Контрольні запитання.
- В чому полягає явище поглинання світла?
- Виведіть закон Бугера-Ламберта-Бера.
- На чому базуються методи концентраційної колориметрії?
- Яку інформацію можна одержати при вивченні спектрів поглинання гемоглобіну?
- Опишіть принцип роботи КФК-3.
 2018-01-08
2018-01-08 1066
1066







