ЛЕКЦИЯ 12
Изоляция металлов от агрессивной среды ( ПОКРЫТИЯ ):
Металлические покрытия – покрытие защищаемого металла слоем другого металла, практически не корродирующего в тех же условиях.
При покрытии изделия различными металлами надо помнить, что покрытие и защищаемый металл могут образовывать гальваническую пару. Ее работа в определенных условиях может либо усиливать защитное действие, либо наоборот усиливать коррозию защищаемого металла.
Анодное покрытие. Например при локальном нарушении цинкого покрытия в гальвано паре цинк–железо анодом будет цинк, который и будет разрушаться, защищая железо.
Катодное покрытие. А в паре олово–железо при нарушении оловянного покрытия разрушению будет подвергаться железо, т.к. в этой паре именно оно является анодом.
Различия коррозиционной стойкости покрытий в тех или иных агрессивных средах и свойства конечных продуктов коррозии определяют специфические области применения этих покрытий.
| Анодное покрытие | |||
 | |||
  | (–) А, Zn | H2SO4| Fe, К (+) А (–) Zn – 2ē ® Zn2+ К (+) 2Н++ 2ē ® Н2 | ||
| Zn + 2Н+® Zn2+ + Н2 Zn + H2SO4 ® ZnSO4+ Н2 |
| Катодное покрытие | |||
 | |||
  | (–) А, Fe | H2O, O2| Sn, К (+) А (–) Fe – 2ē ® Fe2+ К (+) 2H2O + O2 + 4ē → 4OH– | ||
| 2Fe + 2H2O + O2® 2Fe2+ + 4OH– 2Fe + 2H2O + O2 ® Fe(OH)2 ¯ |
Неметаллические покрытия – пленки высокополимерных веществ (каучуки, пластмассы), лаки, олифа, композиции из высокополимерных и неорганических красящих веществ.
Покрытие резиной называется – гуммирование, а бетоном – торкретирование
90% всех металлических изделий защищают подобным образом. Дешевы, их просто наносить, но они не прочны.
Химические покрытия(более надежны):
пленки из оксидов металлов (толщиной 0,3 микрона), получаемые при действии кислорода или подходящих окислителей (HNO3, K2Cr2O7 и др.) на поверхность металлов. Часто такие оксидные пленки образуются на поверхности металлов просто при соприкосновении с воздухом, что делает химически сравнительно активные металлы (Zn, Al) практически коррозионно-стойкими;
подобную же роль могут играть защитные нитридные пленки, образующиеся при действии азота или аммиака на поверхность некоторых металлов;
искусственное оксидирование (толщиной до 30 микрон), азотирование и фосфатирование, причем лакокрасочные покрытия наносятся на оксидированный, азотированный и фосфатированный металл.
Так оксидирование железа (выроненная сталь) проводят в смеси гидроксида натрия (800г/л) с нитратом (50г/л) и нитритом (200г/л) натрия при температуре 140 оС.
Оксидирование железа приводит к формированию на его поверхности пленок Fe3O4 – черного цвета или Fe2O3 – коричневого цвета.
А для фосфотирования применяют фосфаты марганца и железа, которые приводят к формированию трудно растворимых пленок трехвалентного железа.
Фосфатные и оксидные пленки нередко используют как электроизоляционные покрытия, например на трансформаторных пластинах (пробивное напряжение таких пленок может достигать 600 В).
Электрохимические методы защиты – основаны на изменении потенциала защищаемого металла и не связаны с изоляцией металла от коррозионной среды.
| Катодная защита | |
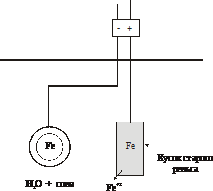 | катодная (электрозащита) – защищаемая конструкция, находящаяся в среде электролита (например, в почвенной воде), присоединяется к катоду внешнего источника электричества (к отрицательному полюсу). В ту же агрессивную среду помещают кусок старого металла (рельс или балка), присоединенный к аноду внешнего источника электричества. Фактически он служит источником электронов, поставляемых на катод. В процессе коррозии этот кусок старого металла разрушается. |
| Протекторная зашита | |||
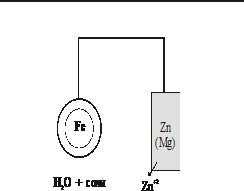 | протекторная (анодная) – используется специальный анод – протектор, в качестве которого применяют металл более активный, чем металл защищаемой конструкции (Zn, Mg). Протектор соединяют с защищаемой конструкцией проводником электрического тока. В процессе коррозии разрушается протектор. Этот метод применяется для защиты от коррозии лопастей турбин подводных частей кораблей, для защиты холодильного оборудования, работающего с солевыми продуктами. | ||
  | (–) А, Zn | H2O, O2| Fe, К (+) А (–) Zn – 2ē ® Zn2+ К (+) 2H2O + O2 + 4ē → 4OH– | ||
| 2Zn + 2H2O + O2 ® 2Zn2+ + 4OH– 2Zn + 2H2O + O2 ® 2Zn(OH)2 | |||
Воздействие на агрессивную среду
Для замедления коррозии металлических изделий в агрессивную среду вводят вещества (чаще всего органические), называемые ингибиторами коррозии, которые пассивируют поверхность металла и препятствуют развитию коррозионных процессов. Это имеет большое значение в тех случаях, когда металл необходимо защищать от разъедания кислотами. Ингибиторы коррозии широко применяют при химической очистке паровых котлов от накипи, для снятия окалины с отработанных изделий, а также при хранении и перевозке HCl в стальной таре. В качестве органических ингибиторов коррозии применяют тиомочевину (сульфид-диамид углерода C(NH2)2S), диэтиламин, уротропин (гексаметилентетрамин (CH2)6N4) и другие производные аминов, а в качестве неорганических – силикаты, нитриты, дихроматы щелочных металлов и др.
К этой же группе методов защиты металлов от коррозии относится также освобождение воды, идущей на питание паровых котлов, от растворенного в ней кислорода, что достигается, например, при фильтровании воды через слой железных стружек.
 2018-01-08
2018-01-08 1230
1230






