Мини-тест по Теме «Теория Бутлерова. Изомерия»
1.Элемент, который обязательно входит в состав органических соединений
а)кислород б)азот в) углерод г)фосфор
2. Причиной многообразия органических веществ не является
а) явление изомерии
б) способность атомов углерода соединяться друг с другом
в) способность атомов углерода образовывать одинарные, двойные и тройные связи
г) способность атомов углерода образовывать аллотропные модификации.
3.Принадлежность к органическим веществам можно установить:
а)по окраске вещества
б) по продуктам сгорания вещества
в)по растворимости веществ в воде в)по агрегатному состоянию вещества.
4.Правой части уравнения CO2+ 2H2Oсоответствует левая
а)CH4+ 2O2
б) CH4 + CL2
в) 2С2H6+ 5O2
5. Формулу CH3– CH2– CH2– CH2называют
а) полная структурная б)краткая структурная в)молекулярная г) все ответы верны
Тема: Непредельные углеводороды
Урок: Алкены. Строение, номенклатура, изомерия и физические свойства
1. Понятие о алкенах и их классификация
Алкены (олефины, этиленовые углеводороды)– углеводороды, которые содержат в молекуле одну двойную связь. Общая формула – CnH2n.
Первый член ряда – этилен (этен) C2H4: 
2. Номенклатура алкенов
Двойную связь обозначают с помощью суффикса - ен. Основная цепь должна включать кратную связь. Нумерация цепи проводится с того конца, к которому ближе двойная связь.
CH3-CH2-CH2-CH=CH-CH3 гексен-2  2-этилпентен-1
2-этилпентен-1
3. Строение алкенов
sp3-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 4.
sp2-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 3.
sp-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 2
 Рис. 1. Строение этилена
Рис. 1. Строение этилена
Атомы углерода при двойной связи находятся в состоянии sp 2-гибридизации. Двойная связь состоит из σ-связи, образованной sp 2-гибридными орбиталями, и π-связи, возникающей за счет перекрывания p -орбиталей. Три σ-связи атома углерода направлены к вершинам треугольника с атомом С в центре, угол между связями 120о. Молекула этилена плоская, а электронная плотность π-связи расположена над и под этой плоскостью. Рис. 2. В других алкенах плоским является фрагмент, который непосредственно примыкает к двойной связи. Рис. 3. В углеродных соединениях π-связь значительно слабее, чем σ-связь.Под воздействием реагентов π-связь легко разрывается. Шаростержневые модели молекул этена и пропена отражают их пространственное строение.
4. Изомерия алкенов
1. Изомерия углеродного скелета.

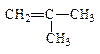
бутен-1 2-метилпропен
2. Изомерия положения двойной связи.


бутен-1 бутен-2
3. Межклассовая изомерия (с циклоалканами)

циклобутан метилциклопропан
4. Геометрическая изомерия.
 Рис. 4. Геометрические изомеры бутена-2
Рис. 4. Геометрические изомеры бутена-2
Вращения вокруг двойной связи не происходит, ведь для этого нужно разорвать π -связь. Из-за этого у алкенов существует изомерия, связанная с тем, что заместители могут располагаться по одну или по разные стороны двойной связи, как, например, у бутена-2. Рис. 4.
Для бутена-1 геометрическая изомерия невозможна (у одного из атомов С при двойной связи оба заместителя одинаковы: 2 атома водорода).
5. Физические свойства и нахождение в природе алкенов
Этен, пропен и бутен – газы. Алкены, содержащие от 5 до 18 атомов С в молекуле, – жидкости. Если атомов в молекуле алкена больше 19 – это твердые вещества.
Алкены бесцветны, нерастворимы в воде и легче ее, обладают характерным резким запахом.
Алкены в природе
Этилен образуется в фруктах, регулируя процесс их созревания. К классу алкенов принадлежат феромоны некоторых насекомых.
дз
 2018-01-21
2018-01-21 352
352






