ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Для полного описания химической реакции необходимо знать также закономерность ее протекания во времени, т.е. ее скорость и механизм. Раздел химии – химическая кинетика изучает скорость и механизм химических реакций. Одни химические реакции протекают быстро, а другие медленно. Например, нейтрализация кислоты основанием происходит сразу же после того, как мы смешаем их в одном сосуде. Также при смешивании раствора Ag+ с раствором Cl- на глазах происходит выпадение осадка AgCl.
Другие реакции, например, сгорание бензина протекает быстрее или медленнее в зависимости от того, каким образом осуществляется контакт между реагентами. Если смешать пары бензина с воздухом, то скорость так велика, что при этом происходит взрыв. Но если поджечь небольшое количество бензина, он будет гореть довольно медленно. Очень медленно протекают например, ржавление железа (окисление), переваривание пищи, сбраживание сахара в спирт и фотосинтез.
Скоростью химической реакции называется изменение концентрации реагирующих веществ в единицу времени при неизменном объеме системы.
Графически изобразим зависимость концентрации исходного вещества от времени:
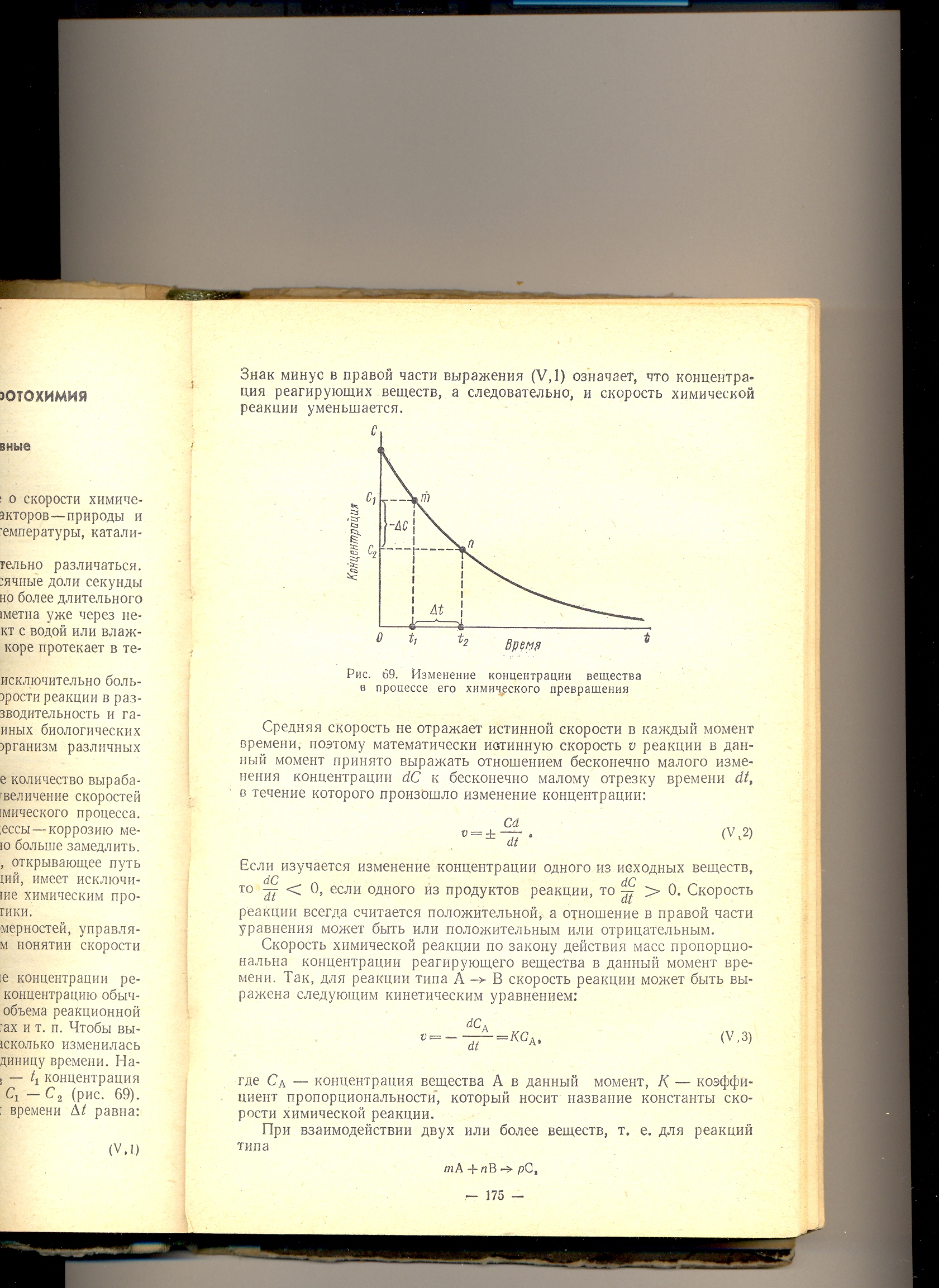
Рис. 1.4.1. Зависимость концентрации исходного вещества от времени:
Скорость реакции может быть установлена лишь для определенного промежутка времени. Так, концентрация исходного вещества в некоторый момент времени t1 равна с1, в момент t2 – c2., то за промежуток времени Dt = t2 - t1 изменение концентрации составит
D c = c2 - c1
Тогда средняя скорость реакции будет равна
с2 – с1 D c
Vср = - -------- = - ---
t2 – t1 D t
Знак минус ставится потому, что хотя концентрация исходного вещества убывает, скорость может быть только положительной величиной.
Скорость химической реакции зависит от многих факторов, среди которых:
- природа и концентрация реагирующих веществ;
- температура;
- давление (для реакций с участием газов);
- присутствие катализаторов;
- среда (для реакций в растворах);
- интенсивность света (в фотохимических реакциях).
 2018-01-21
2018-01-21 1551
1551
