9.Қайсы оксид суда еріп қышқыл түзедi? А) N2O5
10.Қайсы оксид суда еріп негіз түзедi? В)BaO
11.Fe2O3 қайсы затпен әрекеттеседi? С) H2SO4
12.H2SO4 қайсы затпен әрекеттеседi? B) CuO
13. C aCO3 (қ) Û CaO(қ) + CO2 (г) реакциясының тепе-теңдік константасының өрнегі: А) K =pCO2;
14.Қай реакция нәтижесiнде қышқылдық тұз түзiледi? B) H2SO4+NaOH®
15.MgCO3(қ) Û MgO(қ) + CO2 (г) реакциясының тепе-теңдік константасының өрнегі: D) K= pCO2;
16.Қайсы қатарда тек амфотерлi гидроксидтер жазылған? В) Be(OH)2, Zn(OH)2, Cr(OH)3
17.Қай теңдеу негiздiк тұздың түзiлуiне сәйкес келедi? В) Zn(OH)2+HNO3®
18.Қай теңдеу қышқылдық тұздың түзiлуiне сәйкес келедi? С) NaOH+H2SO3®
19.Қайсысы негiздiк тұз болып саналады?
Е) FeOHCl2
20.NaOH-пен әрекеттесетiн затты көрсетiңiз? Е) HCl
21.Негiздiк тұз алынатын теңдеу қайсы?
А) Al(OH)3+HCl®
22.Натрий гидроксидi әрекеттесетiн затты көрсетiңiз. С) SO3
23.Негiздiк тұз түзiлетiн теңдеудi көрсетiңiз.
С) AlCl3+NaOH®
24.Берилий гидроксидi түзiлетiн теңдеу қайсысы?
D) Be(NO3)2+Ca(OH)2®
25.Қай теңдеу реакция жылдамдығының температураға тәуелділігін сипаттайды:
D) u(Т2) = u(Т1) . g (Т2-Т1)/ 10;
26.Мырыш гидроксидi түзiлетiн реакцияны көрсетiңiз. В) ZnCl2+KOH®
27.Хлор қышқылының формуласын көрсетiңiз.
Е) HClO4
28.Тұздардың қайсысы қышқылдық тұзға жатады?
С) NaHCO3
29.Оксидтердiң негiздiк қасиетi қай қатарда артады?
А) CaO®SrO®BaO
30.Қышқылдық тұз түзетiн реакция теңдеуiн көрсетiңiз. В) NaOH+H2S®
31.Температураны 300С арттырғанда реакция жылдамдығы 64 есе артатын болса, онда температуралық коэффициент неге тең? В) 4;
32.Қай қатарда тек амфотерлi гидроксидтер жазылған? D) Be(OH)2, Zn(OH)2, Al(OH)3
33.Қай оксид сумен әрекеттескенде қышқыл түзiледi? Е) SO2
34.Қай оксид суда ерiп гидроксид түзiледi? С) Na2O
35.Берiлген тұздардың қайсысы калийдiң дигидрофосфаты? А) KH2PO4
36. (MnOH)2SO3 тұзы қалай аталады?
В) марганецтің гидроксосульфиті
37.Тотығу дәрежесi “+1” хлор оксидiне сәйкес келетiн қышқылды көрсетiңiз. В) HClO
38.Үш Валенттi марганец оксидiне сәйкес келетiн графикалық формуланы көрсетiңiз.
В)
|
39.Қай қатарда оксидтердiң негiздiк қасиетi артады?
А) CaO®SrO®BaO
40.Берiлген реакциялар iшiнен нейтралдау (бейтараптану) реакциясын көрсетiңiз.
D) 2KOH+H2SO4®K2SO4+2H2O
41.Қай теңдеу кальций гидрокарбонатының қышқылдық тұзының түзілуіне сәйкес келедi?
D) CaCO3+CO2+H2O®
42.44,5 г AlCl3 –гі хлор атомының саны неге тең?
В)6,02 . 1023;
43. Реакцияны толықтырып, қорғасынның амфотерлiгiн дәлелдеңiз.Pb(OH)2+2KOH=…+2H2O
В) K2PbO2
44.Реакцияны толықтырып, хром гидроксидiнiң амфотерлiгiн дәлелдеңiз.Сr(OH)3+KOH=…
А) K3[Cr(OH)6]
45.Электролит ерiтiндiлерде электр тогын қандай бөлшектер өткiзедi? С) иондар
46.Электролит қосылысты көрсетiңiз. D) NaCl
47.Қай зат электролит емес? В) CaCO3
48.Ең күштi электролит қайсысы? А) KOH a=95%
49.Ең әлсiз қышқыл қайсысы? Е) H2SiO3 Kд=2*10-12
50.Көрсетiлген суда жақсы еритiн негiздердердiң қайсысы әлсiз электролит? С) NH4OH a=1,35%
51.Қайсы электролит сатылап диссоциацияланады?
С) H2SO4
52.Fe2(SO4)3 тұзының диссоциациясы нәтижесiнде барлығы қанша ион түзiледi? Е) 5
53.Қайсы электролиттiң диссоциациясы кезiнде хлорид ионы Cl- түзiледi? Е) NaCl
54.Еру кестесін пайдаланып реакцияның иондық теңдеуiн жазғанда қайсы қосылыстың молекула түрiнде жазылатынын анықтаңыз. D) AgCl
55.Бiрдей жағдайдағы қышқылдардың қайсысында Н+ ионының концентрациясы ең аз болады?
Е) H2CO3 Kд=5,6*10-11
56.Тұздың гидролиздену реакциясын көрсетiңiз.
С) MgCl2+H2O®
57.Қай тұз гидролизденедi? А) Cu(NO3)2
58.Қай тұз гидролизденбейдi? С) KCl
59.FeCl3 тұзының гидролизi неше сатыда жүредi С)3
60.Қай тұз гидролизденгенде реакцияның ортасы қышқылдық болады (рН<7)? А)AlCl3
61.Қысқартылған иондық теңдеу Al+6H+® Al3++3H2 қай реакцияға сәйкес келедi? В) Al+HCl®
62.Сутегi ионының концентрациясы [Н+]=1•10-4 болғанда ерiтiндiнiң рН-ы қаншаға тең болады (рН=-lg[H+]) А) 4
63.Массалық үлесi 20 % (w,%) 100 г натрий хлоридi ерiтiндiсiн дайындау үшiн қанша грамм натрий хлоридiн өлшеп алу керек? С) 20
64.0,5 л 1Н Na2SO4 ерiтiндiсiн дайындау үшiн қанша грамм Na2SO4 өлшеп алу керек? С) 35,5
65.1 литр ерiтiндiде 98 г H2SO4 болса (M H2SO4=98 г/моль) осы ерiтiндiнiң мольдік концентрациясы қандай? С) 1М
66.100 мл ерiтiндiде 3,4 г AgNO3 ерiтiлген. Ерiтiндiнiң нормальдығы қандай?
M(AgNO3 )=170 г/моль). А) 0,2
67.Ерiтiндiнiң эквиваленттiк концентрациясын анықтаңыз, егер 100 мл ерiтiндiде 6,3 г HNO3 болса. М(HNO3) = 63 г/моль). В) 1,0
68.80 г электролит емес зат 2 кг суда (Н2О) ерiтiлген. Бұл заттың мольдік массасы 80 г/моль. KH2O=1,860. Ерiтiндiнiң қату температурасын анықтаңыз (Dt). D) -0,930 Е) -3,720
69.0,01М HNO3 ерiтiндiсiнiң рОН мәнiн есептеңiз. В)12
70.0,01М КОН ерiтiндiсiнiң рН мәнiн есептеңiз. Е)12
71.Ерiтiндi сiлтiлiк орта болатын тұзды көрсетiңiз (рН>7). В) K2CO3
72.Ерiтiндiде рОН=3 болғанда, сутегi ионы концентрациясы неге тең? Е) 10-11
73.Гидролизге ұшырамайтын тұзды көрсетiңiз. А)KNO3
74.Қай тұз гидролизiнде негiздiк тұз түзіледi? С)FeCl3
75.0,25н NaOH ерiтiндiсiнiң титрiн анықтаныз. А)0,01
76.Әлсiз электролиттi көрсетiңiз. С) Al(OH)3
77.Қай электролит екi сатыда диссоциацияланады?
В) H2CO3 С) Na2CO3
78.Na3PO4 толық диссоциацияланғанда түзiлетiн ион саны: С) 4
79.Берiлген заттардың қайсысының гидролизiнде қышқылдық тұз түзiледi? D) K2S
80.Құрамында 50 г тұзбен 200 г суы бар ерiтiндiдегi тұздың массалық үлесiн (%) есептеңiз. В)2 0
81.Қай электролит диссоциацияланғанда тек ОН- ионы түзiледi? С) NaOH
82.Мыс хлориді ерітіндісін электролиздегенде катодтың массасы 10 г артты. Анодта қандай газ, қанша көлемде бөлінді С) 3,53 л оттегі;
83.Көлемдерi бiрдей 0,04М HCl мен 0,03М NaOH әрекеттескенде алынған ерiтiндiнiң рН-ын есептеңiз. С) 2
84.20 %-тiк ерiтiндi дайындау үшiн 400 г суда NaNO3-тiң қандай мөлшерiн ерiту керек? D) 100г
85.Қайсы тұз ерiтiндiсi гидролизденгенде сiлтiлiк орта болады? рН>7. D) CH3COONa+HOH®
86.100 мл ерiтiндiде 49 г H2SO4 бар болса, осы ерiтiндiнiң нормальдығы қандай? А)10
87.Қай тұздың ерiтiндiсi үш сатыда жүредi? А)CrCl3
88.Қай тұз ерiтiндiсi гидролизденгенде қышқыл орта болады? (рН<7). С) CuCl2
89.Ерiтіндiнiң рН-ы 3-ке тең болса, ОН- иондары концентрациясы неге тең? Е) 10-11
90.Құрамында 3,46 г мочевина, 100 мл суы бар ерiтiндiнiң қайнау температурасын анықтаңыз. Судың эбулиоскопиялық константасы 0,520 (Е=0,520С). В)1 00,3
91.100 мл ерiтiндiде 3,4 г AgNO3 болса, осы ерiтiндiнiң нормальдығы қандай?
M(AgNO3) =170 г/моль А) 0,2
92.Тұздар бiрлесе гидролизденгенде қандай газ түзiледi?AgCl3+Na2CO3+HOH® Е) CO2
93.Қайсы тұз ерiтiндiсiнде рН мәнi жоғары болады?
А)K2CO3
94.30 г бейэлектролит (электролит емес) 500 г суда ерiтiлген. КН2О=1,860С. Ерiтiндi –1,860С-та қатады. Ерiтiлген заттың молекулалық массасын анықтаңыз (г/моль). В) 60
95.Қай тұз ерiтiндiсi гидролизденгенде сiлтiлiк орта болады? рН>7. D) CH3COONa+HOH®
96.Көлемi 11,2 л азоттың массасы неге тең (қ.ж.)?
С) 14 г
97.Оттегiнiң және сутегiнiң эквивалентiнiң мольдік көлемiн анықтаңыз (қ.ж.)? С) 5,6 лО2 және 11,2 л Н2 98.Қай тұз үшiн гидролиз негiздiк тұз түзiлу арқылы жүредi? А) ZnCl2
99.Гидроксид ионының концентрациясы рОН=10-4 болса, ерiтiндiнiң рН-ы қандай? D) 10
100.Егер [Н+] концентрациясы 10-3 болса, хлорлы сутегi қышқылының ерiтiндiсiнiң рН нешеге тең? Е)3
101.Массасы 120 г ерiтiндiде 24 г калий гидроксидi бар болса, осы ерiтiндiнiң массалық үлесi қандай (w, %)? С)20
102.160 г суда 40 г тұз ерiтiлген. Ерiтiндiдегi заттың массалық үлесi қандай (w, %)? D)20
103.250 мл ерiтiндiдегi 10,5 г натрий фторидiнiң нормальдық концентрациясы неге тең? MNaF=42 г/моль. С)1
104.Күштi электролиттi көрсетiңiз? С)NaNO3
105.400 г 50 % H2SO4 ерiтiндiсiнен (массасы бойынша) буландырып 100 г суды бөлiп алдық. Қалған ерiтiндiдегi H2SO4 массалық үлесi (%) неге тең? В)66,7
106.500 мл 0,25Н Na2CO3 ерiтiндiсiнде қанша Na2CO3 (г) ерiтiлген? В)6,63
107.Ерiтiндiде сутегi ионы концентрациясы 1*10-3 моль/л. Ерiтiндiнiң рН-неге тең? С)3
108.180С температурада Mg(OH)2 –магний гидроксидiнiң суда ерiгiштiгi 1,7•10-4 моль/л. Осы температурадағы Mg(OH)2-ерiгiштiк көбейтiндiсiн анықтаңыз (моль/л). А)1,96•10-11
109.250 г суға 54 г глюкоза (C6H12O6) ерiтiлген. Осы ерiтiндi қандай температурада (0С) кристалданады?
В)-2,23
110.1 литр құрамында 49 г H2SO4 бар. Осы ерiтiндiнiң нормальдық концентрациясы неге тең? Mr(H2SO4)=98 г/моль. А)1
111.Массасы 125 ерiтiндiде 25 г натрий гидроксидi (NaOH) бар. Осы заттың ерiтiндiдегi массалық үлесi неге тең (w, %)? Е)20
112.рН=6-ға тең ерiтiндiдегi сутегi ионы концентрациясы неге тең (моль/л)? В) 10-6
113.рОН=5-ке тең ерiтiндiдегi сутегi ионы концентрациясы неге тең (моль/л)? Е) 10-9
114.250 мл сулы ерiтiндiде 10,5 г натрий фторидi ерiтiлген. (Мr(NaF)=42). Ерiтiндiнiң нормальдық концентрациясын анықтаңыз. А)1
115.Келтiрiлген ерiтiндiнiң қайсысында рН –мәнi 7-ден жоғары? D)Na2CO3
116.Қай зат ерiтiндiсiнде күмiс ионы (Ag+) көп мөлшерде, егер ол заттардың ерiгiштiк көбейтiндiсi белгiлi болса? В)AgCl 1,7•10-10
117.Массалық үлесi 10% 120 г ерiтiндi дайындау үшiн ас тұзы (NaCl) ерiтiндiсiнiң қандай мөлшерi (г) қажет? С)12
118.250С температурада 0,5 М глюкозà (С6Н12О6) ерітіндісінің осмос қысымы неге тең? В) 1,24
119.1 л ерітіндіде 6,3 г HNO3 (М HNO3 =63 г/моль) ерітілген. Осы ерітіндінің мольдік концентрациясын анықтаңыз. В) 0,1
120.Массасы 5,0 г 200 г суда еріту нәтижесінде электр тогын өткізбейтін және кристалдану температурасы -1, 45 тең ерітінді алынды. Еріген заттың молекулалық массасын анықтаңыз. D) 32
121.Тығыздығы 1,310 г/мл 9,28 М ерітіндідегі натрий гидроксидінің массалық үлесін анықтаңыз. А) 28,3
122.Еріген зат мөлшерінің еріткіш массасына қатынасы С) молялды концентрация
123.Еріген зат эквивалент санының ерітінді көлеміне қатынасы В) нормальдық концентрация
124.Ерітіндінің рН бір мәнге өсуі үшін ерітіндідегі сутегі ионы концентрациясын қалай өзгерту қажет
D) 10 есе төмендету
125.Қай электролит ерітіндісінде хлорид ион бар?
В) NaCl
126.Қай электролит диссоциацияланғанда гидрооксокатион түзеді? D) CuOHCl
127.Қай электролит диссоциацияланғанда гидроанион түзеді? Е) Na2HPO4
128.Электролит емес затты көрсетіңіз С) C6H6
129.Концентрациясы бірдей қышқыл ерітінділерінің қайсысы электр тогын жақсы өткізеді? С) HNO3
130. 40%-к ерітіндіде 0,45 г еріген зат бар, ерітіндінің массасын табыңыз. А) 1,125 г
131.Мольдік концентрациясы 0,5 тең (M HNO3=63 г/мл, С HNO3=0,5 М) 400 мл ерітіндіде қанша г азот қышқылы бар? С) 12,6
132.Концентрациясы 0,25 H 0,5 л күкірт қышқылында қанша г күкірт қышқылы бар? M H2SO4=98 г/моль. А) 6,125
133.200 г Н2О да 40 г қантты С12Н22О11 еріткенде қант ерітіндісінің қайнау температурасы қанша градусқа өседі? (МС12H22O11=342 г/моль). ЕН2О=0,520. А) 0,30С
134.100 г Н2О да 10 г глицеринді С3Н8О3 еріткенде глицерин ерітіндісінің қату температурасы қанша градусқа төмендейдi? (МС3Н8O3=92 г/моль). КН2О=1,860С. В) 2,020С
135.Тұздардың гидролиздену реакциясын көрсетіңіз. D) Zn(NO3)+H2O®
136.Қай тұз гидролизденбейді? С) Na2SO4
137.Қай тұздың гидролизі кезінде орта сілтілік болады, рН>7. А) NaCN
138.Қай тұздың гидролизі кезінде орта бейтарап болады рН=? В) NH4CH3COO
139.Екі тұз бірге гидролизденгенде қандай газ бөлінеді AlCl3+(NH4)2S+HOH®? С) H2S
140.рН=5 кезіндегі ОН- ионының концентрациясы.
В) 10-9
141. ОН- ионының концентрациясы 10-4 болса, Н+ ионының концентрациясы қандай болады? Судың иондық көбейтіндісі 1,0•10-14. В) 10-10
142.рН=7 рОН-ң мәні қанша? Е) 7
143.рОН=3 болса, рН-ң мәні қандай? Е) 11
144.Реакция ортасы бейтарап болғанда, сутектік көрсеткіш неге тең? D) 7
145.Қайсы затта күкірттің тотығу дәрежесі нольге тең? С) S
146.Хлордың тотығу дәрежесі -1-ге тең. A)HCl
147.Марганецтің тотығу дәрежесі +6-ғà тең қосылыс. С) K2MnO4
148.Тотығу дәрежесі тұрақты элемент. В) Al
149.Қай реакция тотығу-тотықсыздану реакциясына жатады? С)Zn+HCl®
150.Берiлген тотығу-тотықсыздану реакциясы нәтижесiнде қандай элементтер тотығу дәрежелерiн өзгертедi?Na2SO4+SiO2+C® Na2SiO3+CO2+SO2
D)S және C
151.Қышқылдық ортада жүретiн тотығу-тотықсыздану реакциясын көрсетiңiз.
В)Mg+H2SO4®
152.Сiлтiлiк ортада жүретiн тотығу-тотықсыздану реакциясын көрсетiңiз. D)Cl2+NaOH®
153.Тотығу (электрон берiп жiберу) процесiн көрсетiңiз. А)S+4®S+6
154.Тотықсыздану (электрон қосып алу) процесiн көрсетiңiз. Е)Cl+1®Cl-
155.Қай қосылыстағы селен (Se) тек тотықсыздандырғыш қасиетiн көрсетедi? В)H2Se
156.Қай қосылыстағы күкiрт әрi тотықсыздандырғыш, әрi тотықтырғыш қасиет көрсетедi? С)Na2SO3
157.Электрондық баланс әдiсiмен тотығу-тотықсыздану реакциясын теңестiрiп, тотықсыздандырғыштың моль санын табыңыз: H2S+Cl2+H2O®H2SO4+HCl А)1
158.Электрондық баланс әдiсiмен тотығу-тотықсыздану реакциясын теңестiрiп, тотықтырғыштың моль санын анықтаңыз: KMnO4+Zn+H2O=KOH+MnO2+Zn(OH)2 В)2
159.H2S+H2SO3®S+H2O тотығу – тотықсыздану реакциясын теңестiрiп, түзiлген күкiрттiң моль санын анықтаңыз. С)3
160.Қай зат тек тотықтырғыш қасиет көрсетедi?
D)MnO3 Е)KMnO4
161.Қай зат тек тотықсыздандырғыш қасиет көрсетедi? С)H2S
162.Тотығу дәрежесi “+4” болатын ионы бар қосылысты көрсетiңiз. D)Na2SO3
163.Берiлген схемадан тотығу процесiн көрсетiңiз.
А)NO2-®NO3-
164.Берiлген схемадан тотықсыздану процесiн көрсетiңiз. С)MnO4-®MnO2
165.Берiлген реакциядағы тотықсыздандырғыштың эквивалентi неге тең?K2Cr2O7+SnCl2+H2SO4® Sn(SO4)2+CrCl3+K2SO4 (M K2Cr2O7=294 г/моль; M SnCl2=190 г/моль). D)190/2
166.Реакция теңдеуiн аяқтап, тотықтырғыш алдындағы коэффициентiн анықтаңыз: KIO3+Na2SO3+H2SO4® В)2
167.Азоттың төменгi және жоғарғы тотығу дәрежесi неге тең? А)-3; +5
168.ClO3- ионы Cl- -на тотықсызданғанда қатысатын Н+ моль саны неге тең? Е)6
169.Тотықсыздану процесiн көрсетiңiз. D)O2®O22-
170. F2 молекуласының еселік байланысын және магниттік қасиетін анықтаңыз: В)1 – диамагнитті;
171.Орталық ионының тотығу дәрежесi “+6” болатын қосылысты көрсетiңiз. С)K2Cr2O7
172.Na2O2+CO2®Na2CO3+O2 реакцияның қай типiне жатады: D)диспорпорциалану
173.Тотықтырғышты көрсетiңiз: А)KMnO4
174.Mg0+HNO3®Mg(NO3)2+NH4NO3+H2O реакция теңдеуiн аяқтап, тотықсыздандырғыш алдындағы коэффициентiн анықтаңыз: В)4
175.Тотықсыздану процесiн көрсетiңiз. В)NO3-®NO
176.Тотығу процесiн көрсетiңiз. А)H3AsO3®H3AsO4
177.Тотықсыздану процесiн көрсетiңiз. А)MnO4-®MnO2
178.Тотығу процесiн көрсетiңiз. С)P2O3®H3PO4
179.KMnO4+H2S+H2SO4®MnSO4+K2SO4+S¯+H2O. Осы реакциядағы тотықтырғыштың моль санын табыңыз. А)2
180.KMnO4+NaNO2+H2SO4®MnSO4+NaNO3+K2SO4+H2O тотығу-тотықсыздану реакциясына қатысатын электрондар санын анықтаңыз. В)10
181.KMnO4+NaNO2+КОН®К2MnO4+NaNO3+H2O ТТР-дағы тотықтырғыштың моль санын табыңыз. В)2
182.Тотығу процесiнiң схемасын көрсетiңiз.
С)PbO2®Pb+2
183.NaBr+NaBrO3+H2SO4®Br2+Na2SO4+H2O ТТР-дағы тотықтырғыштың моль санын анықтаңыз. С)1
184.NaCrO2+PbO2+NaOH®Na2PbO2+Na2PbO2+Na2CrO4+H2O В)2
185.Төмендегi ТТРдың қайсысында тотықсыздандырғыштан тотықтырғышқа 8 электрон берiледi? С)K2Se+4NaNO3=K2SeO4+4NaNO2
186.Қай ТТР-да тотықсыздандырғыштан тотықтырғышқа 12 электрон берiледi?
В)4HMnO4=4MnO2+3O2+2H2O
187.Қорғасынның қайсы қосылысы тек тотықтырғыш қасиет көрсетедi? В)PbO2
188.Хлордың қайсы қосылысы тек тотықтырғыш қасиет көрсетедi? С)HClO4
189.Күкiрттiң қайсы қосылысы тек тотықсыздандырғыш қасиет көрсетедi? А)H2SO4
190.Қай металдың пластинкасы CuSO4 ерiтiндiсiнде тез еридi? D)Fe
191.Мырышты-күмiстi гальваникалық элементтiң стандартты Э.Қ.К. есептеңiз: φ0Zn2+/Zn=-0,76B. φ 0Ag+/Ag=+0,80B. В)-1,56
192.Қорғасын пластинкасы массасы қайсы тұз ерiтiндiсiмен әрекеттескенде азаяды? В)CuSO4
193.Mg(NO3)2 тұзы ерiтiндiсi электролизiнде анодта бөлiнетiн затты көрсетiңiз. С)O2
194.Егер катодта 5,6 л (қ.ж.) көлем сутегi бөлiнсе, натрий сульфаты ерiтiндiсi электролизiнде катод маңында түзiлетiн NaOH массасын анықтаңыз. D)20
195.Қай электродтың стандартты потенциалы нөлге тең деп алынады? В)сутектi
196.0,01М ZnSO4 тұзы ерiтiндiсiндегi мырыштың электрод потенциалын есептеңiз: φ 0Zn2+/zn=-0,76B.
С)-0,82
197.AuCl3 және KCl ерiтiндiсiнiң қоспасын электролиздегенде, электродта қандай заттар бөлiнедi? D)Au және Cl2
198.Гальваникалық элементтiң (Zn0/Zn2+//Mg2+/Mg0) электр қозғаушы күшi неге тең, егер φ 0Zn/Zn2+=-0,76B, φ 0Mg/Mg2+=-2,37B? В)+1,61
199.Фарадей заңы бойынша, электролиз кезiнде зат массасы қандай формуламен анықталынады?
С) 
200.AuCl3 ерiтiндiсiн 30 минут бойы электролиздегенде катодта 0,5 г Au бөлiну үшiн қажеттi ток күшiн анықтаңыз. С)0,4А
201.AgNO3 ерiтiндiсiн электролиздегенде анод маңында қайсы зат концентрленедi? В)HNO3
202.0,01М CuSO4 ерiтiндiсiндегi мыстың электродтық потенциалын (В) анықтаңыз: φ0Cu2+/Cu=+0.34B. С)+0,28
203.Бiрге болғанда қайсы металл катионы бiрiншi болып тотықсызданады? Е)Cu2+
204.FeCl3 ерiтiндiсi арқылы 2 минут бойы 1,5 А ток күшiн жiбергенде катодта темiрдiң қандай мөлшерi бөлiнедi? С)0,03 г
205.Мырыш ионы концентрациясы 0,01 моль/л-ге тең ерiтiндiге батырылған мырыштың электродтық потенциалы (φ, В) неге тең? А)-0,82
206.Ag/AgNO3 (0,001M)//AgNO3 (0,1M)/Ag гальваникалық элементтiң ЭҚК (В) есепте, егер φ0Ag/Ag+=+0,80В тең болса. С)0,12
207.Ток күшi 2,5 А электролит ерiтiндiсi арқылы 30 мин аралығында өткенде, ерiтiндiден 2,77 г метал бөлiнедi. Металл эквивалентiнiң молярлық массасы неге тең? В)59,4
208.2 моль су мөлшерiн 2А ток күшiмен ыдыратуға қанша уақыт (сағ-мөлшерiмен) қажет? А)53,6
209.Гидролизі қышқыл орта (рН<7көрсететін тұзды көрсетіңіз: С)MgCl2
210.Гидролизі сiлтiлiк орта (рН>7) көрсететін тұзды көрсетіңіз: В)Na2S
211.Келтiрiлген тұздардың қайсысы гидролизге ұшырамайды? D)LiCl
212.Магний пластинкасы қайсы тұз ерiтiндiсiнде тез еридi? С)Ag2SO4
213.Қайсы тұз гидролизi үш сатыда жүредi? В)AlCl3
214.Келтiрiлген металл катиондарының қайсысы бiрiншi болып катодта тотықсызданады? D)Cu2+
215.Келтiрiлген гальваникалық элементтiң қайсысында ЭҚК мәнi (стандартты жағдайда) жоғары болады? В)Zn0/Zn2+//Ag+/Ag0
216.MgCl2 ерiтiндiсiн электролиздегенде катодта бөлiнетiн зат: Е)H2
217.CuCl2 ерiтiндiсiн электролиздегенде катодта бөлiнетiн зат: А)Cu
218.Су құрамынан сутектi ығыстыра алатын металл:
А)Mg
219.Қай тұзды суда ерiткенде сiлтiлiк ортаны көрсетедi? D)K2S
220.Газ көлемiн қалыпты жағдайға келтiруде қолданылатын формула: Е) 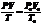
221.0,5 моль сутегiнiң (қ.ж.) көлемiн анықтаңыз. В)11,2
222.Эквиваленттер заңын көрсететiн формула:
С) 
223.11,2 л көмiртегi (IV) оксидiнiң қалыпты жағдайдағы мөлшерi нешеге тең? В)0,5
224.Мольдік көлемдi есептеуде қолданылатын формуланы көрсетiңiз. D) V = n•Vm
225.2 моль хлордың (Cl2) қалыпты жағдайдағы көлемi қандай? D)44,8
226.Массасы 2,8 г темiр қышқылдан 0,1 г сутегiн ығыстырып шығарады. Металдың эквивалентiнiң мольдік массасы неге тең? В)28
227.5,6 л азот оксидiнiң (NO) қ.ж. мөлшерiн (n) табыңыз? С)0,25 моль
228.Ауа бойынша газдың салыстырмалы тығыздығы 1,5 болса, осы газдың мольдік массасын табыңыз. Мауа=29 г/моль. C)44
229.Қай формула көмегiмен мольдік көлемдi есептеуге болады? D) V = nVm
230.Массалық үлесi 25% 200 г натрий нитраты ерiтiндiсiн дайындау үшiн неше грамм натрий нитратын (NaNO3) алу керек? В)25 г
231.Гомогендi реакция үшiн: 2NO(г)+O2(г)=2NO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз: С) V=K•C2NO•CO2
232.Гетерогендi реакция үшiн S(к)+O2(г)=SO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз: В) V=K•C(O2)
233.Берiлген реакция бойынша: Н3РО4+Са(ОН)2=СаНРО4+2Н2О фосфор қышқылы эквивалентiнiң мольдік массасын табыңыз: А)49
234.Газдың ауа бойынша салыстырмалы тығыздығы 2,21. Осы газдың молекулалық массасын табыңыз. D)64
235.СИ-жүйесiнде зат мөлшерiнiң өлшем бiрлiгi ретiнде не алынады? С)моль
236.Қайсысы дұрыс: “1 моль зат құрамында”:
В) 6,02*1023 структуралық бiрлiк
237.Заттың эквивалентiнiң молярлық массасының өлшем бiрлiгi қандай? А)г/моль
238.Кальций гидроксидiнiң молярлық массасының мәнiн көрсетiңiз MCa(OH)2. С)74г/моль
239.Азоттың қандай көлемiнде (қ.ж.) 6,02*1024 атом болады? А)22,4 л С)224 л
240.2 моль темiр сульфидiнiң (FeS) массасын көрсетiңiз. В)176 г
241.Күкiрт оксидiнiң (SO3) сутегi бойынша салыстырмалы тығыздығын көрсетiңiз. В)40
242.Массасы 1,7 кг аммиак (NH3) қ.ж. қандай көлем алады? А)2,24 м3
243.Сутегiнiң және оттегiнiң (қ.ж.) молярлық көлемiнiң мәнiн көрсетiңiз. А)11,2 л/моль және 5,6 л/моль
244.Газдың көлемiн қалыпты жағдайға келтiретiн формуланы көрсетiңiз. В) 
245.56 г азоттың (N2) қ.ж. моль санын көрсетiңiз. В)2,0
246.Массасы 2,8 г темiр қышқылдан 0,1 г сутегiн ығыстырады. Осы металдың эквивалентiнiң молярлық массасы (г/моль) тең болады. С)28
247.Х-затының молекуласының абсолюттiк массасы 7,3•10-22 грамға тең. Осы заттың салыстырмалы молекулалық массасы қандай? С)44,0
248.Қайсысында қ.ж. молекула саны көп болады? С)10 г NH3
249.Реакциядағы Н3РО4+Са(ОН)2=СаНРО4+2Н2О ортофосфор қышқылы эквивалентiнiң мольдік массасын көрсетiңiз. С)49
250.Қалыпты жағдайдағы қысымды көрсетiңiз:
В)101325 Па
251.Авогадро тұрақтысын көрсетiңiз: В)6,02•1023моль-1
252.Универсальды газ тұрақтысын көрсетiңiз:
А) 8,314 Дж/моль•К
253.Қалыпты жағдайдағы газдың мольдік көлемiн көрсетiңiз: В)224 л/моль
254.H2SO4-күкiрт қышқылының мольдік массасы қандай? В) M(H2SO4)=98 г/моль
255.CH3COONa – натрий ацетатының мольдік массасы қандай? В) M(NaCH3COO)=82 г/моль 256.Ca(OH)2 – кальций гидроксидiнiң эквиваленттiк массасының мәнiн көрсетiңiз:
D) МЭСа(ОН)2)=37 г/моль
257.Қай заттың эквивалентi ең азы? С)O2
258.Қай заттың эквивалентi ең көп? D)Na2SO4
259.Қай жағдайда Н2-нiң молекула саны көп? А)11,2 г Н2
260.0,5 моль күкiрт қышқылының массасы (г) қандай? M (H2SO4)=98 г/моль В)49 г
261.34 г аммиак (NH3) қалыпты жағдайда қандай көлем (л) алады? А)44,8 л
262.Эквивалент заңын өрнектейтiн өрнектi көрсетiңiз. А) Д= 
263.Клайперон теңдеуінің өрнегiн көрсетiңiз.
D) 
264.Газдың сутегiмен салыстырылып алынған тығыздығы 22, 1 л осы газдың қалыпты жағдайдағы массасын табыңыз. В)1,96
265.5 л газдың қалыпты жағдайдағы массасы 7,15 г. Осы газдың азотпен салыстырғандағы тығыздығын табыңыз. А)1,14
266.Реакция жылдамдығының температуралық коэффициентi неге тең, егер температураны 400С-ге жоғарылатқанда реакция жылдамдығы 81 есе артса?
С)3
267.Қайтымды реакцияның қайсысында, қысымды жоғарылатқанда тепе-теңдiк тура реакция бағытына ығысады? D)N2+3H2Û2NH3
268.Берiлген реакцияның 2NO(г)+O2(г)=2NO2(г) -жылдамдығы қалай өзгередi, егер көлемдi 3 есеге азайтса? D) 27 есе артады
269.Егер реакцияның температуралық коэффициентi 2-ге тең болса, реакцияның жылдамдығын 64 есе арттыру үшін температураны қанша градусқа арттыру керек? D)600С
270.Берiлген реакцияның N2(г)+3Н2(г) Û2NН3(г) жылдамдығы қалай өзгередi, егер жүйедегi қысымды 3 есе арттырса? С)81
271.Егер реакцияның температуралық коэффициентi 4-ге тең болса, температураны 400С-дан 800С-қа дейін көтергенде реакция жылдамдығы қанша есе артады? А)256
272.Аррениус теңдеуінің өрнегі: В)k= A.z.e-Ea/RT
273.2А+В®А2В –реакция жылдамдығы қалай өзгередi, егер А–заты концентрациясын 2 есе арттырып, ал В заты концентрациясын 2 есе азайтса? А) 2 өсе өседi
274.2А2(г)+В2(г)=2А2В(г)-реакциядағы А-заты концентрациясын 4 есе төмендету нәтижесiнде тура және керi реакция жылдамдығы өзгермеуi үшiн В2 заты концентрациясын неше есе арттыру қажет?
В) 16 есе
275.Келтiрiлген теңдеудiң N2+3Н2®2NН3 тура реакция жылдамдығының математикалық теңдеуi:
В) V=k1•CN2•C3H2
276.Темірдің массалық үлесі 70 процентке тең қосылыстың формуласын көрсет: D)Fe2O3 ;
277.Әрекеттесушi заттар концентрациясын арттырғанда реакция жылдамдығы: В)артады
278.2NO+O2®2NO2+Q-реакция тепе-теңдiгi солға қарай қай жағдайда ығысады? В)температураны көтергенде
279.Вант-Гофф ережесiне сәйкес, температураны әрбiр 100С-ке көтергенде реакция жылдамдығы:
В) 2-4 есе өседi
280.Келтiрiлген реакциялардан гомогендi реакцияны көрсет: D) N2(г)+3Н2(г) ®2NН3(г)
281.4HCl(г)+O2(г)®2H2O(г)+2Cl2(г) реакциясының жылдамдығы HCl концентрациясын 2 есе өсiргенде қанша есе өседi? D)16
282.3H2(г)+N2(г)®2NH3(г) реакциясының жылдамдығы сутегi концентрациясын 2 есе өсiргенде қанша есе өседi? D)8
283.Газдық фазада жүрiп жатқан реакцияның температурасын 320 дан 340К өсiргенде реакция жылдамдығы қанша есе өседi? g=3. Е)9
284.2NO(г)+O2(г)Û2NO2(г) жүйесiндегi қысымды 4 есе өсiрсе реакция жылдамдығы қанша есе өседi? Е)64
285.2SO2(г)+O2(г)Û2SO3(г) жүйесiнiң қысысымын 2 есе азайтқанда реакция жылдамдығы қалай өзгередi? D)8 есе кемидi
286.Температураны 500 ден 1000К өсiргендегi реакцияның активациялық энергиясын есептеп табыңыз. Жылдамдық константасы 105 есе өседi.
А)95,5 кДж/моль
287.Температураны 300С өсiргенде реакция жылдамдығы қанша есе өседi? Температуралық коэффициент g=2. А)8
288.Реакция жылдамдығын 81 есе азайту үшiн температураны қанша градусқа төмендету керек, егер g=3 болса? А)400
289.4NН3(г)+5NO2(г)=4NO(г)+6H2O(Бу) жүйесiнiң қысымын 2 есе өсiрсе реакция жылдамдығы қанша есе өседi? Е)512
290.Температуралық коэффициентi g=3 тең реакцияның температурасын 400 тан 600С өсiрсе реакция жылдамдығы қалай өзгередi? В)9 есе өседi
291.Тепе-теңдiк константасы Ктепе-теңдiк=  тең реакцияның схемасын көрсетiңiз. С)А+3ВÛС+2Д
тең реакцияның схемасын көрсетiңiз. С)А+3ВÛС+2Д
292.Fe3O4(қатты)+4CO(г) Û 3Fe(қатты)+4CO2 (г) тепе-теңдiкте тұрған реакция қысымын өсiрсе тепе-теңдiк қалай қарай ығысады? В)ығыспайды
293.С(қатты)+2N2O(г) Û CO2 (г) +2N2(г)+Q жүйесiндегi тепе-теңдiктi солға ығыстыру үшiн:
В)қысымды өсiредi
294.3H2(г)+N2(г) Û 2NH3(г) жүйесiндегi тепе-теңдiктi оңға, яғни аммиак түзiлу жағына ығыстыру үшiн:
А)қысымды өсiредi
295.2CO(г) +O2 (г) Û 2CO(г)+Q жүйесiндегi тепе-теңдiктi солға, яғни бастапқы заттар жағына ығыстыру үшiн: D)температураны өсiреді
296.Электрондық формуласы …4s24p3 –сәйкес элемент қай топта орналасқан? D)4
297.Келтiрiлген электрондық формулалардың қайсысы алюминий атомына (
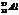 ) сәйкес келедi? В)3s23p1
) сәйкес келедi? В)3s23p1
298.Сыртқы электрон қабаты 3s23p4-сәйкес келетiн атом қандай терiс таңбадағы тотығу дәрежесiн көрсетуi мүмкiн? В)-2
299.“f”-электрон бұлты деңгейiндегi орбиталь санын көрсет: D)7
300.Электрондық формуласы …s2p3-сәйкес фосфор атомының қалыпты жағдайдағы Валенттiлiгiн көрсет. С)3
301.Магний ( ) атомындағы нейтрон саны: С)12
) атомындағы нейтрон саны: С)12
302.S2- -ионына сәйкес келетiн электрондық формула: А)3s23p6
303.Ереже бойынша, атомдарда 4р-деңгейiнен кейiн қай деңгейшеге электрондар толтырылады? D)5s
304.Бас квант саны мәнi n=4-ке тең атомда жалпы қанша электрон болуы мүмкiн? Е)32
305.1 л натрий сульфатында 0,5 моль сульфат бар. Осы ерітіндінің 1л қанша натрий ионы болуы мүмкін? Е) 6,02 . 1023
306.Келтiрiлген элементтер қатарында: Li, Be, B, C, N, F, Ne –иондану потенциалдар мәнi қалай өзгередi? С)бiрқалыпсыз өзгередi, бiрақ артуға мүмкiншiлiгi бар
307. Қай қосылыста күкіртттің массалық үлесі ең аз? В) K2SO4;
308.NH4+ ионы түзiлуi кезiнде қайсы атом немесе ионның электрон жұбы донор қызметiн атқарады? С)N
309.МО теориясы тұрғысынан келтiрiлген бөлшектердiң қайсысы тұрақты жағдайда болуы мүмкiн емес? D)Не2
310.N2-молекуласында қанша p-байланысы бар?
С) екi p-байланысы
311.BF3 молекуласындағы орбиталдардың гибридтену күйi: В) sp2
312.Сутектiк байланыс: D)электртерiстiлiгi жоғары элемент пен сутек арасында
313.Таза тек s- және p-бұлттарының бірлесуi нәтижесiнде түзiлген байланысы бар молекула: С) HCl
314.Байланыс аралығы 1200 болатын молекула:
D)AlCl3
315.Электрон жұбы арқылы түзiлетiн байланыс:
А)коваленттiк
316.HCl молекуласындағы химиялық байланыс түрiн көрсет: В)коваленттiк, полюстi
317.Келтiрiлген молекулалардың қайсысында орбиталдардың гибридтенуi жүредi? А)SiH4
318.Кеңiстiкте электрон бұлтының пiшiнiн көрсететiн квант саны қалай аталады: D)орбитальдiк
319.Элементтiң массалық саны көрсетедi:
 2018-01-21
2018-01-21 1549
1549







