Кіріспе
1780 жылы, француз зерттеушілер Антуан Lavuaze (1743 - 1794) және Пер Саймон Лаплас (1749 - 1827), олар калориметрия деп аталатын белгілі бір жылу өлшеу үшін құрылғыны, ұсынды.
Калориметр физикалық, химиялық немесе биологиялық процестер бөлінетін немесе сіңірілетін жылу мөлшерін өлшеуге арналған құрылғы аталды.
Әдетте, калориметр нақты жылу, жану булану және жылу жылу анықтау үшін пайдаланылады. ыдырайтын бейтарап пиондар, фотондар ағыны қалыптастыру - құрылғы қайталама бөлшектердің ұрпақ онда көміртегі нысанаға, тұрады. Олар нысанаға астында раковина және қорғасын арасында орналасқан детекторлардың қабаттарын жазылған. қайталама бөлшектердің мөлшерін өлшеу, бастапқы энергия анықталуы мүмкін. детекторлардың көп қабаттар, дәлірек өлшенеді энергия.
1750 жылы Петербург физигі - Георг Richman (1711 - 1753), М. В. Lomonosovym бірлесіп жұмыс жасап, су аралас тең сомалары түрлі температураны бар болса, қоспаның температурасы орташа температурасы бөліктері болады деп эксперимент жасады. Бұл эксперименттер Германияда Йоханнес Wilke арқылы 1772 жылы қайталанды. Бір дәрежесі бойынша су бірлік массасының температурасын өзгерту үшін қажетті жылу мөлшері сияқты калориялы - Wilke бірлік жылу мөлшерін кірді. Бұл біздің күнге дейін сақталған.
ХІХ ғасырдың ортасына дейін және «жылу мөлшеріне» тұжырымдамасы, «нақты жылу», «калориметрия», «Fusion жылу», «булану жылуы» енді (сөз «жасырын дейін сақталған - 100 жыл молекулалық-кинетикалық теориясы бәсекелес калориялық тұжырымдамасы жақында ғана оқулықтар беттерінде жоғалып кеткен. Бұл ұғымдар өзінде молекулалық-кинетикалық теориясының бейімделді.
XIX ғасырдың ортасынан бастап ол жылу механикалық теориясы ретінде белгілі болған теориясын дамытуда молекулалық теориясы энергия мен аванстар сақтау заңының ашылуы органдарының соқтығысқан молекулалардың механикалық қозғалыс беру үрдісі ретінде жылу процесінің тұжырымдамасын әкелді. Импульс беру газ тамырларының қабырғаларын бөлшектер ретінде газ қысым түсіндірілді. Температура бөлшектердің қозғалыс қарқындылығы қарым-қатынас бастады. Молекулалар кімнің қозғалыс классикалық механика заңдарына бағынады бөлшектердің ретінде қарастырылды.
1 Калориметр туралы жалпы мәлімет
Калориметр (латынша: calor - жылу, ыстық және метр) — әр түрлі физикалық, химиялық және биологиялық процестер кезінде денелерден бөлінетін немесе олардың қабылдайтын жылу мөлшерін өлшейтін аспап.
Қазіргі қоғамның даму жылдамдығы үнемі артып отырады. Өндірістің әртүрлі салалары технологияландырылуда, ғылым тәжірибелік мәндерді алу үшін ғана емес, оларды қңдеуде қолданылатын жетілген жаңа мәселелермен тоғысуда.
Органикалық заттар химиясы – органикалық синтездің «құрылыс блогы» - қарқынды даму жолында. Жоғары реакциялық қабілетке ие болғандықтан озық технология, медицина және ауыл шаруашылығы үшін ғылыми химиялық өнімдер өндірісінде химиялық дамудың заманауи үрдісіне жауап береді.
Органикалық синтез саласында ғалымдардың негізгі назары пайдалы қасиеттері алдын-ала белгілі заттардың технологиялық тиімді тәсілдерін табу және өңдеу сияқты мәселелерді шешуге аударылған. Көптеген жылдар бойы органикалық заттардың қасиеттерін анықтауға арналған зерттеулер маңызды болып келеді, себебі олардың синтетикалық мүмкіндігі мен болашағы зор және тәжірибелік қолдану салалары да кең. Мысалы, органикалық заттар түрлі биологиялық белсенділікке ие және олар полиэфирлі антибиотиктердің, полиэцитиленді көмірсутектердің, бактерицидтік препараттардыңижәне сұйық кристаллды заттардың синтезінде интермедиаттар болып табылады.
Сонымен бірге, органикалық қосылыстарды реакциялық қабілеттілігі жоғары полимерлер мен олигомерлердің, жылуға және қыздыруға тұрақты
материалдар синтезіндеикеңінен қолданылады. Органикалық полимерлер синтезінде қолдану бағалы қасиеттерге ие полимерлер алу саласында үлкен бетбұрысқа әкелді.
Органикалық қосылыстардың қасиеттерін анықтау бұрыннан белгілі болғанымен және бұл салада көптеген ғалымдардың зерттеулері жүргізілгеніне қарамастан, олардың қасиеттерін құрылымына ұштастыра отырып зерттеу, олардың алынуы, химиялық қасиеттері сияқты термодинамикалық қасиеттерін анықтау маңызды болып саналады.
Органикалық қосылыстар алдағы синтетикалық айналулардың маңызды қосылыстары болып табылады. Олар қатысатын көптеген синтездер белгілі.
Осы синтездердің негізгі кинетикалық және термодинамикалық өлшемдерін қарастыруда калориметрлік иәдіс ерекше орын алады.
Құрылысы теориялық және тәжірибелік мәніне әсер ететін болғандықтан, олардың физико-химиялық қаситтеріне, көбінесе термодинамикалық қасиеттеріне де әсер етеді. Сондықтан калориметрлік әдіс арқылы зерттеудің маңызы зор.
Калориметрияда қолданылатын аппараттар мен өлшеу әдістері әртүрлі болып келеді, себебі калориметрлік тапсырмаларды шешу зерттеліп отырған процеске және оны өткізу шарттарына сәйкес орындалады. Осы немесе басқа процестерде бөлінген (немесе сіңірілген) жылу мөлшерін анықтау арнайы құрылғы-калориметрде жүргізіледі. Өлшеуге тиісті барлық жылу таралатын калориметр бөлшектерінің жиынтығы калориметрлік жүйе деп аталады. Ережеге сәйкес калориметрлік өлшеу тәжірибе кезіндегі калориметрлік жүйенің температурасын бақылаудан тұрады. Көп жағдайларда «калориметрлік жүйе» сөзін қысқарту мақсатында «калориметр» терминін қолдану енгізілген. Осыған байланысты ол екі мағынада да қолданылады. Құралдардың калориметрлік әдістердің көптүрлілігіне байланысты калориметрлердің толық классификациясын атау мүмкін емес. Сондықтан калориметрия негіздерін қарапайым және көп қолданысқа ие калориметрлер құрайды. Оларды, көбінесе, белгісіне, температураның жұмыстық интервалына, реакциялық камера санына және т.б байланысты ажыратады. Калориметр, ережеге сай, өлшнетін жылу құбылыстары өтетін түтікше. Осы түтікшеде бөлінетін немесе сіңірілетін жылу калориметр температурасының өзгеруін тудырады. Нәтижесінде ішкі сыртқы жылу алмасу процесі жүреді.Жылу алмасу калориметрлік түтіктің беткі бөлігі (сыртқы қабықша) арасында жүреді. Екі қабықша арасында орнатылатын жылу ағыны W неғұрлым көп болса, соғұрлым температуралар айырымы DT ортаның
жылуөткізгіштігі L жоғары болады. Тұрақты температура режимінде
W=L•DT
Ом заңын еске түсіретін бұл теңдеуде L қолданыстағы прибордың негізгі қасиетін көрсетеді және калориметрдің әртүрлі класситфикациясы үшін қолданылады. Әсіресе, калориметрлер жұмысының жылу шарттары олардың классификациясының ортақ белгісі болып саналады.
2 Калориметрлер классификациясы мен құрылысы
Осы тұрғыдан калориметрия және микрокалориметрия бойынша жұмыстар анализдерін қорытындылау тұрғысынан қарасақ, калориметрдің кең таралған келесі түрлері белгілі: адиабаттық, изометриялық (тұрақты температурада), диатермиялық (ауыспалы температурада), жылу өткізетін және ағынды (өлшеудің жылу шарттары және реакциялық камераның сыртқы ортамен байланысуы бойынша).
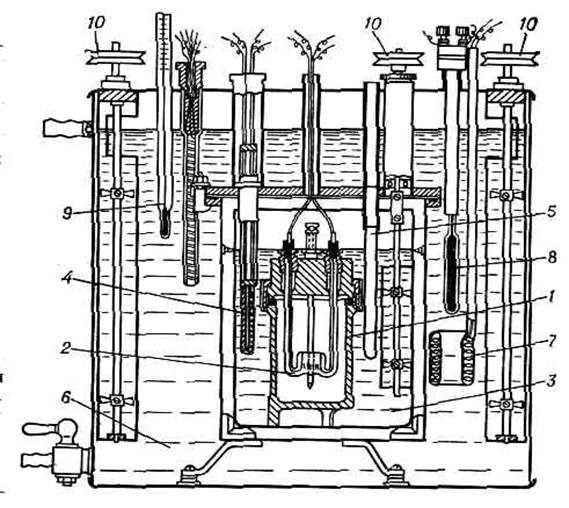
Қабықтың (схемасы): 1 - «калориметрлік. бомба; 2 - реакция қозғау үшін жылытқыш; 3 - іс жүзінде калориметр (сумен кеме); 4 - қарсыласу термометрі; 5 - тоңазытқыш (салқын ауаны өтті байқалғаны туралы түтік); жылы - изотермиялық. сумен толтырылған қабығы; 7 - жылытқыш қабықтың; 8 - байланыс термометр; 9 - бақылау термометр; 10 – механикалық араластырғышты. 1 сурет - Изотермиялық интеграторы сұйық калориметр. Адиабаттық калориметрлердереакциялық камера (калориметрлік жүйе) мен сыртқы орта арасында жылуалмасу болмады (немесе минималды).
Бұл жағдайда ішкі және сыртқы қабықша бір-бірінен термиялық изолятормен ажыратылған, сол себепті калориметр жылу өткізбейді. Мұндай шартта тәжірибе басында бөлінген жылу Q іс жүзінде калориметрдің ішіндегі құраушыларды жылытуға жұмсалады. Тәжірибе соңында калориметр температурасы бастапқыдан DT жоғары болады және Q=С•DT. Мұнда, С – калориметр жылусыйымдылығы. Бұл құрал тәжірибе кезінде бөлінетін барлық жылу мөлшерін қосатын интегратор болып табылады: реакция жылуы, механикалық араластыру, булану және т.б жылуалмасудың минималды шартын қамтамасыз ету үшін реакциялық камера мен калориметрдің сыртқы қабықша аралығын вакуумдейді. Бұл жағдайда бір немесе бірнеше қамтитын калориметрлік жүйе экранын пайдалану тиімді болып келеді. Өлшеу процесі кезіндегі температура калориметрлік жүйенің сыртқы бетіндегі температурамен бірдей ұсталынады. Температура теңдігін температуралар айырымы мен электрлік жылытқыш және терморегулятор көмегімен бақылап отырады. Іс жүзінде адиабаттық қабықшалар негізінен қоршаған ортаның төмен температурасында қолданылатын Дьюар түтікшелерімен жабдықталған. Бірақ олар бірнеше сағатқа созылатын тәжірибелерде пайдаланылмайды; сонымен қатар, Дьюар түтікшелерінің жылусыйымдылығы тәжірибе ұзақтылығына қарай таңдалады.
Алғаш рет француз ғалымы Персон ұсынған (1849) адиабаттық әдіс тәжірибеге Ричардспен енгізілген (1905) және ол қазіргі уақытқа дейін пайдаланылады. Бірақ адиабаттық калориметрлер жоғары инерцияға ие және өткізілетін тәжірибе уақытында өзгеретін температураға функцияланады. Нәтижесінде қалыпты жағдай үшін бөлінген жылудың нақты ритмін шығару қиын болады.
Төмен температурада жылу сыйымдылығын өлшеу үшін Адиабаталық калориметрия дәл калориметрия үшін аппаратының жақсы үлгісі болып табылады. Мұндай калориметрия қимасы сызба көрсетілген. Оның орталығында калориметр кеме болып табылады; содан кейін - Адиабаталық қалқан және вакуумдық контейнер; одан әрі - Дьюар кеме (криостата). вакуумды контейнер орталық түтікке бекітіледі; Адиабаталық экран қатты жіп немесе балық аулау желісі контейнерге ішіндегі тоқтатылды. контейнер ішіндегі кеңістік жақсы жылу оқшаулау үшін көшірілді отыр. Бұл түрі экранда ұйымдастырылған арнайы (қауіпсіздік) жылытқыштар, өйткені, ол 0,01 ° C (немесе одан кем) шеңберінде үшін калориметр температурасын тең сақталады, Адиабаталық калориметрия (оқшауланған) деп аталады. Жылу беру ғана калориметрия жылу ағып тасталады.
Жоғарыда сипатталған адиабаталық калориметрия классикалық дәлдіктегі калориметрияға жатқызуға болады. полимерлер ерекше жылу өлшеу кезінде көптеген үлгілері жеткілікті термодинамика өзгеріссіз болып келеді.. Көптеген жағдайларда, тек тұрақты және жеткілікті тез қыздыру режимі өлшеу процесінде нәтижесінде, үлгідегі қайтымсыз өзгертулерді болдырмауға болады. Қыздыру жылдамдығы шамамен 65 С температурада 1 және 2 C / мин арасында қол жеткізіледі.
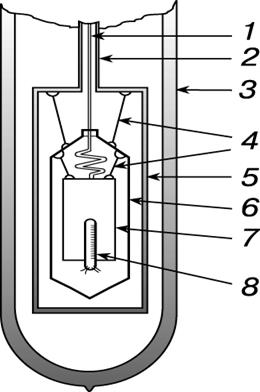
1 - калориметр толтыру үшін түтік; 2 - калориметр айдау үшін түтік; 3 - криостата (Дьюар кеме); 4 - жіп стенділер; 5 - вакуумдық контейнер; 6 - Адиабаталық экран; 7 - калориметр кеме; 8 - термометр жылытқыш. 2 сурет - Адиабаталық калориметрия
Изотермиялық калориметрлердекалориметр жылу өткізгіштігі L өте жоғары және жылу калориметрлерде жинақталмайды да, сыртқы ортаға тез тарап кетеді. Бұл жерде температуралар айырымы DTмөте аз. Оны өлшеу өте қиын әрі нақты емес. Сонымен қатар, оны есептеу маңызды емес. Бұл әдісте термометр емес бөлінген жылудың ағынға пропорционал мөлшерін өлшейтін құрал қолданылады. Изотермиялық калориметрлерде жылу мөлшерін өзінің агрегаттық күйін өзгерткен (балқыған қатты зат немесе буланған сұйықтық)
заттардың санына байланысты анықтайды. Изотермиялық калориметрлер ұзақ процестің жылулық эффектісін анықтау үшін кең қолданылады және арнайы тағайындауы бар. Аталған категориялы калориметрияға агрегаттық күйі өзгерген заттық мөлшері – энергия өлшемі болып табылатын калориметрлерді (мысалы, «мұздық» Бунзен калориметрі) жатқызамыз. Бірақ, осы типті калориметрге эндотермиялық жылу эффектісі электр энергиясына, ал экзотермиялық – Пельтье эффектісіне теңесетін калориметрлерді де жатқызуға болады.
Диатермиялық (ауыспалы температуралы) калориметрлердежылу мөлшері калориметрлік жүйе температурасының өзгеруімен анықталады. Әдетте, мұнда калориметрлік түтік немесе блок белгілі бір ұяшықта орналасады. Ол температура реттегішінің ортасында орналасады. Калориметрлік жүйені қоршайтын құралдар калориметрдің қбықшасын құрайды. Ауыспалы температуралы калориметрлерді жұмыс жасау режимі бойынша екіге бөлуге болады: изотермиялық қабықшалы және адиабатикалық қабықшалы калориметрлер. Калориметрдің сыртқы ортамен жжылу алмасу есебі өлшеу жүргізу режимімен анықталады. Мұндай типті калориметрлерге кондуктивті микрокалориметрлерді жатқызуға болады. Онда реакциялық камера мен термостат арасында жылуөткізгіштік коэффициенті белгілі зат немесе датчик орналасқан.
Дифференциалды сканирлеуші калориметрлер (ДСК), негізінен, ауыспалы температуралы, үздіксіз энергия енгізіліп отыратын, адиабатикалық режимде жұмыс жасайтын калориметр типіне жатады. Соңғы кезде ДСК кең қолданысқа ие болды, соған байланысты көп көлемде аспап жасаушы өндірісте шығарады және оны калориметрлік құралдың қарапайым түріне жатқызады.
Жылуөткізгіш калориметр немесе Кальве калориметрі сонымен қатар калориметрлердің арнайы типіне жатқызады. Оларда реакциялық камералар (екі немесе үш) дифференциалды қосылған термобатареялармен қоршалған. Калориметр жұмысы термоэлектрқозғаушы күшті өлшеуге негізделген. Термоэлектрқозғаушы күш термобатареяда реакциялық камерадан термостаттың калориметрлік блогына жылу ағынының өту кезінде пайда болады. Мұнда калориметрлік реакциялық камераның температурасы аздап өзгереді, бірақ бұндай калориметрлерді диатермиялық немесе изотермиялық деп атауға болмайды. Сондықтан осындай типті калориметрлер жылу ағынды калориметрлер деп аталады.
Ағынды калориметрлерде(ереже бойынша оларға микрокалориметрлер жатады) жылу эффектісі қыздыру немесе суыту үшін реакциялық камерадан алынатын газдың немесе сұйықтықтың белгілі салыстырмалы жылусыйымдылығымен анықталады.
Жоғарыда келтірілген негізгі калориметрлердің типтеріне қысқаша мәлімет олар туралы толық ақпарат бермейді, бірақ кең таралған калориметрлер болып саналады.
Ғылыми термохимиялық зерттеулердің ерекшелігі, зертханалық тәжірибеде- ауыспалы температуралы калориметрлер кең қолданылады. Ауыспалы температуралы калориметрлер өлшемі, құрылымы, белгісі және т.б бойынша бірнеше типке бөлінеді.
Сұйықтықты калориметрлердің негізгі бөлігі болып оның калориметрлік түтікшесі табылады. Ол сұйықтықпен толтырылған және зерттеулер үшін реакциялық камераны орналастырады. Егер зерттеу бөлме температурасында өткізілетін болса, онда, сұйықтық ретінде кәдімгі су алынады. Сулы еріткіштер мен органикалық сұйықтықтар сирек жағдайларда қолданылады.
Массивті немесе анероидты калориметрлерде энергияны өлшейтін орта ретінде массивті блок алынады. Ол жоғары температураға тұрақты металлдан (әдетте, мыс, алюминий немесе күміс) жасалады. Массивті калориметрлер жлғары температуралы химиялық зерттеулерде көп пайдаланылады.
Сұйықтықты және массивті калориметрлер қос және
Дифференциалды болуы мүмкін. Қос калориметрлерде калориметрлік түтіктің біреуі ондағы процессті жүргізу үшін қолданылса, екіншісі энергияның белгілі немесе белгісіз мөлшерін салыстыруға арналған. Мысалы, жұмыс калориметрлік жүйеде химиялық реакция жүрсе, екінші жүйеде бірдей қыздыру жылдамдығына ие бола отырып электрлік тоқпен қыздырады.

1 - калориметр, 2 - сусымалы материал, 3 - жылу изоляциялық цилиндр, 4 - қақпақ, 5 - термометр, 6 - су құйылған бак, 7 - бу ыдысы, 8 - түтік, 9 - электр қыздырғыш, 10 - электр айыры, 11 - электр сымы, 12 - бак мойыны, 13 - тығын, 14 - деңгей көрсеткіш, 15 - бу щығатын тесік, 16 - винт, 17 – бұлғауыш.
3 сурет - Сусымалы денелердің жылуөткізгіштігін анықтау қондырғысы
3 Калориметрлердің жұмыс істеу принципі
Протолиттік реакциялар түсінігін қышқыл-негіздік әрекеттесу деп түсінеміз, онда Бренстед-Лоури қышқыл-негіздік теориясына сәйкес, қышқыл рөлін протон беретін қосылыстар, ал негіз рөлін протон қабылдағыш қосылыстар атқарады. Қарапайым протолиттік процесстің элементарлы акты болып протондық ауысу кезеңі болып табылады. Белл бойынша, берілген жағдайда стериялық фактордың көптеген әсеріндегі протонның, және практикалық әрекеттесуші бөлшектердің байланыстырушы электрондардың қайта бөлінуі жүрмегенде осы акттың элементарлығы элементарлық бөлшектің ауысуы болып табылады. Бірақ, берілген нақтылау күшті қышқылдардың сулы ерітінділері үшін қолданылатынын атап өту керек. Ал сулы емес ерітінділерде көбінесе протондық ауысу процесіне қарағанда аралық комплекстердің пайда болуы бірінші болады, және реакцияға деген стериялық талаптар айтарлықтай жоғарылайды және анықтаушы мәнге ие болады.
Протондық ауысуға қарағанда молекулааралық протондық ауысудың реакциясы күрделі әрекеттесу болып табылады. А.И.Бродский бойынша, протондық ауысу процесі «кооперативтік» механизмге ие.
Қазіргі уақытта молекулааралық протондық ауысу кезінде сутектік байланыс арқасында аралық циклдық комплек (СБЦК) түзілудің қатал дәлелдері жоқ, бірақ оның болуы көптеген квантты химиялық есептеулердің нәтижесінде айқындалған болатын.Протондық ауысудың жылдамдығы сұйықтардағы диффузия жылдамдығымен тең екені атап өтілген болатын, ол ауысу жылдамдығы реагенттердің қышқылдығына және сондай-ақ реакцияға қатысатын гетероатомдардың электродонорлық қабілеттілігімен байланысты болуымен түсіндіріледі.
Калориметр градуировкасы
Калориметр градуировкасы энергия мөлшері арасындағықатынасты орнатудан тұрады. Энергия мөлшері калориметрлік жүйеден алынады және онда күйі өзгереді (көбінесе температура, сирек-масса, көлм және т.б). Төменде калориметрлердің кейбір түрлерінің градуировкасына мысалдар келтірілген. Кең қолданысқа ие болғандықтан ауыспалы тепературалы калориметрлер градуировкасына көп көңіл бөлінеді.
Калориметрге қажетті энергияның мөлшерін жеткізу үшін (калориметрді калибрлеу) келесі екі әдістің біреуін қолданады:
-жұмсалған электр энергиясын нақты өлшеу арқылы калориметрлік жүйені электр тогымен жылумен қыздырады («Джоуль» жылумен калибровка);
-жылу эффектісі нақты белгілі процесті калориметрде жүргізу (көбінесе химиялық реакция).
Электр тогымен градуировка-ауыспалы температуралы калориметрлердің кең таралған әрі әмбебап градуировка әдісі. Осындай әдісті қолдану үшін, қазіргі заманғы калориметрлер электр қыздыру аспаппен жабдықталады. Калориметрге жеткізілген энергия көлемін келесі теңдеу анықтайды:
Q=I2•R•t,
Мұнда, Q-энергия мөлшері, Дж; I-ток күші, А; R-қыздыру кедергісі, Ом; t-токты жіберген уақыт, сек.
Қазіргі уақытта, электр өлшемдері уақыт сияқты нақты өлшенеді. Әсіресе осы жағдайда электрлік градуировканың кең қолданысын қамтамасыз етеді.
Электр тогымен градуировка температураны4 2рт8рл3 диапазонында жылусыйымдылықты анықтауда қолданылады. Ол үшін калориметр контейнерді қыздырғыш көмегімен қыздырамыз. Тәжірибенің әр сатысында калоиметрге енгізілген электр энергиясы мен калориметр температурасының өзгерісін өлшейді. Өлшеу зерттеудің барлық температуралар интервалында жүргізіледі. Егер бос контейнердің жылу мәні W белгілі болса, алынған мәліметтер бойынша контейнердің ішіндегі заттың жылусыйымдылығын есептейді. Бұл жағдайда калориметр градуировкасын есептеу температураның барлық интервалында осы шаманың есептеуіне әкеледі.
5 Калориметрлік әдістерінің жалпы сипаттамасы
Практикада әдетте жартылай эмпирикалық және эмпирикалық емес әдістер қолданылады. Олар кванттық химияның негізгі теңдеулеріндегі электрондардың өзара және электрондар мен атомдық ядролардың әрекеттесуін сипаттайтын матрицалық элементтерді анықтау әдісімен ерекшеленеді. Осы мақсат үшін жартылай эмпирикалық әдістерде жуықталған эмпирикалық формулалар және эксперименттен белгілі атомдық параметрлер қолданылады. Эмпирикалық емес әдісте матрицалық элементтердің тікелей аналитикалық есептеулері жүргізіледі. Маман емес адамдарға «эмпирикалық емес» атауына синоним «тура» сөзі болып табылады, бірақ шынында олай емес. Эмпирикалық емес әдісте жуықталған болып табылады, пайдаланылған базистің толық еместігіне байланысты. Көптеген эмпирикалық емес есептеулерді үлкен емес және орташа базисте жүргізеді. Бұл есептің нәтижесіне айтарлықтай қателік туғызады, өйткені мұндай базистік жиындар молекуладағы электрондық тығыздықтың таралуының кейбір ерекшеліктерін бере алмайды. Нәтижесінде барлық молекулалардың параметрлері аздаған қателікпен анықталады. Мүмкіндігінше (уақыттың көп кетуінен мұны практикада жасау өте қиын) өте үлкен базистарды қолдануға болар еді, олар хФ-ның шектеуіне жетуге қамтамасыз етеді, онда базистік орбитальдің өсу саны алынған нәтижелеріне жетпейді. Бұндай жағдайда да Шредингер теңдеуінің нақты шешімін таба алмаймыз. Шредингер теңдеуінің нақты шешімін табу үшін электрондық корреляцияны ескеру қажет.
Қорытынды
Калориметрлік әдіс әртүрлі физикалық, химиялық және биологиялық процесстермкезінде денелерден бөлінетін немесе олардыңқабылдайтын жылу мөлшерін анықтауға негізделген.
Калориметрияда қолданылатын аппараттар мен өлшеу әдістері әртүрлі болып келеді, себебі калориметрлік тапсырмаларды шешу зерттеліп отырған процеске және оны өткізу шарттарына сәйкес орындалады. Осы немесе басқа процесстерде бөлінген немесе сіңірілген жылу мөлшерін анықтау арнайы құрылғы-калориметрде жүргізіледі. Өлшеуге тиісті барлық жылу таралатын калориметр бөлшектерінің жиынтығы калориметрлік жүйе деп аталады. Ережеге сәйкес калориметрлік өлшеу тәжірибе кезіндегі калориметрлік өлшеу тәжірибе кезіндегі калориметрлік жүйенің температурасын бақылаудан тұрады. Көп жағдайларда «калориметрлік жүйе» сөзін қысқарту мақсатында «калориметр» терминін қолдану енгізілген. Осыған байланысты ол екі мағынада қолданылады. Құралдардың калориметрлік әдістердің көптүрлілігіне байланысты калориметрлердің толық классификациясын атау мүмкін емес. Сондықтан калориметрия негіздерін қарапайым және көп қолданысқа ие калориметрлер құрайды. Оларды, көбінесе, белгісіне, температураның жұмыстық интервалына, реакциялық камера санына және т.б байланысты ажыратады.
Пайдаланылған әдебиеттер тізімі
1 Кабашев Р. А., Кадырбаев А.К., Кекилбаев А. М Жылутехникасы. Оқулық - Алмат: «Бастау» баспаханасы, 2008.-425б.
2 Матулис В.Э Прикладная квантовая химия
3 Бочарова А.В ЭПР-спектроскопия и квантовая химия реакций протонного и электронного переносав семихинонных радикалах: дис.... канд.хим.наук: 02..00.04;
 2017-11-01
2017-11-01 2396
2396






