Для синтеза нуклеиновых кислот, коферментных нуклеотидных группировок ферментов, макроэргических нуклеозидполифосфатов необходимы пуриновые и пиримидиновые нуклеотиды. Продуктами их первичного синтеза являются соответствующие рибонуклеотиды, из которых в дальнейшем в результате восстановительных реакций образуются дезоксирибонуклеотиды.
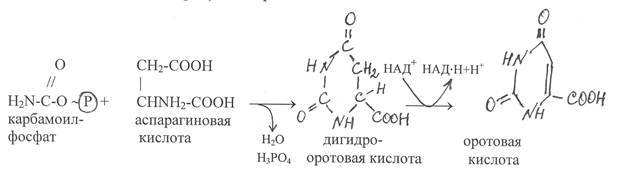 |
Пиримидиновые рибонуклеотиды синтезируются из аспарагиновой кислоты и карбамоилфосфата, на образование которого используются аммонийный азот, бикарбонат-ионы и молекулы АТФ (стр. …). Под действием фермента карбамоилтрансферазы карбамоильная группировка карбамоилфосфата переносится на остаток аспарагиновой кислоты и в результате отщепления молекулы воды из указанных компонентов синтезируется молекула дигидрооротовой кислоты. На следующем этапе дигидрооротовая кислота окисляется флавиновым ферментом, который отщепляет от неё атомы водорода и переносит их на окисленные динуклеотиды НАД+. В результате этой реакции образуется оротовая кислота:
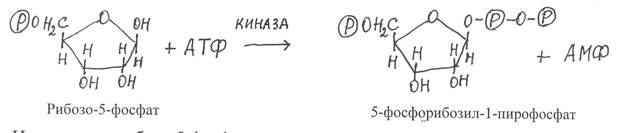
Далее в реакции вступает рибозо-5-фосфат, который вначале активируется путём фосфорилирования от АТФ и превращается в 5-фосфо-рибозил-1-пирофосфат:
Источником рибозо-5-фосфата для синтеза нуклеотидов служат реакции цикла Кальвина и пентозофосфатного цикла.
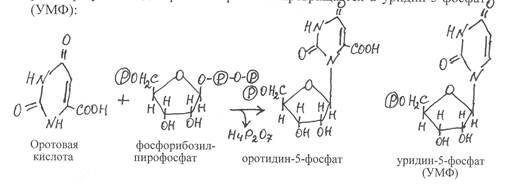 |
Образовавшийся фосфорибозилпирофосфат при взаимодействии с оротовой кислотой даёт первичный нуклеотид – оротидин-5-фосфат, который в результате декарбоксилирования превращается в уридин-5-фосфат (УМФ):
В ходе реакций фосфорилирования из УМФ синтезируются УДФ (уридиндифосфат) и УТФ (уридинтрифосфат):
|
Необходимый для синтеза РНК ЦТФ (цитидинтрифосфат) образуется из УТФ в результате аминирования азотистого основания в составе нуклеотида. Донором аминной группы служит амидная группировка гдутамина. Реакция аминирования сопряжена с гидролизом АТФ до АМФ.
Исходным соединением для синтеза пуриновых нуклеотидов, как и пиримидиновых, служит фосфорибозилпирофосфат, к которому присоединяются радикалы глутамина, глицина, аспарагиновой кислоты, углеродсодержащие группировки СО2, формил- и метенилтетрагидрофолиевой кислоты. В ходе довольно сложных превращений постепенно в соединении с фосфорибозильным радикалом строится структура азотистого основания. На ряде этапов построение гетероциклической группировки азотистого основания сопряжено с гидролизом АТФ.
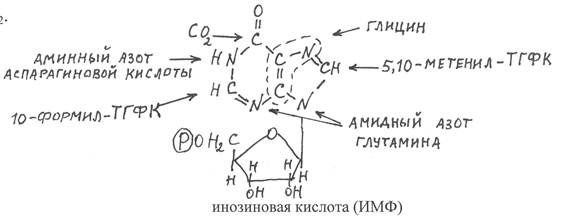
Первичным пуриновым нуклеотидом, который синтезируется в процессе указанных выше превращений, является инозиновая кислота (ИМФ). Два атома углерода азотистого основания ИМФ гипоксантина включены в его гетероциклическую группировку из молекул глутамина (амидный азот), один атом азота из аспарагиновой кислоты и ещё один атом азота из аминной группы глицина. Кроме того, глицин является также донором двух атомов углерода. Ещё два атома углерода гипоксантина происходят от от формильных группировок 5,10-метенилтетрагидрофолиевой кислоты (5,10-метенил-ТГФК) и 10-формилтетрагидрофолиевой кислоты (10-формил-ТГФК). Донором карбонильной группы гипоксантина является СО2.
 |
В результате аминирования от аспарагиновой кислоты в ходе двухэтапного превращения из инозиновой кислоты синтезируется адениловая кислота. В связи с тем, что эта реакция эндергоническая, она сопряжена с гидролизом ГТФ. При окислении инозиновой кислоты НАД-зависимой дегидрогеназой происходит её превращение в ксантиловую кислоту, которая далее в результате аминирования от глутамина и сопряжённого гидролиза АТФ образует гуаниловую кислоту (ГМФ).
Из соответствующих монофосфатов далее синтезируются дифосфат- и трифосфатпроизводные пуриновых нуклеотидов. АДФ и АТФ образуются в результате субстратного или окислительного фосфорилирования АМФ:
|
По аналогичной схеме в результате фосфорилирования от АТФ из ГМФ синтезируются ГДФ и ГТФ:
|
Таким образом, нами рассмотрены механизмы образования пиримидиновых и пуриновых рибонуклеотидов и их трифосфатпроизводных, необходимых для синтеза рибонуклеиновых кислот и использования в качестве макроэргических соединений.
Дизоксирибонуклеотиды образуются из дифосфатпроизводных (у некоторых организмов из трифосфатов) рибонуклеотидов при их восстановлении ферментом рибонуклеотидредуктазой, который переносит ко второму углеродному атому рибозы водород от восстановленной формы белка тиоредоксина.
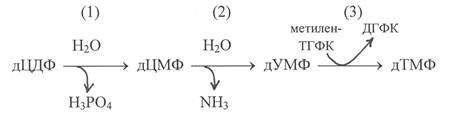 |
Более сложным путём осуществляется синтез дезокситимидиловой кислоты. У эукариотических организмов исходным соединением для её образования служит дезоксицитидиндифосфат (дЦДФ). Превращение дЦДФ в дезокситимидиловую кислоту (дТМФ) осуществляется по следующей схеме:
В первой реакции происходит гидролитическое отщепление от дЦДФ фосфорной кислоты, во второй реакции – дезаминирование цитозиновой группировки в составе нуклеотида и превращение её в остаток урацила. Более сложное превращение происходит на третьем этапе, которое катализирует фермент тимидилатсинтетаза. Под действием этого фермента осуществляется метилирование остатка урацила в нуклеотиде с участием метилентетрагидрофолиевой кислоты и превращение его в остаток тимина.
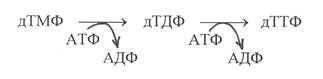 |
В результате последующего фосфорилирования от АТФ дТМФ образуется дизокситимидинтрифосфат (дТТФ), необходимый для синтеза ДНК:
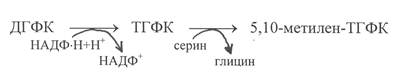 |
Важным этапом в синтезе дезокситимидиловой кислоты является обратное превращение дигидрофолиевой кислоты в метилентетрагидрофолиевую кислоту. На первом этапе дигидрофолиевая кислота восстанавливается в тетрагидрофолиевую кислоту под действием фермента дигидрофолатредуктазы. Донорами электронов и протонов в этой реакции служат восстановленные динуклеотиды НАДФ×Н. А далее уже другой фермент серинтрансоксиметилаза переносит на тетрагидрофолиевую кислоту формильный остаток от серина, превращая последний в глицин.
Ферменты тимидилатсинтетаза и дигидрофолатредуктаза, существенно влияющие на скорость образования тиминовых нуклеотидов, являются активными инициаторами синтеза ДНК. При понижении их активности замедляется или прекращается образование дезокситимидиловой кислоты, что далее вызывает прекращение синтеза ДНК. Подбирая эффективно действующие ингибиторы этих ферментов, можно при необходимости направленно подавлять синтез ДНК в клетках организма. Такие ингибиторы положены в основу химиотерапии рака, так как способны подавлять развитие раковых клеток, в которых интенсивно происходит синтез ДНК.
 2014-01-31
2014-01-31 1171
1171
