Для нагревания до 300 0С реакционных сосудов и для упаривания растворов используются бани. Колбонагреватели применяются чаще всего для нагрева горючих и легковоспламеняющихся жидкостей в колбах.
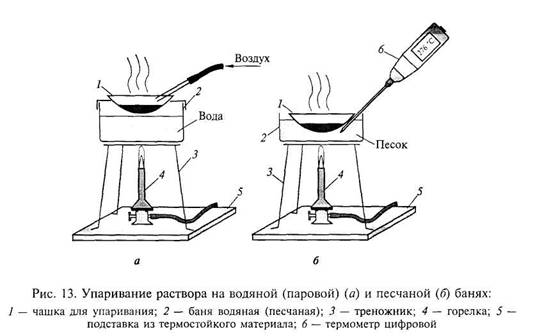
Водяная баня (рис. 13, а) представляет металлический сосуд 2, закрытый рядом колец разного диаметра. Такие бани удобны для упаривания растворов. Чашка 1 с упариваемым раствором не касается поверхности воды и обогревается водяным паром. Колбу, наоборот, частично погружают в воду.
В сосуд 2 наливают воду, не более 2/3 его объема, и помещают на треножник 3, стоящий на подставке 5 из термостойкого материала. Чашку 1 для упаривания ставят сверху, сняв такое количество колец, чтобы чашка была утоплена примерно на 2/3 (рис. 13). Воду в бане доводят до кипения на пламени горелки 4 и поддерживают в состоянии слабого кипения в течение всего опыта, добавляя новые порции по мере выкипания. Уровень воды в бане не должен изменяться. Используются бани с газовым или электрическим обогревом. Для ускорения испарения рекомендуется обдувать поверхность упариваемого раствора струей воздуха из стеклянной трубки (см. рис. 13, а).
Для подогрева реакционных сосудов и пробирок в качестве водяной бани иногда берут обычный химический стакан. В этом случае нагреваемый объект частично погружают в воду.
Песчаную баню (рис. 13,5) применяют для нагрева веществ до 200 – 300 0С и упаривания растворов. Она представляет металлический сосуд (противень) 2, заполненный чистым прокаленным песком. Песок нагревают пламенем газовой горелки 4 или электрическим нагревателем.
Температуру измеряют цифровым термометром 6 с длинным щупом.
Электрические печи
Для нагревания или прокаливания при высокой температуре используют электрические печи с терморегуляторами: трубчатые (рис. 14, а), тигельные (шахтные) (рис. 14, б) и муфельные (рис. 14, в).
Трубчатые печи применяют для проведения реакций в токе газов. Вещества в фарфоровой, кварцевой или металлической лодочке вносят в кварцевую или фарфоровую трубку, помещенную в трубчатую электрическую печь. Для прокаливания небольшого количества вещества в тиглях наиболее удобны тигельные (шахтные) печи. Большие количества веществ прокаливают в муфельной печи.

3 Проведение химического эксперимента
Взвешивание
Химический эксперимент начинается с подготовки исходных реагентов (взвешивания, смешения веществ, приготовления растворов), подготовки посуды и сборки прибора (если необходимо) и завершается выделением и идентификацией полученных веществ.
В студенческом практикуме применяют весы с точностью взвешивания 0,1 – 0,01 г, достаточной при проведения большинства опытов и синтезов, и пределом взвешивания 200 – 300 г. Для более точных взвешиваний, например, при проведении химического анализа, необходимо использовать аналитические весы с точностью взвешивания ±0,2 мг.
Правила взвешивания
Взвешивание неагрессивных веществ. Взвешивание на весах (рис. 15) всегда проводят с использованием тары. Химические вещества никогда не помещают прямо на чашку весов. В качестве тары используют стаканчики для взвешивания или бюксы (см. рис. 15, а, б). Допускается взвешивание на часовом стекле. Фарфоровые чашки использовать не рекомендуется – они слишком тяжелы.

Для взятия небольших навесок неагрессивных веществ можно использовать кальку. Другая бумага, особенно фильтровальная, в качестве тары при взвешивании не пригодна, так как часть вещества неизбежно к ней прилипнет. Кроме того, масса бумаги зависит от влажности окружающего воздуха. Не допускается взвешивание нагретых или горячих предметов.
Взвешивание агрессивных веществ. Агрессивные вещества взвешивают только в закрытых бюксах (см. рис. 15, б). Ампулы, пробирки и приемники с полученным веществом взвешивают в стеклянном стакане (рис. 16).
Взятие навесок сыпучих веществ. Взвешивание проводят следующим образом.
Стаканчик для взвешивания поместите на чашку весов и запишите его массу ли обнулите показания весов (нажмите клавишу «тара»).
 Снимите стаканчик с чашки весов, поставьте на лист чистой бумаги, насыпьте в него взвешиваемое вещество (см. рис. 15, в) и верните обратно на весы. Если масса вещества не соответствует заданной, то стаканчик с веществом вновь снимите с чашки весов и добавьте (или отберите) необходимое количество вещества. Для взятия точной навески допускается добавлять на весах небольшое количество вещества маленьким шпателем.
Снимите стаканчик с чашки весов, поставьте на лист чистой бумаги, насыпьте в него взвешиваемое вещество (см. рис. 15, в) и верните обратно на весы. Если масса вещества не соответствует заданной, то стаканчик с веществом вновь снимите с чашки весов и добавьте (или отберите) необходимое количество вещества. Для взятия точной навески допускается добавлять на весах небольшое количество вещества маленьким шпателем.
(При взвешивании не насыпайте вещество в тару над весами (см. рис. 15, е), так как вещество может попасть на весы и загрязнить их. В этом случае необходимо тотчас же выключить весы и протереть их и лишь затем повторить взвешивание.)
3.2. Измерение объема жидкости
При проведении химического эксперимента количество жидкости обычно определяют по ее объему при известной плотности, а не взвешивают. Для измерения объема жидкости используют мерные цилиндры и мерные пипетки (см. рис. 6). Так, например, если по уравнению реакции необходимо взять 0,62 г брома (ρ = 3,102 г/см3), то нужно взять мерную пипетку с делениями подходящей емкости и отмерить 0,2 мл брома.
 2018-02-13
2018-02-13 1623
1623








