Распульповка
Поступило:
- кек (r = 1,5 г/см3) в количестве 1550 кг влажностью 50 % от массы сухого (в т.ч. 23,25 кг Мо) или 1033,4 л;
- раствор с доукрепления в количестве 310 кг (в т.ч. 1,51 кг Мо) или 249,6 л;
Отношение Т:Ж на выщелачивании должно быть Т:Ж = 1:0,8, следовательно масса пульпы будет:
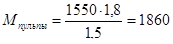 кг
кг
Плотность пульпы:
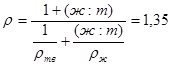 кг/м3 (19)
кг/м3 (19)
Для разложения молибденита требуется азотной кислоты:
MoS2 + 6HNO3 = H2MoO4 + NO + 2H2SO4 (20)
Молибдена в кеке в сульфидной форме 20 %, что составляет 4,65 кг Мо.
Масса МоS2:
Мо 96 кг – MoS2 160 кг
Мо 4,65 кг – х
х = 8,25 кг
Остальные 19,81 кг Мо в окисленной форме.
По реакции на 1 моль молибденита затрачивается 6 моль азотной кислоты, следовательно для разложения молибденита потребуется 290,6 моль азотной кислоты, что составляет 29 кг. Избыток 100 % от СНК следовательно масса азотной кислоты составляет 58 кг.
Для соблюдения Т:Ж = 1: 0,8, необходимо добавить раствора:
 кг.
кг.
Материальный баланс распульповки представлен в таблице 11.
Таблица 11 – Материальный баланс приготовления пульпы
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Кек | 1550,00 | 23,25 | 911,77 |
Пульпа 1 |
1860,00 |
24,76 |
1208,00 |
| Раствор с доукрепления | 310,00 | 0,51 | 249,60 | ||||
| Итого | 1860,00 | 24,76 | 1161,37 | Итого | 1860,00 | 24,76 | 1208,00 |
Выщелачивание
Основные реакции выщелачивания – (1) (22).
MeMoO4 + H2SO4 = MeSO4 + H2MoO4 (22)
Поступило:
- пульпа (Т:Ж = 1:0,8) в количестве 1860 кг (в т.ч. 24,76 кг Мо) или 1208,00л.
Необходимое количество азотной кислоты по реакции (22) 58 кг
Количество MeMoO4:
Мо 96 кг - MeMoO4 252
19,81 кг – х
х = 52,00 кг
Количество серной кислоты на реакцию 22:
MeMoO4 252 кг – H2SO4 98 кг
52 кг – х
х = 20,22 кг
Вскрытие кека составляет 90%, следовательно в раствор не перешло 2,476 кг Мо. Т.е. масса твердой фазы пульпы составит 979,11 кг.
Количество образовавшейся серной кислоты:
MoS2 160 кг – HNO3 378 кг
6,975 – Х
Х = 16,47 кг
Остаточная масса серной кислоты после выщелачивания:
Мост = 880,89 . 0,002 = 17,62 кг
Суммарное количество серной кислоты:
 кг
кг
Количество образовавшегося NO:
HNO3 63 кг – NO 30 кг
16,47 кг – х
х = 7,84 кг
Количество пульпы после выщелачивания:
1860 – 7,84 = 1852,16 кг или 1202,8 л.
Масса твердой фазы составляет: 979,11 кг, а масса жидкой фазы: 873,05 кг
Материальный баланс автоклавного выщелачивания представлен в таблице 12.
Таблица 12 – Материальный баланс автоклавного выщелачивания
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Пульпа 1 | 1860,00 | 24,76 | 1208,00 | Пульпа 2 | 1852,16 | 24,76 | 1202,80 |
| Газы | 7,84 | - | 5850,75 | ||||
| Итого | 1860,00 | 24,76 | 1208,00 | Итого | 1860,00 | 24,76 | 7053,55 |
Разбавление
Поступило:
- Пульпа 2 в количестве 1852,16 кг (в т.ч. 24,76 кг Мо) или 1202,8 л;
- маточный раствор после промывки (ρ = 1,01 г/см3).
Получено:
- пульпа 3 (в т.ч. 25,22 кг Мо);
Количество маточного раствора:
После выщелачивания отношение составляет: Т: Жпульпы2 = 1:0,9
После разбавления отношение Т: Ж, должно составить Т: Ж = 1:1,25
Значит воды нужно добавить: 1,25 – 0,9 = 0,35 частей или:
0,35 ×873,05 = 305,57 кг
Итого суммарная масса жидкой фазы составит:
873,05 + 305,57 = 1178,62 кг
Масса пульпы 3 составит 2157,73 кг или 1508,73 л.
Материальный баланс разбавления, представлен в таблице 13.
Таблица 13 – Материальный баланс Разбавления
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Пульпа 2 | 1852,16 | 24,76 | 1202,80 | Пульпа 3 | 2157,73 | 25,22 | 1508,37 |
| Маточный раствор | 305,57 | 0,46 | 305,57 | ||||
| Итого | 2157,73 | 25,22 | 1508,37 | Итого | 2157,73 | 25,22 | 1508,37 |
Сорбция
Поступило:
- Пульпа 3 (ρ = 1,39 г/см3, рН = 2-3) в количестве 2157,73 кг (в т.ч. 25,22 кг Мо) или 1508,37 м3;
- смола с регенерации ВП-1п (ПОЕ = 5 мг-экв сухой смолы, коэффициент использования емкости = 0,5, Vуд = 3,3 см3/г (в т.ч. 0,009 кг Мо)
Емкость смолы по Мо в составе иона 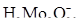 составляет 190 %.
составляет 190 %.
Количество смолы, необходимое на сорбцию:
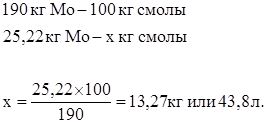
Количество ионов 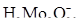 содержащихся в смоле, приходящей на сорбцию:
содержащихся в смоле, приходящей на сорбцию:
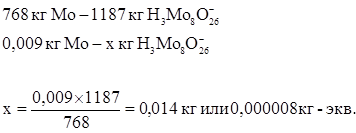
Тогда 0,0014 кг 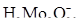 заменит:
заменит:

Количество смолы, приходящей на сорбцию:
13,27 – 0,000384 + 0,014 = 13,28 кг или 43,84 л.
Получено:
Количество ионов 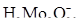 , перешедших в смолу:
, перешедших в смолу:
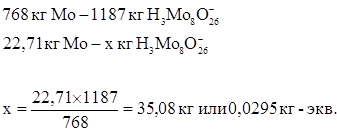
Тогда 35,08 кг  заменит:
заменит:
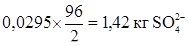 .
.
Количество смолы после сорбции:
13,28 – 1,42 + 35,08 = 46,94 кг или 43,35 л.
Количество пульпы после сорбции:
2157,73 + 1,42 – 35,08 = 2124,07 кг или 1830,74 л.
Тогда раствора:
2124,07 – 979,11 = 1144,96 кг
Концентрация молибдена в растворе:

Масса твердой фазы пульпы 3 составляет: 979,11 кг, а жидкой: 1178,62 кг.
Материальный баланс операции сорбции представлен в таблице 14.
Таблица 14 – Материальный баланс операции сорбции
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| Пульпа 3 | 2157,73 | 25,22 | 1508,37 | Смола | 46,94 | 22,71 | 43,35 |
| Смола | 13,27 | 0,01 | 43,80 | Пульпа 4 | 2124,07 | 2,52 | 1830,74 |
| Итого | 2191,89 | 25,23 | 1522,18 | Итого | 2191,89 | 25,23 | 1874,09 |
Промывка
Поступило:
- Смола в количестве 46,94 кг (в т.ч. 22,71 кг Мо) или 43,35 л.
Материальный баланс промывки представлен в таблице 15.
Таблица 15 - материальный баланс промывки
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Смола | 46,94 | 22,71 | 43,35 | Смола | 45,98 | 22,25 | 44,38 |
| Вода | 304,61 | _ | 304,61 | Маточный раствор | 305,57 | 0,46 | 305,57 |
| Итого | 351,55 | 22,71 | 347,96 | Итого | 351,55 | 22,71 | 349,95 |
Десорбция молибдена
Основная реакция десорбции (23):
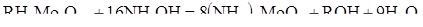 (23)
(23)
Поступило:
- смола ВП-1п в количестве 45,98 кг (в т.ч. 22,25 кг Мо) или 44,38 л;
- 10 % раствор аммиака (r = 0,93 г/см3) с избытком 25 % от СНК.
Количество NH4OH, необходимое на десорбцию:
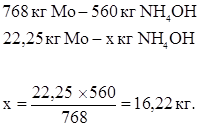
или в пересчете на аммиак:
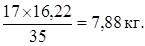
Тогда необходимое количество 10 % раствора аммиака:
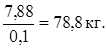
С учетом 25 %-го избытка суммарное количество 10 % раствора аммиака составит:
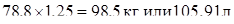
Или 25 % раствора аммиака:
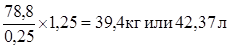
Получено:
Количество образовавшегося молибдата аммония:
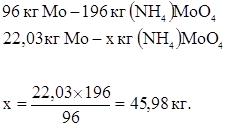
Количество образовавшейся воды:
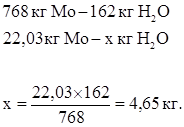
Количество ионов  , перешедших в раствор:
, перешедших в раствор:
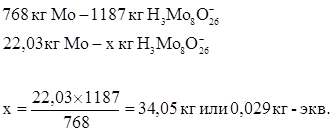
Количество ионов OH–, перешедших в смолу:
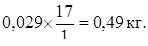
Количество NH4OH, вступившего в реакцию:
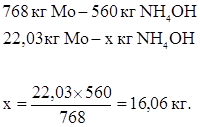
Всего в растворе аммиака:
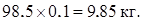
Пошло на десорбцию:
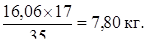
Тогда в растворе осталось аммиака:

или в пересчете на NH4OH:
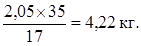
Количество смолы после десорбции:
45,98 – 34,05 + 0,49 = 12,42 кг или 41,47 л.
Количество раствора молибдата аммония:
98,5 – 16,06 + 45,98 + 4,65 = 132,07 кг или 105,90 л.
Концентрация MoO3 в растворе:
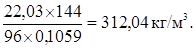
Материальный баланс десорбции молибдена представлен в таблице 16.
Таблица 16 – Материальный баланс десорбции молибдена
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| Раствор NH4OH | 98,5 | _ | 105,90 | Смола | 12,42 | 0,22 | 41,47 |
| Смола | 45,98 | 22,25 | 44,38 | Раствор (NH4)2MoO4 | 132,07 | 22,03 | 105,90 |
| Итого | 144,48 | 22,25 | 150,28 | Итого | 144,49 | 22,25 | 147,37 |
Промывка
Поступило:
- Смола в количестве 12,42 кг (в т.ч. 0,22 кг Мо) или 41,47 л.
Материальный баланс промывки представлен в таблице 17.
Таблица 17 - материальный баланс промывки
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| Смола | 12,42 | 0,22 | 41,47 | Смола | 12,36 | 0,04 | 41,47 |
| Вода | 100,00 | _ | 100,00 | Промвода | 100,06 | 0,18 | 100,00 |
| Итого | 112,42 | 0,22 | 141,47 | Итого | 112,42 | 0,22 | 141,47 |
Регенерация
Основная реакция регенерации (24):
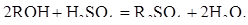 (24)
(24)
Поступило:
- смола в количестве 12,36 кг (в т.ч. 0,04 кг Мо) или 41,47 л;
- 10 % раствор серной кислоты (r» 1 г/см3) с 30 % избытком.
Из расчета десорбции молибдена известно, что смола содержит 0,49 кг (или 0,029 кг-экв) ионов OH–.
Тогда для регенерации необходимо ионов 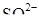 :
:
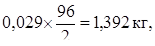
или в пересчете на H2SO4:
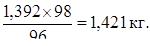
Количество 10 %-го раствора серной кислоты с 30 % избытком:

Получено:
Количество образовавшейся воды:
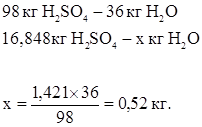
Также известно, что в раствор переходит 0,036 кг молибдена, т.е.

Тогда 0,06 кг 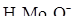 заменит:
заменит:
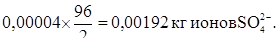
Масса раствора после рагенерации:
18,47 – 1,42 + 0,52 = 17,57 кг
Количество смолы после регенерации:
12,36 – 0,06 – 0,49 + 0,00192 + 1,392 = 13,26 кг или 43,8 м3.
Материальный баланс регенерации представлен в таблице 18.
Таблица 18 – Материальный баланс регенерации
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| Смола | 12,36 | 0,04 | 41,47 | Смола | 13,26 | 0,009 | 43,8 |
| Раствор серной кислоты | 18,47 | _ | 18,53 | Раствор | 17,57 | 0,031 | 18,53 |
| Итого | 30,83 | 0,04 | 60,00 | Итого | 30,83 | 0,04 | 62,33 |
Очистка от примесей
Поступило:
- Раствор с десорбции 132,07 кг (в т.ч. 22,03 кг Мо) или 105,9 л.
- Нитрат аммония (ρ=1,467 г/см3) с двукратным избытком
- Раствор аммиака с двукратным избытком
Основная реакция:
Na2HAsO4 + Mg(NO3)2 + NH4OH = Mg(NH4)AsO4 + 2NaNO3 + H2O (25)
В исходном сырье содержится 2,48 кг As. Принимаем, что раствор перешло 50 % As. Тогда в растворе содержится 1,24 кг As.
Количество нитрата магния необходимое для осаждения мышьяка:
186 кг Na2HAsO4 - 148 кг Mg(NO3)2
1,24 кг Na2HAsO4 - х
Х= 0,99 кг
С учетом избытка 2 кг.
Количество раствора аммиака необходимое для реакции:
186 кг Na2HAsO4 - 35 кг NH4OH
1,24 кг Na2HAsO4 - х
Х=0,23 кг
С учетом избытка» 0,5 кг.
Материальный баланс операции очистки от примесей представлен в таблице 19.
Таблица 19 - материальный баланс очистки от примесей
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Нитрат магния | 2,00 | _ | 1,36 | Осадок | 1,2 | 0,22 | 0,8 |
| Аммиак | 0,5 | _ | 0,5 |
Раствор на нейтрализацию |
133,37 |
21,81 | 107,57 |
| Раствор с десорбции | 132,07 | 22,03 | 105,90 | ||||
| Итого | 134,57 | 22,03 | 107,76 | Итого | 134,57 | 22,03 | 108,37 |
Осаждение ПоМА
Для простоты расчетов принимается, что полимолибдаты содержат, в основном ТМА.
Основные реакции осаждения ТМА (26) и (27):
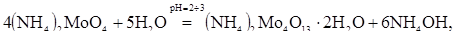 (26)
(26)
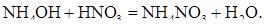 (27)
(27)
Поступило:
- раствор молибдата аммония (r = 1,247 г/см3, концентрация ~312,04 кг/м3 МоО3) в количестве 133,37 кг (в т.ч. 21,81 кг Мо) или 107,57 л;
- маточный раствор с перекристаллизации (r = 1,23 г/см3, концентрация 250 кг/м3 МоО3) в количестве 7,79 кг (в т.ч. 1,41 кг Мо) или 6,33л;
- 45 % раствор азотной кислоты (r = 1,28 г/см3) с 5 %-м избытком.
Получено:
Из расчета десорбции молибдена известно, что раствор молибдата аммония содержит 44,98 кг (NH4)2MoO4.
Тогда количество образовавшегося ТМА по реакции:

Количество ТМА в осадке:
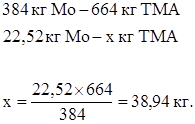
С учетом 25-%-ной влажности масса ТМА составляет 48,675 кг
Количество образующегося NH4OH:

Количество NH4OH, которое необходимо нейтрализовать:
12,05 + 4,22 = 16,27 кг.
Необходимое количество азотной кислоты (100 %-й) для нейтрализации:
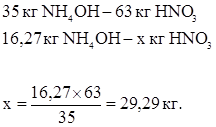
Тогда с учетом 5 %-го избытка, необходимо 45 %-й HNO3:
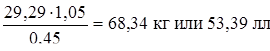
Избыток HNO3 в растворе:
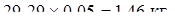
Количество образовавшегося NH4NO3 в результате нейтрализации:

Количество образовавшейся воды в результате нейтрализации:
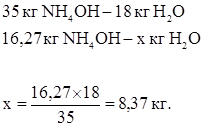
Количество полученной пульпы:
133,37 + 68,34 + 7,79 = 209,50 кг или 167,15 л.
Материальный баланс осаждения полимолибдатов представлен в таблице 20.
Таблица 20 – Материальный баланс осаждения полимолибдатов аммония
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| Раствор с очистки | 133,37 | 21,81 | 107,57 | Маточный раствор на произво удобрений | 160,82 | 0,70 | 141,17 |
| HNO3 | 68,34 | _ | 53,39 |
Полимолибдат (влажность 25 %) |
48,68 |
22,52 |
20,68 |
| Маточный раствор | 7,79 | 1,41 | 6,33 | ||||
| Итого | 209,50 | 23,22 | 167,29 | Итого | 209,50 | 23,22 | 161,85 |
Перекристаллизация
Поступило:
- кристаллы полимолибдатов аммония (r = 2,4 г/см3) в количестве 38,94 кг (в т.ч. 22,52 кг Мо), с учетом 25 % влажности их масса составляет 8,68 кг или 20,68 л;
- маточный раствор с перекристаллизации (r = 1,23 г/см3, концентрация 250 кг/м3 МоО3) в количестве 70,09 кг (в т.ч. 12,67 кг Мо) или 56,99 л;
- 5 % раствор аммиака (r = 0,88 г/см3).
Т.к. кристаллы ПоМА растворяют в маточном растворе и растворе аммиака до насыщения (т.е. плотности ~1,40–1,42), то необходимо добавить раствора аммиака 10,89 кг.
Или 25 % раствора аммиака:
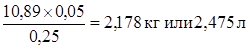
Получено:
- раствор (r = 1,40 г/см3, концентрация ~500 кг/м3 МоО3).
После охлаждения из раствора выпадают кристаллы ПМА (r = 2,4 г/см3).
Количество ПМА в осадке:
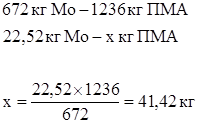
С учетом 25 % влажности количество ПМА:
41,42 × 1,25 = 51,775 кг или 21,57 л
Материальный баланс перекристаллизации представлен в таблице 21.
Таблица 21 – Материальный баланс перекристаллизации
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| ПоМА | 48,68 | 22,52 | 20,68 | Маточный раствор | 77,88 | 14,07 | 63,32 |
| Раствор аммиака | 10,89 | _ | 12,37 |
ПМА |
51,77 |
21,11 |
21,57 |
| Маточный раствор | 70,09 | 12,67 | 56,99 | ||||
| Итого | 129,65 | 35,19 | 90,22 | Итого | 129,65 | 35,19 | 84,89 |
Промывка
Поступило:
- ПМА в количестве 51,77 кг (в т.ч. 21,11 кг Мо) или 17,26 л.
Материальный баланс промывки представлен в таблице 22.
Таблица 22 - материальный баланс промывки
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
| ПМА | 51,77 | 21,11 | 21,57 | ПМА | 51,39 | 20,90 | 21,41 |
| Вода | 50,00 | _ | 50,00 | Промвода | 50,38 | 0,21 | 50,16 |
| Итого | 101,77 | 21,11 | 71,57 | Итого | 101,77 | 21,11 | 71,57 |
Сушка
Поступило:
- ПМА в количестве 51,39 кг (в т.ч. 20,90 кг Мо) или 21,41 л.
Материальный баланс сушки представлен в таблице 23.
Таблица 23 - материальный баланс сушки
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
|
ПМА | 51,39 | 20,90 | 21,41 | Готовый продукт (влажность 5 %) | 43,49 | 20,90 | 18,12 |
| Пар | 7,90 | - | 98,75 | ||||
| Итого | 51,39 | 20,90 | 21,41 | Итого | 51,39 | 20,90 | 116,87 |
Сгущение-отстаивание
Масса твердой фазы пульпы 4 составляет: 797,11 кг, а жидкой: 1144,96 кг.
Таблица 24 - материальный баланс операции Сгущение-отстаивание
| Поступило | Получено | ||||||
| Материал | кг | Mo, кг | Объем, л | Продукт | кг | Mo, кг | Объем, л |
|
Пульпа 4 с сорбции |
2124,07 |
2,52 |
1830,74 | Сливной раствор | 225,51 | 1,51 | 192,06 |
| Шлам | 1898,56 | 1,01 | 1637,68 | ||||
| Итого | 2124,07 | 2,52 | 1830,74 | Итого | 2124,07 | 2,52 | 1830,74 |
 2020-01-14
2020-01-14 489
489








