В последнее время липосомы находят все большее признание в мире как перспективные носители лекарственных веществ, поскольку многочисленные клинические испытания показали, что лекарства, вводимые в составе липосом, более эффективны и менее токсичны, чем вводимые в свободном виде.
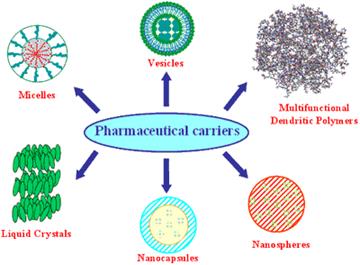
Рис. 1
На рисунке 1. показаны различные по своей природе транспортные частицы для лекарств.
Достоинства липосом как носителей лекарств очевидны: полученные из природных фосфолипидов липосомы в отличие от полимерных систем доставки лекарств полностью биодеградируемы и биосовместимы, пригодны для включения в них многих фармакологических агентов, в том числе ферментов, гормонов, витаминов, антибиотиков, иммуномодуляторов, цитостатиков. Включенные в липосомы лекарственные вещества становятся более устойчивыми в организме, так как изолированы липидной мембраной от повреждающих воздействий внешних условий, в частности от разрушения в желудочно-кишечном тракте, и в свою очередь в меньшей степени оказывают общее токсическое действие на организм. Уникальной особенностью липосом является возможность доставки лекарственных препаратов внутрь клеток, с которыми они взаимодействуют путем слияния или эндоцитоза. Модифицируя мембрану липосом молекулами, обеспечивающими «узнавание» клетки или органа-мишени, можно осуществлять направленную транспортировку лекарств.
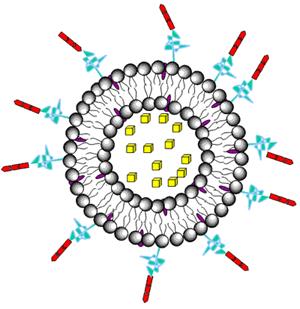
Рисунок 2. Схематичное изображение липосомы с лекарством
Особый интерес вызывает возможность орального применения липосомальных белковых препаратов, поскольку их инъекционные лекарственные формы быстро деградируют в желудке. Хотя механизм всасывания липосомальных препаратов в желудочно-кишечном тракте до конца не ясен, сообщений об их эффективности при пероральном приеме в литературе достаточно много. Так, например, несмотря на неоднозначные результаты по пероральному применению липосомального инсулина при лечении сахарного диабета, исследования в этом направлении продолжаются, а некоторые фирмы предполагают наладить промышленный выпуск этого препарата. Разработанный в дочернем государственном унитарном производственном предприятии (ДГУ ПП) «Вектор-Фарм» ГНЦ ВБ «Вектор» г. Новосибирска липосомальный генноинженерный альфа-2b интерферон (Липоферон) для энтерального применения (для приема внутрь) оказался эффективен при многих вирусных и ассоциированных с ними заболеваниях человека. В ряде клинических испытаний, проведенных в ведущих медицинских центрах страны, таких как ЦНИИ эпидемиологии МЗ РФ, НИИ педиатрии и детской хирургии МЗ РФ, ГНЦ Институт иммунологии МЗ РФ, Институт гриппа, были получены положительные результаты у взрослых и детей при лечении острого и хронического гепатита В, как свободного, так и ассоциированного с гломерулонефритом, гриппа, ОРЗ, атопических заболеваний, таких как риноконъюнктивит и бронхиальная астма.
Спектр терапевтического применения Липоферона для перорального применения постоянно расширяется, так как продолжающиеся клинические испытания выявляют все новые нозологические формы заболеваний, при лечении которых он эффективен. Очень важно, что липосомальный интерферон в пероральной форме хорошо переносится больными. При его применении не обнаруживаются побочные эффекты, сопровождающие парентеральное применение интерферона, такие как повышение температуры, озноб, утомляемость, кожные высыпания, лейко- и тромбоцитопения. Естественный путь введения — «peros» — делает препарат незаменимым в педиатрической практике. Немаловажно и то, что при пероральном приеме липосомальных препаратов отсутствует риск передачи вирусов СПИДа и гепатита.
Использование липосом оптимально при необходимости направленной транспортировки лекарственного вещества к органам ретикулоэндотелиальной системы (селезенка, печень и т.д.). В настоящее время тщательно разработана система применения и лечения антибактериальными препаратами в липосомах так называемых «инфекций РЭС». Доказана эффективность подобных препаратов при многих заболеваниях (лейшманиоз, сальмонеллез, брюшной тиф, бруцеллез, малярия и др.), появились работы по использованию липосомальных противовирусных препаратов при герпесе, вирусном гепатите, лихорадке долины Рифт, ВИЧ-инфекции в эксперименте на животных. При парентеральном введении распределение липосом в организме зависит от состава липосомальной мембраны, их размера, заряда, других химических и физических параметров везикул и иммобилизованных в них веществ, а также от способа введения. Так, например, после подкожного введения основное количество липосом депонируется в месте введения и элиминируется оттуда преимущественно лимфогенным путем. Таким образом, местное введение липосомальных препаратов является оптимальным способом их доставки в регионарные лимфоузлы. При внутримышечном введении липосомы способны создавать депо препарата в месте введения, скорость элиминации из депо зависит от размера и свойств липосом и составляет от нескольких часов (если липосомы мелкие) до нескольких дней (если крупные). Мелкие бислойные липосомы в отличие от крупных при внутрибрюшинном или внутримышечном введении гораздо быстрее проникают в кровеносное русло, что указывает на ограниченную способность последних проходить через капилляры и мембраны сосудов. При внутривенном введении мелкие липосомы выводятся из кровотока медленнее, чем крупные.
Для повышения тропности (способность воздействовать на что-либо) липосом к определенным органам и тканям их изготавливают из фосфолипидов, изолированных из этих органов, или фиксируют на поверхности специфические антитела против соответствующих тканевых антигенов, или применяют так называемые молекулы-посредники, обладающие двумя типами сродства: с одной стороны — к клеткам макроорганизма, с другой — к липосоме. Как отмечают исследователи, липиды в определенной степени участвуют в «узнавании» клеток, поскольку каждому типу мембран соответствует определенное, характерное только для него соотношение полярных липидов. В процессе «узнавания» важную роль играют также гликолипиды (ганглиозиды), участвующие в межклеточных взаимодействиях и являющиеся специфическими рецепторами ряда биологически активных веществ. То есть механизм взаимодействия липосом с клетками определяют не только фосфолипиды, но и ганглиозиды, входящие в состав липосом. Изучение распределения липосом, содержащих фосфатидилхолин, холестерин и гликолипид, при внутривенном введении в организм показало, что наилучшим гликолипидом для липосом в отношении их переноса в ткани головного мозга и печени является сульфатид, в ткани селезенки — ганглиозиды, в ткани легких — сфингомиелин. Так, например, человеческий a-интерферон, иммобилизованный в липосомы, мембрана которых построена из фосфатидилхолина, холестерина и сульфатида, после внутрибрюшинного введения в большей степени обнаруживается в крови, печени, селезенке и опухолевой ткани мозга.
Если необходимо локальное воздействие на клинический процесс, то для исключения системного влияния на организм целесообразно местное применение лекарственных препаратов.
Липосомальные препараты по сравнению с традиционными лекарственными формами для наружного применения, такими как мази и гели, обладают большей способностью проникать в кожу и волосы, а потому они более доступны для живых клеток-мишеней. Установлено, что липосомы интенсифицируют процессы взаимодействия активных веществ с кожей при лечебной наружной терапии, что приводит к повышению терапевтической эффективности иммобилизованных в них лекарственных веществ. Вероятнее всего, такой эффект вызван слиянием липосом с липидными ламеллами, не доходя до базального слоя, и высвобождением их внутреннего содержимого. Подвижные липиды липосом встраиваются в липидные ламеллы, увеличивая таким образом «жидкостность» барьера, что улучшает проницаемость. Другим важным путем проникновения липосом и их содержимого вглубь кожи являются волосяные фолликулы. Эффективность трансдермального липосомального переноса лекарственных веществ можно усиливать, используя методы ионо- и фонофореза.
 2020-01-14
2020-01-14 221
221








