Почти все металлы реагируют с кислотами, образуя соли. Характер взаимодействия металла с кислотой зависит от активности металла, его свойств и концентрации кислоты.
При действии кислоты на металл роль окислителя играет или ион водорода ( , разбавленная
, разбавленная  ), или кислотный остаток кислородсодержащей кислоты (
), или кислотный остаток кислородсодержащей кислоты ( ,
,  – концентрированная).
– концентрированная).
Взаимодействие металлов с соляной кислотой.
С соляной кислотой взаимодействуют металлы, стоящие в ряду напряжений до водорода.
 .
.


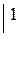
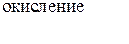
Вывод: окислителем являются катионы водорода, которые принимают электроны от атома металла.
Взаимодействие металлов с азотной кислотой
Концентрированная и разбавленная азотная кислота окисляет металлы без выделения водорода, так как в ней окислителем является нитрат-ион (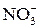 ).
).
Восстановление азотной кислоты различной концентрации при взаимодействии с металлами разной активности можно представить в виде схемы.








Согласно схеме степень окисления азота при взаимодействии кислоты с металлами меняется от +5 до -3.
Рассмотрим несколько примеров.
1.  .
.
Коэффициенты в уравнении реакции подбираем ионно-электронным методом.
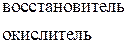

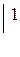
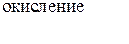

или  .
.
2.  .
.
Разбавленная азотная кислота при взаимодействии с неактивными металлами восстанавливается до  , образуется соль
, образуется соль  и вода.
и вода.
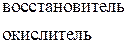


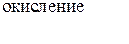

или 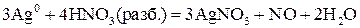 .
.
3.  .
.
При взаимодействии активных металлов с разбавленной азотной кислотой образуется соль, вода и 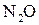 или
или  .
.
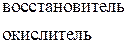

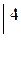
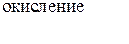
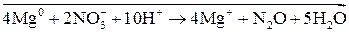
или 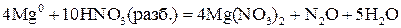 .
.
 .
.
При взаимодействии активных металлов с очень разбавленной азотной кислотой образуется соль, вода и аммиак или нитрат аммония.
или 
Вывод: окислителем в азотной кислоте является нитрат-анион. Концентрированная азотная кислота пассивирует 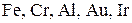
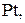 …
…
Следует иметь в виду, что во многих случаях при действии азотной кислоты на металлы образуется смесь различных азотсодержащих соединений, в которых преобладает какое-либо из них.
 2020-04-12
2020-04-12 243
243








