Состояние данной массы полностью определено, если известны давление, температура и объем газа. Эти величины называют параметрами состояния газа.
Уравнение, связывающее параметры состояния, называют уравнением состояния.
Для произвольной массы газа единичное состояние газа описывается уравнением Менделеева— Клапейрона:
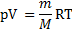
где р — давление, V — объем, m — масса, М — молярная масса,
 R — универсальная газовая постоянная. R = 8,31 Дж/моль • К/
R — универсальная газовая постоянная. R = 8,31 Дж/моль • К/
Особую роль в физике и технике играют три процесса: изотермический, изохорным и изобарный.
Изопроцессом  называют процесс, происходящий с данной массой газа при одном постоянном параметре — температуре, давлении или объеме. Из уравнения состояния как частные случаи получаются законы для изопроцессов.
называют процесс, происходящий с данной массой газа при одном постоянном параметре — температуре, давлении или объеме. Из уравнения состояния как частные случаи получаются законы для изопроцессов.
Изотермическим называют процесс, протекающий при постоянной температуре. Для газа данной массы произведения давления на оббьем постоянно, при неизменной температуре- закон Бойля-Мариотта
Т = const.. pV = const.
P1V1=P2V  2
2
Изохорным называют процесс, протекающий при постоянном объеме. Для газа данной массы отношение давления к температуре постоянно при постоянном объеме-закон Шарля.
 V = const. = const.
V = const. = const.
 Изобарным называют процесс, протекающий при постоянном давлении. Для газа данной массы отношении объема к температуре постоянно при постоянном объеме- закон Гей-Люссака.
Изобарным называют процесс, протекающий при постоянном давлении. Для газа данной массы отношении объема к температуре постоянно при постоянном объеме- закон Гей-Люссака.
 р = const == const.
р = const == const.
 2020-04-07
2020-04-07 1097
1097
