Строение и особенности альдегидов.
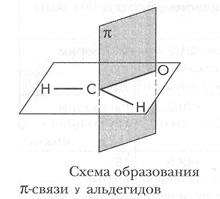
В альдегидной группе между атомами углерода и кислорода имеются две связи, одна из них σ, другая – π связь, подобная той, что образуется у алкенов. Двойная связь способна разрываться. Альдегидам присуща изометрия углеродного скелета.
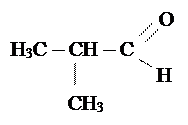
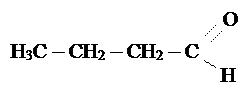 Например,
Например,
бутаналь 2 – метилпропаналь
Гомологический ряд предельных альдегидов.
| молекулярная формула | 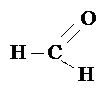 структурная формула структурная формула
| названия | t° кипения |
| СH2O |
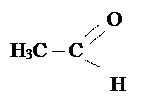
| Метаналь, муравьиный альдегид, формальдегид, | – 21,2 t° |
| C2H4O |
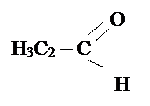
| Этаналь, уксусный альдегид, ацетальдегид, | +20,2 t° |
| C3H6O | Пропаналь, пропионовый альдегид, | +48,8 t° | |
| C4H8O | 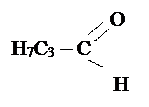
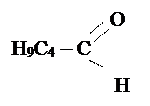
| Бутаналь, масляный альдегид, | +73 t° |
| C5H10O | Пентаналь, валериановый альдегид, | +103 t° |
Важнейшими представителями альдегидов являются формальдегид и ацетальдегид.
Формальдегид – газ с резким запахом, единственный газообразный представитель альдегидов. Хорошо растворяется в воде. Водный раствор его называют формалином. Но! Формалин опасен для здоровья. Он способен вызывать раздражение слизистых тканей и действует на нервную систему.
Ацетальдегид – жидкость с характерным запахом зеленой листвы. Хорошо растворяется в воде. Но! Очень токсичен. Он способен соединяться с белками и подавлять дыхательные процессы в клетках.
Номенклатура альдегидов.
Международная (систематическая, заместительная). а) Названия образуются от названия, соответствующего алкана с таким же числом атомов углерода с добавлением суффикса – аль. б) Нумерацию самой длинной цепи начинают от атома углерода альдегидной группы. в) Перед названием указывают положения и названия заместителей в цепи.
O
3 2 1 ⁄⁄
Например: CH3- CH- C – H 2- метилпропаналь.
|
CH3
1. Тривиальная (историческая). Названия происходят от названий соответствующих органических кислот, в которые они превращаются при окислении.
O
⁄⁄
1. H – C – H - муравьиный альдегид (формальдегид).
O
⁄⁄
2. CH3 – C – H - уксусный альдегид (ацетальдегид).
Изомерия альдегидов.
В пределах класса альдегидов возможен только один вид изомерии – изомерия углеродного скелета (углеродной цепи). Межклассовыми изомерами альдегидов являются кетоны.
Физические свойства:
В молекуле альдегида или кетона вследствие большей электроотрицательности атома кислорода по сравнению с углеродным атомом связь С=0 сильно поляризована за счет смещения электронной плотности п -связи к кислороду.
Альдегиды и кетоны — полярные вещества с избыточной электронной плотностью на атоме кислорода. Низшие члены ряда альдегидов и кетонов (формальдегид, уксусный альдегид, ацетон) растворимы в воде неограниченно. Их температуры кипения ниже, чем у соответствующих спиртов. Это связано с тем, что в молекулах альдегидов и кетонов в отличие от спиртов нет подвижных атомов водорода и они не образуют ассоциатов за счет водородных связей. Низшие альдегиды имеют резкий запах, у альдегидов, содержащих от четырех до шести атомов углерода в цепи, неприятный запах, высшие альдегиды и кетоны обладают цветочными запахами и применяются в парфюмерии.
Метаналь (муравьиный альдегид) – бесцветный газ с резким запахом. Раствор метаналя в воде (35-40%) называется формалином.
C2 – C11 - жидкости
С12 - … - твердые вещества
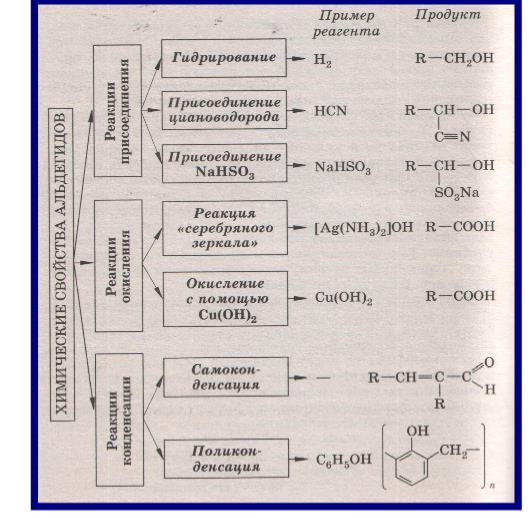
Химические свойства альдегидов.
 2020-05-12
2020-05-12 535
535







